溶液和胶体的关键区别在于,胶体中的颗粒通常比溶液中的溶质颗粒大。
混合物是不同物质的集合,它们在物理上结合,但不以化学方式结合。混合物显示出不同于单个物质的物理或化学性质。溶液和胶体是两种性质不同的混合物。在这些混合物中,固体、气体或液体物质以不同的比例混合。
目录
1. 概述和主要区别
2. 什么是解决方案
3. 什么是胶体
4. 并列比较-溶液与胶体的表格形式
5. 摘要
什么是解决方案(the solution)?
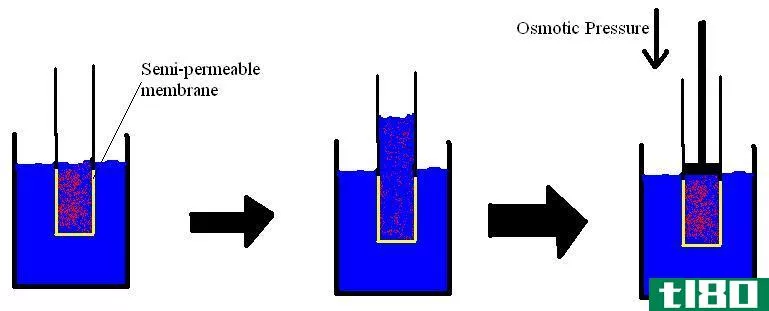
溶液是两种或两种以上物质的均匀混合物。我们称之为均相混合物,因为在整个溶液中组成是均匀的。溶液的成分主要有两种,溶质和溶剂。溶剂溶解溶质并形成均匀的溶液。所以,通常溶剂量比溶质量高。
溶液中的所有粒子都有分子或离子的大小,所以我们不能用肉眼观察它们。如果溶剂或溶质能吸收可见光,溶液可以有颜色。然而,解决方案通常是透明的。溶剂可以是液态、气态或固态。最常见的溶剂是液体。在液体中,我们认为水是一种通用溶剂,因为它比任何其他溶剂都能溶解许多物质。我们可以在液体溶剂中溶解气体、固体或任何其他液体溶质。在气体溶剂中,只有气体溶质可以溶解。

图01:不同的解决方案
然而,在一定量的溶剂中,我们可以添加的溶质数量是有限制的。如果我们向溶剂中加入最大量的溶质,溶液就会饱和。如果溶质含量很低,溶液就会变稀;如果溶液中含有大量的溶质,溶液就会变成浓缩溶液。通过测量溶液的浓度,我们可以知道溶液中溶质的含量。
什么是胶体(colloid)?
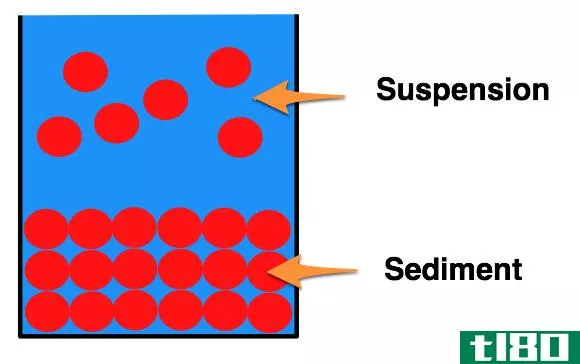
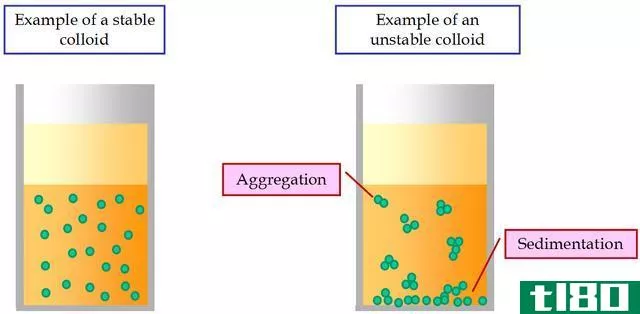
胶体溶液以均匀混合物的形式存在,但有时它是不均匀的(如牛奶、雾)。与溶液和悬浮液中的颗粒相比,胶体溶液中的颗粒尺寸中等(大于分子)。但是,就像溶液中的微粒一样,肉眼看不见,我们不能用滤纸过滤。
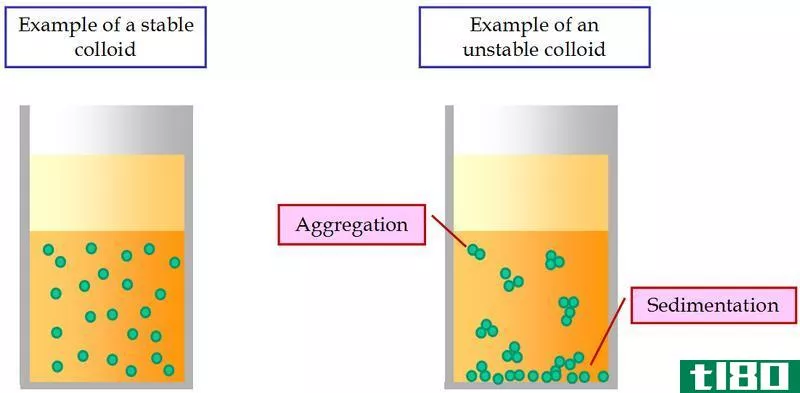
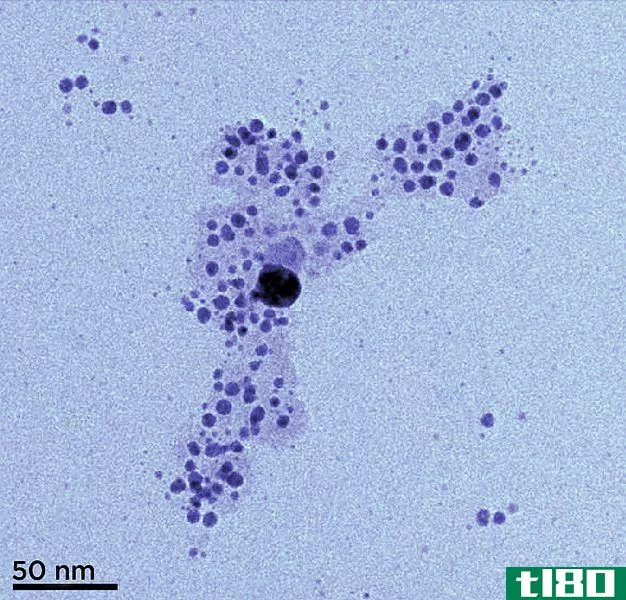
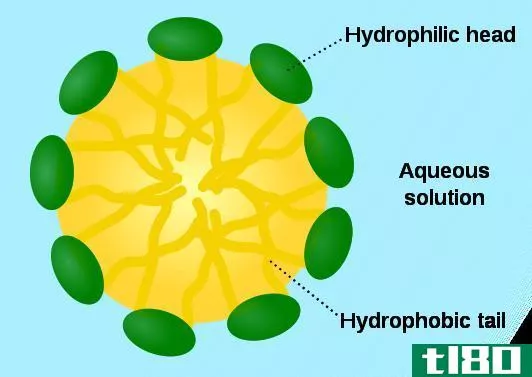
图02:两种胶体
我们称胶体中的粒子为分散物质,分散介质类似于溶液中的溶剂。根据分散的物质和介质的不同,有不同类型的胶体。例如,在液体中形成泡沫(例如,在液体中形成泡沫)。如果两种液体结合在一起,就会形成乳状液(如牛奶)。分布在胶体介质中的粒子如果静止不动,就不会沉淀下来。胶体溶液是半透明或不透明的。有时胶体中的颗粒可以通过离心或凝固分离出来。例如,当我们提供热量或添加酸时,牛奶中的蛋白质会凝结。
解决方案(solution)和胶体(colloid)的区别
溶液和胶体是两种含有两种或两种以上物质的混合物。这些混合物是液态的。然而,溶液和胶体的关键区别在于,胶体中的颗粒通常比溶液中的溶质颗粒大。此外,与胶体相比,溶液是完全均匀的,胶体也可以作为不均匀混合物存在。因此,这是溶液和胶体的另一个区别。此外,溶液和胶体的另一个区别是,胶体不是不透明的就是半透明的,而是溶液是透明的。

总结 - 解决方案(solution) vs. 胶体(colloid)
溶液和胶体都是两种或两种以上物质的混合物。溶液和胶体的关键区别在于,胶体中的颗粒通常比溶液中的溶质颗粒大。
引用
1“解决方案”,维基百科,维基媒体基金会,2018年9月21日。可在此处查阅2。歌词。“胶体”,化学剧本,歌词,2017年1月9日。此处提供
2歌词。“胶体”,化学剧本,歌词,2017年1月9日。