碳12和碳14的关键区别在于,碳12的原子核中有6个中子,而碳14有8个中子。
碳12和碳14是碳原子的同位素。质子总是有6个原子。它通常也有6个中子,这就是为什么我们称它为碳12。但有时有8个中子,而不是6个,当它变成碳14时。在化学反应中,碳12和碳14的行为方式相似。一般情况下,碳以c12状态存在,但偶尔也以c14的形式存在。
目录
1. 概述和主要区别
2. 碳12是什么
3. 碳14是什么
4. 并列比较——碳12与碳14的表格形式
5. 摘要
什么是碳12(carbon 12)?
碳12是质量为12的最常见的天然碳同位素。它是公认的原子质量单位比例尺的基础。这种碳的丰度在99%左右。
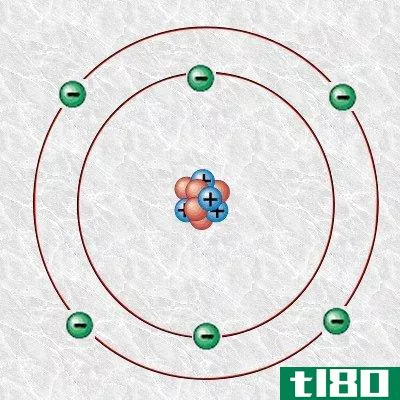
图1:碳原子
此外,这个碳原子由6个质子、6个电子和6个中子组成。我们可以科学地把碳12表示为12C,它的同位素质量是12u。
什么是碳14(carbon 14)?
碳14是碳的一种常见同位素。我们称之为“放射性碳”,因为它是一种放射性碳同位素。这个原子的原子核包含6个质子、6个电子和8个中子。它的同位素质量是14U,而且碳14是非常稀有的,它的丰度大约是万亿分之一。
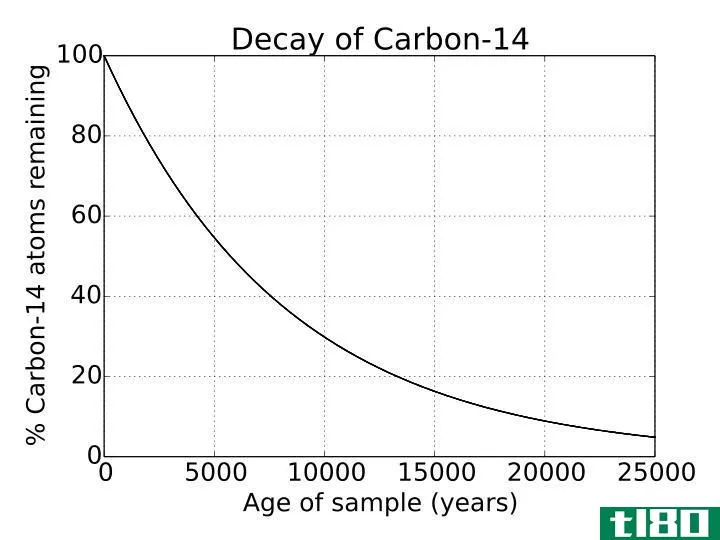
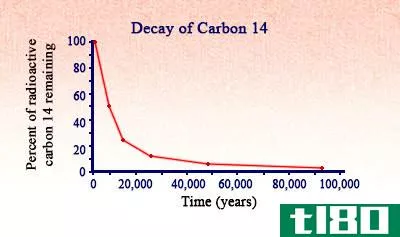
图2:碳14的放射性衰变
由于碳14是碳原子的不稳定同位素,它经历了放射性衰变。这是一个过程,每个不稳定同位素都会发生,这是一个自然过程。它是C14的一种独特性质,用于确定有数千年历史的物体,在考古学中被广泛使用。c14的半衰期是5730年。
碳12(carbon 12)和碳14(carbon 14)的区别
c12和c14是碳原子的同位素。碳12和碳14的关键区别在于,碳12的原子核中有6个中子,而碳14有8个中子。由于质子和中子的重量相同,有8个中子,c14比c12重20%。此外,由于c12和c14有相同数量的质子,它们的原子序数是相同的,但由于中子数的不同,它们的原子量也不同。所以,这是c12和c14之间的显著区别。
此外,当涉及到核反应时,c12和c14的表现也不同。此外,c12和c14之间的另一个区别是c12在地壳中含量丰富,而c14很少见。此外,c12是碳的稳定同位素,c14是碳原子的不稳定同位素,经过放射性衰变。

总结 - 碳12(carbon 12) vs. 碳14(carbon 14)
碳12和碳14是碳原子的同位素。碳原子总是有6个质子,但是中子的数量可以变化。例如,碳12和碳14是具有不同中子数的碳的不同同位素。因此,碳12和碳14的关键区别在于碳12的原子核中有6个中子,而碳14有8个中子。
引用
1“碳。”不列颠百科全书,不列颠百科全书,2019年2月7日,可在此处查阅。