活化络合物理论与碰撞理论的主要区别在于,活化络合物理论在描述反应速率时更准确可靠,而碰撞理论则不太可靠。
活化络合物理论和碰撞理论是描述化学反应热力学的两个重要概念。这些理论可以用来预测化学反应的反应速率。活化络合物理论又称过渡态理论。然而,激活复合物理论被认为比碰撞理论更精确。
目录
1. 概述和主要区别
2. 什么是激活复合理论
3. 什么是碰撞理论
4. 并列比较-激活的复杂理论与表格形式的碰撞理论
5. 摘要
什么是激活复合物理论(activated complex theory)?
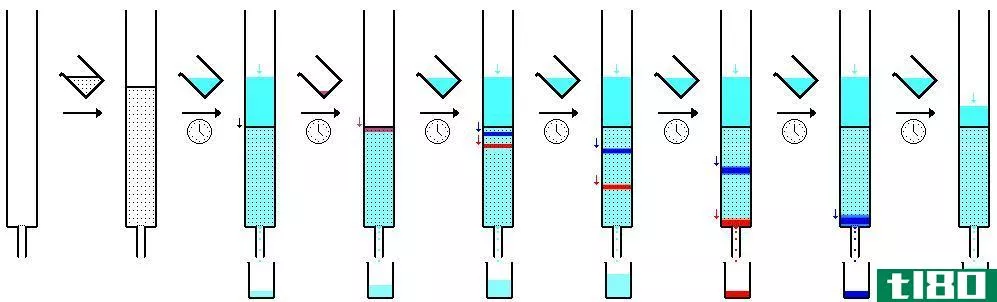
活化络合物理论是描述反应物和最终产物之间存在过渡状态的热力学理论。因此,它也被称为过渡态理论或TST理论。与碰撞理论相比,该理论提供了更准确可靠的信息。这个理论是亨利·艾林在1935年提出的。
活化络合物理论描述了反应混合物的活化能(Ea)和涉及过渡态的热力学性质。这个理论是碰撞理论的发展,它使用了阿伦尼斯方程的基础。此外,该理论还描述了统计频率因子v,它是该理论的一个基本因子。
根据活化络合物理论,反应物的状态和反应混合物的产物之间存在一个中间状态。它被称为过渡态,其中包含一种活化的复合物。这种活化的络合物是由反应物的组合形成的。根据这一理论,我们需要考虑一些主要的事实来确定反应是否会发生。事实如下:
- 过渡态活化络合物的浓度
- 这种活化复合物的分解速率
- 活化络合物的分解方式(络合物可能分解形成产物或再次形成反应物)
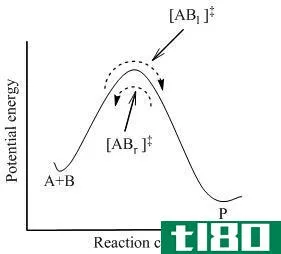
除此之外,活化络合物理论还提出了化学反应活化能的概念。活化能是反应的能量屏障;一定量的能量对于化学反应的发生是必不可少的。活化络合物是一种不稳定的高能络合物,在反应过程中具有最大的能量。如果反应混合物得到的能量量等于这个活化能,那么反应混合物就可以克服势垒,得到反应产物。
什么是碰撞理论(collision theory)?
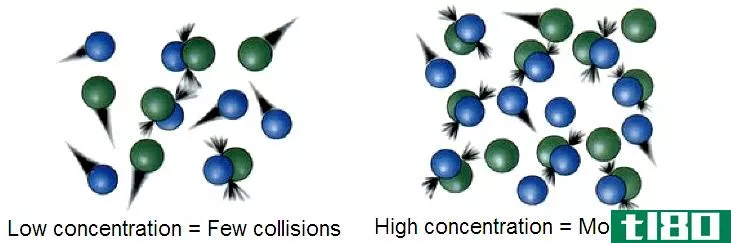
碰撞理论是描述化学反应通过反应物之间的碰撞形成产物的热力学理论。根据这一理论,如果两个分子为了发生化学反应而相互碰撞,那么影响碰撞容易程度的因素对于预测反应的进展是很重要的。E、 向反应混合物提供的能量越多,反应物移动越快,相互碰撞。同样,高温条件会导致反应物之间的更多碰撞和高反应速率。
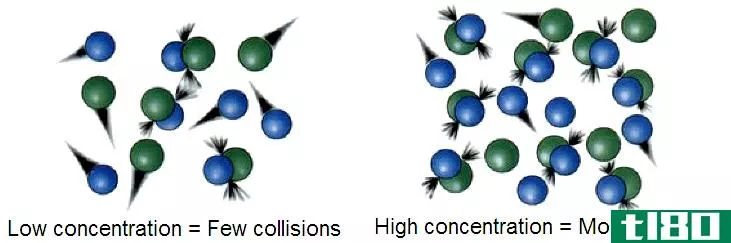
在碰撞理论中,反应物分子相互碰撞的速率称为碰撞频率z,它给出了每单位时间内的碰撞单位。根据碰撞理论,反应物混合物的能量和反应物的浓度影响反应速率。然而,为了使反应物之间发生成功的碰撞,反应物必须以足够的动能相互碰撞,以打破反应物中的化学键并形成新的化学键,形成最终产物。这个能量被称为活化能。
激活复合物理论(activated complex theory)和碰撞理论(collision theory)的区别
活化络合物理论和碰撞理论是重要的热力学理论。活化络合物理论与碰撞理论的主要区别在于,活化络合物理论在描述反应速率时更准确可靠,而碰撞理论则不太可靠。
下面的信息图表更详细地列出了激活复杂理论和碰撞理论之间的区别。

总结 - 激活复合物理论(activated complex theory) vs. 碰撞理论(collision theory)
活化络合物理论和碰撞理论是重要的热力学理论。活化络合物理论与碰撞理论的主要区别在于,活化络合物理论在描述反应速率时更准确可靠,而碰撞理论则不太可靠。
引用
1“激活的复合体”,维基百科,维基媒体基金会,2020年6月18日,可在这里查阅。“9.7:反应速率理论”,化学图书馆,图书馆,2020年9月1日,可在这里查阅。
2“9.7:反应速率理论”,《化学图书馆》,图书馆,2020年9月1日,