原子与分子
单个元素在自然条件下很难稳定。它们在它们之间或与其他元素形成各种组合以存在。当这种情况发生时,单个元素的性质会发生变化,并产生新的混合物。
原子
原子是所有现存物质的组成部分。它们太小了,我们甚至不能用肉眼观察。通常原子在埃范围内。原子是由原子核组成的,原子核有质子和中子。除了中子和质子外,原子核中还有其他小的亚原子粒子,还有电子绕着原子核绕轨道旋转。原子中的大部分空间是空的。带正电荷的原子核(质子带正电荷)和带负电荷的电子之间的吸引力维持着原子的形状。
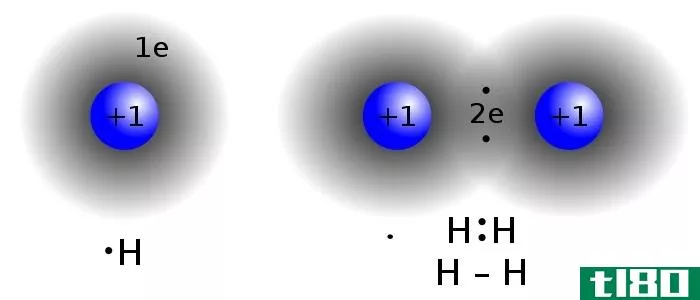
同类原子有相似的质子和电子。同一类型的原子可能会因中子的数量不同而有所不同,这些被称为同位素。原子可以以各种方式与其他原子结合,从而形成数千个分子。除诺贝尔气体外,所有元素都有一个双原子或多原子的排列方式变得稳定。根据它们的给电子或吸电子能力,它们可以形成共价键或离子键。有时,原子之间有很弱的吸引力。
原子的结构是由许多科学家进行的一系列实验确定的。根据道尔顿理论,
- 所有的物质都是由原子组成的,原子不能进一步分解。
- 给定元素的所有原子都是相同的。
- 化合物是由两个或两个以上的原子结合而成的。
- 原子不能被**或毁灭。化学反应是原子的重新排列。
然而,随着对原子的更先进的发现,道尔顿理论也有一些修改。
分子
分子是由同一元素(如O2、N2)或不同元素(H2O、NH3)的两个或多个原子化学键合而成的。分子不带电荷,原子由共价键结合。分子可以很大(血红蛋白)也可以很小(H2),这取决于连接的原子数。分子中原子的类型和数目由分子式表示。
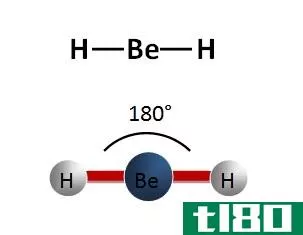
用经验公式给出了原子的整数比。例如,C6H12O6是葡萄糖的分子式,CH2O是经验式。分子质量是考虑分子式中给定的原子总数而计算的质量。每个分子都有自己的几何结构。分子中的原子以最稳定的方式排列,具有特定的键角和键长,以尽量减少排斥和张力。
- 原子是单个元素,而分子是两个或两个以上的原子结合在一起。
- 分子在原子之间有键。它们有分子内和分子间的力,但原子只有原子间的力。
- 分子本身通常是稳定的,而原子是不稳定的(除了惰性气体)。因此,与分子相比,自然界中找不到单原子。