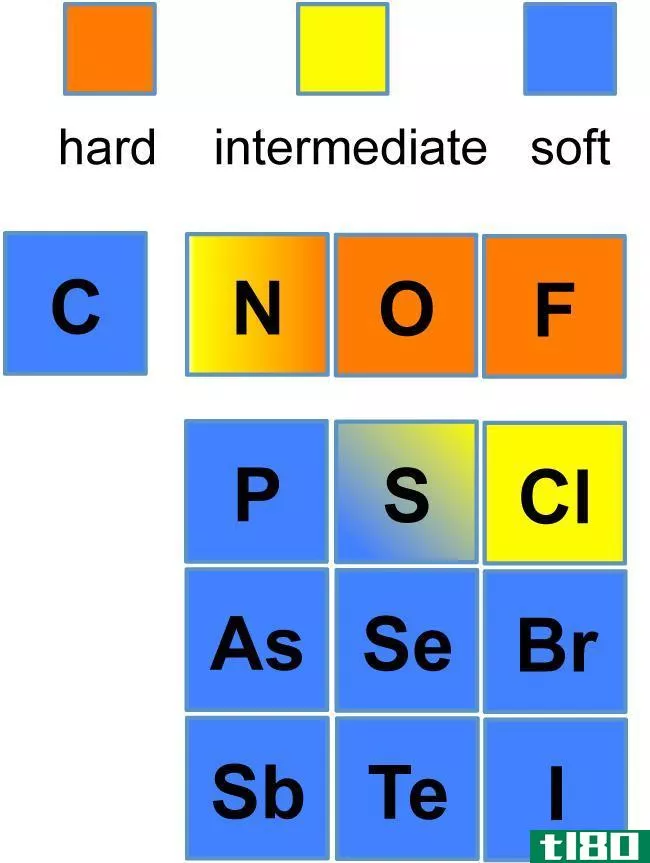
碱与碱的主要区别在于,第1组元素被归为碱元素,而任何具有基本性质的元素或化合物都被归为碱。
我们经常交替使用碱这个词来表示高碱性溶液和碱金属。在这里,碱是指元素周期表第1组的碱金属。然而,碱基可以指任何具有基本性质的元素、分子、离子等。
目录
1. 概述和主要区别
2. 什么是碱
3. 什么是基础
4. 并列比较-以表格形式列出碱与碱
5. 摘要
什么是碱(alkali)?
碱是元素周期表第1组金属的常用术语。这些也被称为碱金属。虽然H也在这个组中,但有点不同;它的行为与这个组的其他成员不同。因此,锂(Li)、钠(Na)、钾(K)、铷(Rb)、铯(Cs)和弗朗(Fr)都属于这一类。
碱金属是柔软、有光泽、银色的金属。它们的外层都只有一个电子,它们喜欢去掉这个电子形成+1阳离子。当最外层的电子被激发时,它回到基态,同时在可见光范围内发射辐射。这种电子的发射很容易;因此,碱金属非常活泼。此外,在周期表的第1组,反应性增加。

图01:氢氧化钠-碱金属的氢氧化物
这些金属与其他负电荷原子形成离子化合物。更准确地说,碱是指碱金属的碳酸盐或氢氧化物。它们也有基本属性。它们的味道苦,滑,并与酸反应,以中和它们。
什么是基础(base)?
定义
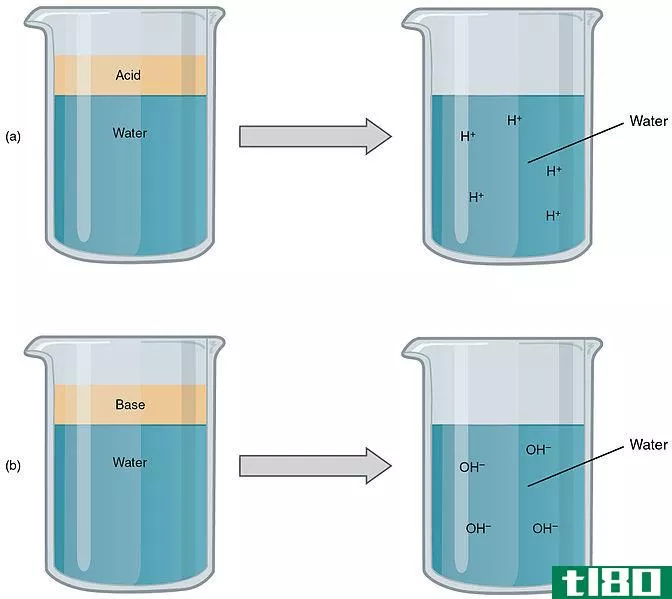
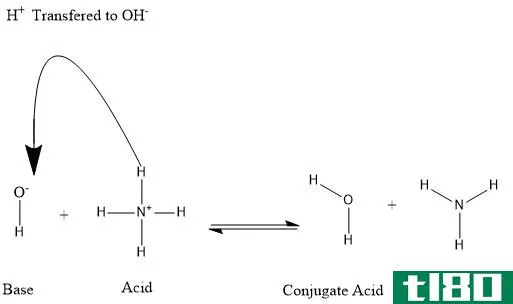
不同的科学家对“基”的定义不同。把它定义为一种物质。Br***ted-Lowry将碱定义为可以接受质子的物质。根据刘易斯的说法,任何电子供体都是碱。根据Arrhenius的定义,一个化合物应该有一个氢氧化阴离子,并且有能力以氢氧化离子的形式将其作为碱。然而,根据Lewis和Br***ted-Lowry的说法,有些分子不含氢氧化物,但可以作为碱。例如,NH3是一个路易斯碱,因为它可以在氮上提供电子对。同样,Na2CO3是一种不含氢氧化物基的Br***ted-Lowry碱,但可以接受氢。
属性
底座有一种滑滑的肥皂般的感觉和苦涩的味道。它们很容易与产生水和盐分子的酸发生反应。烧碱、氨水和小苏打是常见的碱。我们可以将这些化合物分为两类,这取决于它们离解和生成氢氧化物离子的能力。他们是强者和弱者。强碱如氢氧化钠、氢氧化钾,在溶液中能完全电离,产生离子。像NH3这样的弱碱部分离解,生成的氢氧化物离子较少。

图02:氢氧化钡-第2组元素钡的基底
此外,Kb是碱基离解常数。它表示弱碱的氢氧化物离子流失的能力。为了检查一种物质是否为碱,我们可以使用石蕊试纸或pH试纸等几种指示剂。这些化合物的pH值高于7,红色石蕊变成蓝色。
碱(alkali)和基础(base)的区别
第1类金属被称为碱,或者更准确地说,它们的碳酸盐和氢氧化物被称为碱。然而,它们有基本性质;因此,它们是基的子集。碱与碱的主要区别在于,第1组元素被归为碱元素,而任何具有基本性质的元素或化合物都被归为碱。因此,所有碱都是碱,但并非所有碱都是碱。碱和碱的另一个显著区别是碱形成离子盐,而碱不一定是离子盐。
以下关于碱和碱之间差异的信息图以表格形式显示了这些差异。
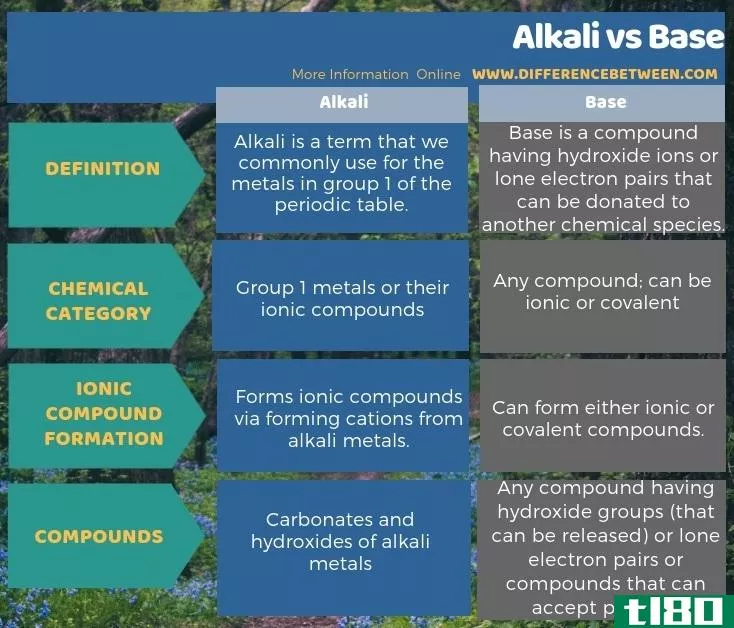
总结 - 碱(alkali) vs. 基础(base)
我们经常交替使用碱和碱这两个术语,但它们是两个不同的术语。碱与碱的主要区别在于,第1组元素被归为碱元素,而任何具有基本性质的元素或化合物都被归为碱。
引用
1大英百科全书的编辑。“碱”,大英百科全书,大英百科全书,2014年1月14日。这里有2个。维基百科(维基百科,2018年11月27日,维基百科)
2“基础(化学)。”维基百科,维基媒体基金会,2018年11月27日