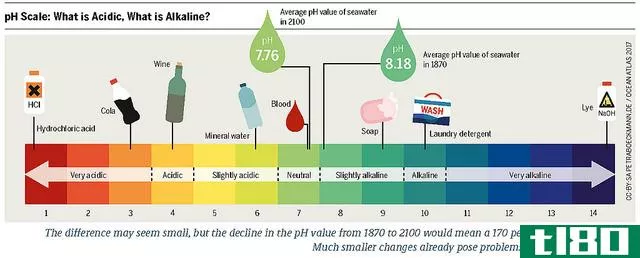
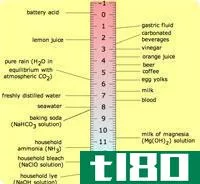
酸和碱的关键区别在于酸的pH值在1到7之间,而碱的pH值在7到14之间。
pH值是H+离子浓度的负对数。pH值7被视为中性pH值。pH值高于7表示存在碱,低于7表示存在酸。根据Brønsted-Lowry理论,酸可以释放H+离子,而碱可以接受H+离子。

目录
1. 概述和主要区别
2. 什么是酸
3. 什么是基地
4. 并列比较-以表格形式列出酸与碱
5. 摘要
什么是酸(an acid)?
酸是水溶液中pH值小于7的物质。酸性介质的存在可以用石蕊试纸来确定。酸能使蓝色石蕊变红。然而,如果使用红色石蕊,颜色不会发生变化。含有易电离氢原子的化合物通常是酸。
根据Brønsted-Lowry理论,酸是一种在含水介质中能释放质子(H+离子)的物质。当H+离子被释放时,这些离子不能单独存在于水介质中。因此,这些离子与水分子结合,形成H3O+离子(氢离子)。因此,氢离子的存在表明酸的存在。
根据Arrhenius理论,酸是一种能增加水介质中氢离子数量的物质。这是由于氢离子的增加。换句话说,酸释放出H+离子,H+离子可以与水分子相互作用,形成氢离子。
当考虑刘易斯理论时,酸是一种能够从共价化学键中接受一对电子的化合物。根据这个定义,没有氢原子的物质也被归类为酸,因为它们能接受电子对。
酸的性质
酸通常有酸味。酸的pH值总是小于7。几乎所有的酸都有燃烧的气味。酸的质地粘而不滑。此外,酸可以与金属(甚至是高度不活泼的金属)反应,形成金属氢化物和氢气。
什么是基地(a base)?
碱是一种在水溶液中pH值高于7的物质。溶液的碱性使红石蕊的颜色变成蓝色。因此,碱的存在可以用红石蕊来确定。然而,当使用蓝色石蕊时,没有颜色变化与基地。具有易电离羟基的化合物通常是碱。
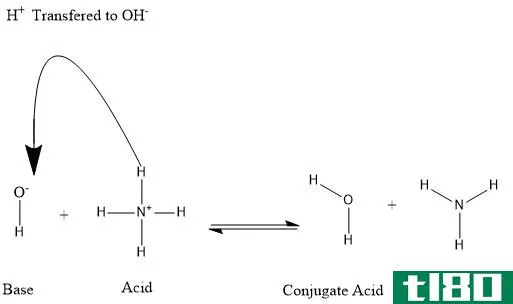
根据Brønsted-Lowry理论,碱是质子受体;换句话说,碱可以接受水介质中的质子。然而,Arrhenius理论也给出了一个类似的定义:碱是一种减少介质中氢离子数量的物质。由于碱从水介质中获得氢离子或质子,氢离子浓度降低。这些离子是形成氢离子所必需的。
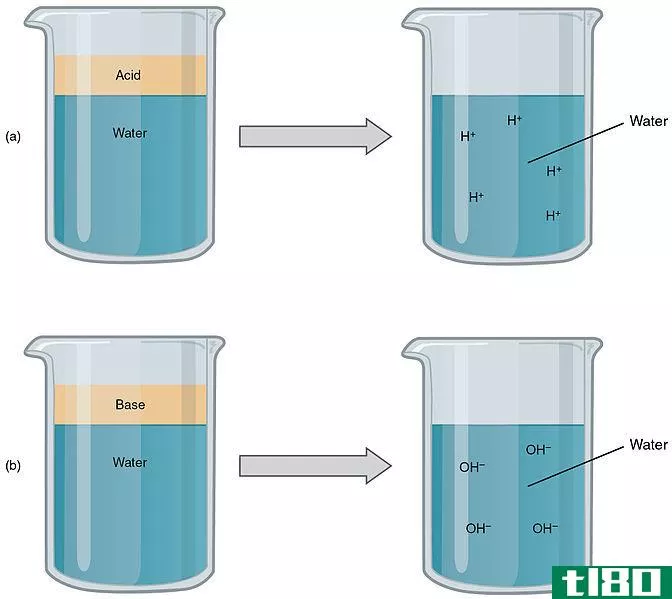
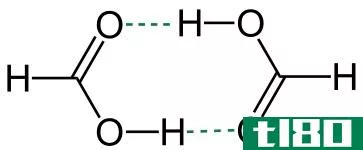
图1:酸和碱的比较
考虑到刘易斯理论,碱是一种可以提供电子对的物质。这些物质提供电子对并形成配位共价键。根据这个理论,大多数没有羟基的化合物都会变成碱。
基的性质
碱有苦味。这些物质的pH值总是高于7。除了氨,几乎所有的碱都是无味的。氨有刺鼻的气味。不像酸,碱摸起来很滑。碱与酸反应时被中和。
酸的(acid)和基础(base)的区别
| 酸与碱 | |
| 酸是指当酸在水溶液中时pH值低于7的物质 | 碱是指当碱在水溶液中时,pH值高于7的物质 |
| 基于Brønsted Lowery理论的定义 | |
| 酸是一种物质,当它在水介质中时,它可以向介质释放质子(H+离子)。 | 碱是质子受体;换句话说,一个碱基可以接受来自水介质的质子。 |
| 基于Arrhenius理论的定义 | |
| 酸是一种能增加水介质中氢化物离子含量的物质。 | 碱是一种能减少水介质中的氢化物离子量的物质。 |
| 基于刘易斯理论的定义 | |
| 酸是一种化合物,它能够接受共价化学键中的一对电子。 | 碱基是一种能捐献电子对的物质。 |
| 石蕊颜色变化 | |
| 酸可以使蓝色石蕊变红,但红石蕊的颜色没有变化。 | 碱可以变成红色的石蕊蓝,但蓝色石蕊没有颜色变化。 |
| 品味 | |
| 艾滋病有酸味。 | 碱基有苦味。 |
| 气味 | |
| 酸有燃烧的气味。 | 碱除了氨以外,没有气味。 |
| 电离 | |
| 酸电离后会形成氢化物离子。 | 碱在电离时会形成羟基离子。 |
| 共轭化学种 | |
| 酸的共轭种是它的共轭基。 | 碱基的共轭种是共轭酸。 |
| 中和 | |
| 酸可以用碱中和。 | 碱可以用酸中和。 |
| 滴定法 | |
| 酸用碱滴定中和。 | 碱与酸反应进行中和。 |
总结 - 酸的(acid) vs. 基础(base)
所有化合物可分为酸、碱和中性化合物。酸和碱的关键区别在于酸的pH值在1到7之间,而碱的pH值在7到14之间。
引用
1赫尔曼斯汀,安妮·玛丽。“这就是酸在化学中的作用。”ThoughtCo,这里有。赫尔曼斯汀,安妮·玛丽。“关键酸和碱的定义。”ThoughtCo,可在这里找到。歌词。“酸碱概述”,化学剧本,歌词,2017年2月13日,可在这里查阅。
2赫尔曼斯汀,安妮·玛丽。“关键酸碱定义”ThoughtCo,
三。歌词。“酸碱概述”,化学剧本,歌词,2017年2月13日,