主要区别
碱和碱的主要区别在于碱是一种能溶于水的碱,而碱是一种能中和酸的物质。
碱(alkali) vs. 基础(base)
碱性化合物释放氢氧化物离子并接受质子;另一方面,碱是用来中和酸形成盐和水的物质。所有碱化合物都是碱的类型。然而,并不是所有的碱都是碱。元素周期表中的第一族元素,碳酸盐和氢氧化物被归类为碱元素;另一方面,这种具有基本性质的化合物被归类为碱和单质碱。碱是离子盐;另一方面,碱不一定是离子盐。碱没有合适的离子盐,而碱化合物是合适的离子盐。
碱化合物通常是碱金属的碳酸盐化合物和氢氧化物化合物;相反,碱可以是任何具有氢氧化物离子和能共享的孤电子对的化合物。碱性化合物总是来自周期表中的碱金属,而碱可以是任何显示出基本性质的化合物。
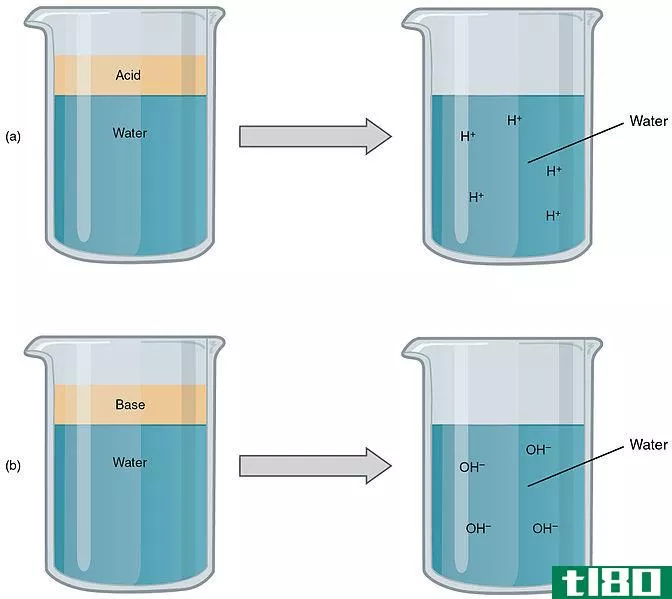
碱性化合物与水反应时不产生OH离子;另一方面,碱性化合物与水反应时产生OH离子。碱在水中溶解时中和酸;另一方面,碱没有中和酸的能力,不能溶解在水中。术语碱是指在溶液中接受氢离子的离子化合物或含有碱金属的盐;另一方面,术语碱是指产生低浓度氢离子溶液而不是纯水的化合物。
对比图
什么是碱(alkali)?
对于门捷列夫周期表第一族元素,我们通常使用碱这个术语。第一组元素称为碱金属。该族包含氢(H)、锂(Li)、钠(Na)、钾(K)、铷(Rb)、铯(Cs)和弗朗(Fr),它们都是第1族的成员,被称为碱金属。氢元素的行为与该族所有其他成员略有不同。碱性化合物性质柔软,外观光亮,颜色呈银色;这些都是碱的一些特殊性质。
碱在它的最外层有一个电子,它们很乐意把这个电子移走或捐给别人,使自己变成阳离子1+。这就是为什么当碱金属开始与最外层的电子反应时,它们会被激发,进入基态,并开始发射可见光范围的辐射。碱金属在自然界是非常活跃的,因为这种激发发射电子。然而,周期表第1族碱金属的反应性自上而下都在增加。
碱形成具有负电荷原子的离子化合物,表现出苦味、滑触和中和酸的能力等基本特性。碱也有不同的性质,比如它们能把红色的石蕊变成蓝色。它们是典型的燃烧和腐蚀性化合物。碱也被称为可溶盐,是从这种植物的灰烬中提取的,这种植物含有高浓度的碳酸钾和碳酸钠。苛性钠和苛性钾是碱的最好例子。
什么是基础(base)?
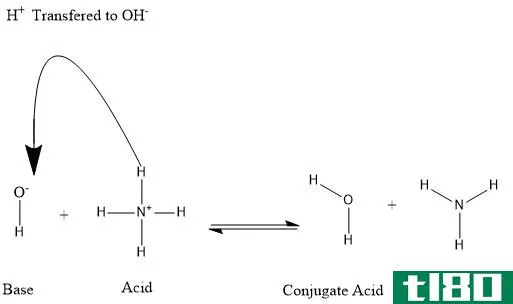
许多科学家对碱基的定义不同。阿伦尼乌斯将碱定义为一种能将氢氧化物离子(OH)提供给相应溶液的物质。Lowry Br***ted将碱定义为可以接受质子的化合物。刘易斯还将碱定义为电子供体。根据阿伦尼乌斯碱的概念,应该有氢氧化物离子捐赠。Lowry Br***ted和Lewis说,这些化合物也可以作为一种不含氢离子的碱。
碳酸钠(Na2CO3)也被称为Lowry-Br***ted碱,因为它不含任何氢氧化物离子,但它有接受质子的能力。碱的性质包括:质地光滑,有肥皂般的感觉;味苦;易与助剂反应,产生盐和水分子,能改变指示剂的颜色。小苏打、碱液、碳酸氢钠是一些最好的碱。
碱根据其解离和产生OH离子的能力可分为弱碱和强碱两大类。氢氧化钠,氢氧化钾,被称为强碱,能在各自的溶液中完全电离。氨是一种弱碱,在各自的溶液中可以部分解离,只产生少量的OH离子。此外,Kb是碱浓度的常数,用作检查丢失的OH离子对碱进行分类的能力的参数。
关键区别
- 碱形成离子化合物,而碱形成离子和共价化合物。
- 碱含有第1族金属氧化物和氢氧化物;另一方面,碱含有氧化物离子和氢氧化物离子。
- “碱”一词仅用于碱性金属;相反,“碱”一词可用于任何具有基本性质的化合物。
- 碱性化合物可溶于水;另一方面,碱不溶于水。
- 所有的碱化合物都可以说是碱,而碱不能说是碱。
- 碱释放OH离子,尽管碱中和了酸。
- 与碱相比,碱具有更高的接受质子的能力。
- 碱不具有释放OH离子的性质,而碱具有释放OH离子的性质。
- 碱释放氢离子并产生氢离子。然而,碱具有降低氢离子浓度的能力。
- 碱从不以纯盐的形式存在;另一方面,碱以纯盐的形式存在。
结论
结果表明,碱产生OH离子,碱是一种提供非键电子的化合物。