原子性(atomicity)和配价(valency)的区别
原子性的主要区别(main difference atomicity) vs. 配价(valency)
原子性和价性是两个常用于原子和分子的化学术语。原子性是分子中存在的原子数。价态是原子为了稳定而必须失去、获得或共享的最大电子数。因此,这是原子和分子的两个截然不同的性质。原子性和价性的主要区别在于原子性解释了分子的性质,而价性描述了元素的性质。
覆盖的关键领域
1.什么是原子性-定义,用例子说明类型2.什么是配价-定义,用例子说明3.原子性和配价之间的区别是什么-关键区别的比较
关键词:原子性,双原子,电子构型,惰性气体,单原子,多原子,硫,价态

什么是原子性(atomicity)?
原子性是分子中存在的原子总数。根据这个定义,分子可以根据分子的原子性被分为若干组。例如,分子可以是单原子的、双原子的、三原子的或多原子的。单原子化合物由一个原子组成。例如,惰性气体,如氦(He)、氩(Ar)等是单原子化合物。双原子化合物由每一分子的两个原子组成。Ex:氧气(O2)、氮气(N2)、氯气(Cl2)等。
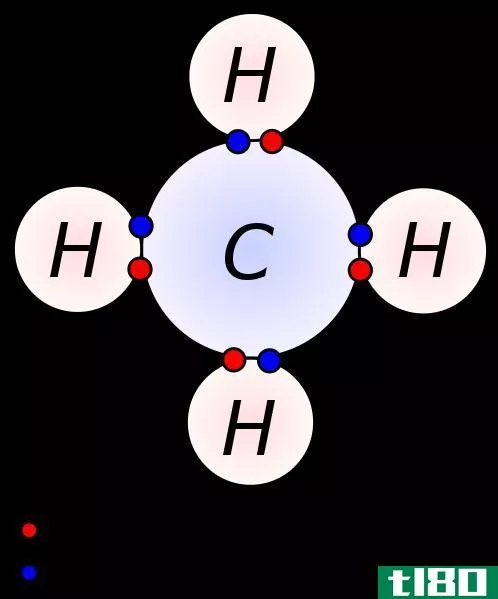
原子性的符号是“a”。因此,对于单原子化合物,a=1,对于双原子化合物,a=2。对于多原子化合物,原子度是一个很大的值。这是因为多原子分子是由大量的原子组成的。

Figure 1: A Polyatomic Molecule
当考虑同一组元素(在周期表中)形成的化合物的原子性时,我们可以观察到这些化合物的化学和物理性质的关系。例如,所有惰性气体都是具有相似化学性质的单原子化合物。尽管有些化合物在化学和物理性质上有很大的不同,但根据这些化合物的原子性,它们可能属于同一类化合物。例如,Cl2是气态化合物,而I2在室温下是固体。但考虑到它们的原子度值,这两种化合物都是双原子化合物。
什么是配价(valency)?
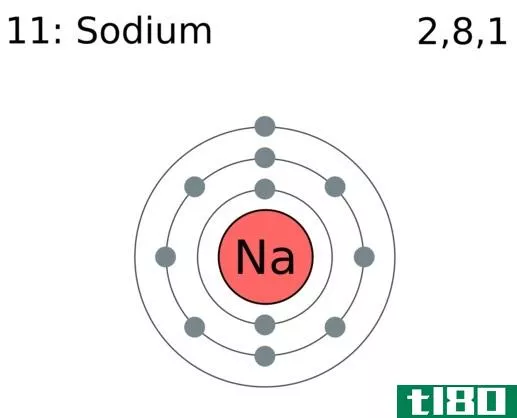
价态可以定义为一个原子为了稳定而失去、获得或共享的最大电子数。对于金属和非金属,八进制规则描述了原子的最稳定形式。它说,如果一个原子的最外层壳层的数目完全被八个电子填满,那么这个构型是稳定的。换句话说,如果s和p子轨道完全填满,有ns2np6,它是稳定的。当然,惰性气体原子具有这种电子构型。因此,其他元素需要失去、获得或共享电子,才能遵守八位元规则。参与这个稳定过程的最大电子数叫做原子价。
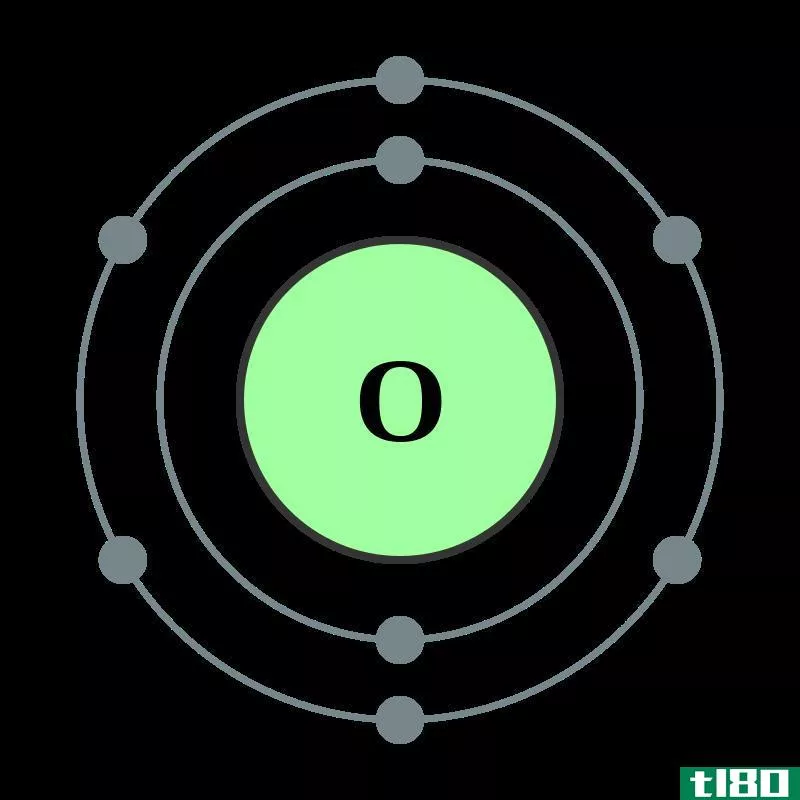
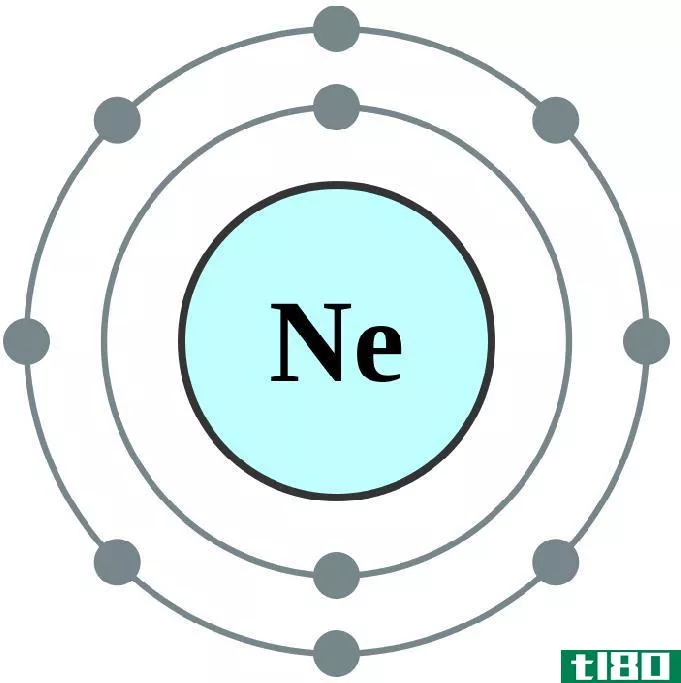
让我们以硫磺为例。硫的价可以确定如下。

Figure 2: Chemical Structure of Sulfur Atom
硫最外层轨道上的电子数为6,为了稳定,最外层轨道上的电子数应为8(根据八位元定律)。然后,硫必须从外部获得或共享2个电子。因此,硫的价为2。
然而,过渡元素可能具有不同的价。这是因为过渡金属可以通过去除不同数量的电子而稳定。
原子性(atomicity)和配价(valency)的区别
定义
原子性:原子性是分子中原子的总数。
价态:价态是一个原子为了稳定而失去、获得或分享的最大电子数。
决心
原子性:原子性可以通过计算物质中每个分子的原子数来确定。
价态:价态可以通过观察原子的电子构型来确定。
原子数
原子性:原子性取决于分子中原子的数量。
原子价:原子价与原子数无关。
与电子的关系
原子性:原子性与原子中的电子数无关。
价:价与电子数有直接关系。
不同类型
原子性:化合物根据原子性可分为单原子、双原子、三原子和多原子化合物。
化合价:根据元素的化合价,元素可分为单价元素、二价元素等。
结论
原子性是分子中存在的原子数。价态是原子为了稳定而必须失去、获得或共享的最大电子数。原子性和价性的主要区别在于原子性解释了分子的性质,而价性描述了元素的性质。
引用
1.“CHEM-GUIDE.”基本气体原子性的推导,CHEM-GUIDE.blogspot.com/2010/03/可在此处获得。2.化学一:原子与分子。这里有。 2.化学一:原子与分子。这里有。
- 发表于 2021-06-29 17:20
- 阅读 ( 206 )
- 分类:科学
你可能感兴趣的文章
价壳(valence shell)和倒数第二壳(penultimate shell)的区别
价壳层与倒数第二层壳层的主要区别在于,价壳层是原子最外层的含电子壳层,而倒数第二层壳层是最外层含电子壳层的内层壳层。 价壳层和倒数第二层壳层这两个术语主要在普通化学中用来确定一个特定原子的电子组成。...
- 发布于 2020-09-26 17:01
- 阅读 ( 869 )
初级的(primary)和二价(secondary valency)的区别
...主价与次价的关键区别在于,主价是配位络合物中心金属原子的氧化态,而次价是配位络合物中心金属原子的配位数。 一级价和二级价属于配位化学范畴。价是一种元素的结合力,特别是用它能置换或结合的氢原子数来衡量的...
- 发布于 2020-10-13 23:58
- 阅读 ( 282 )
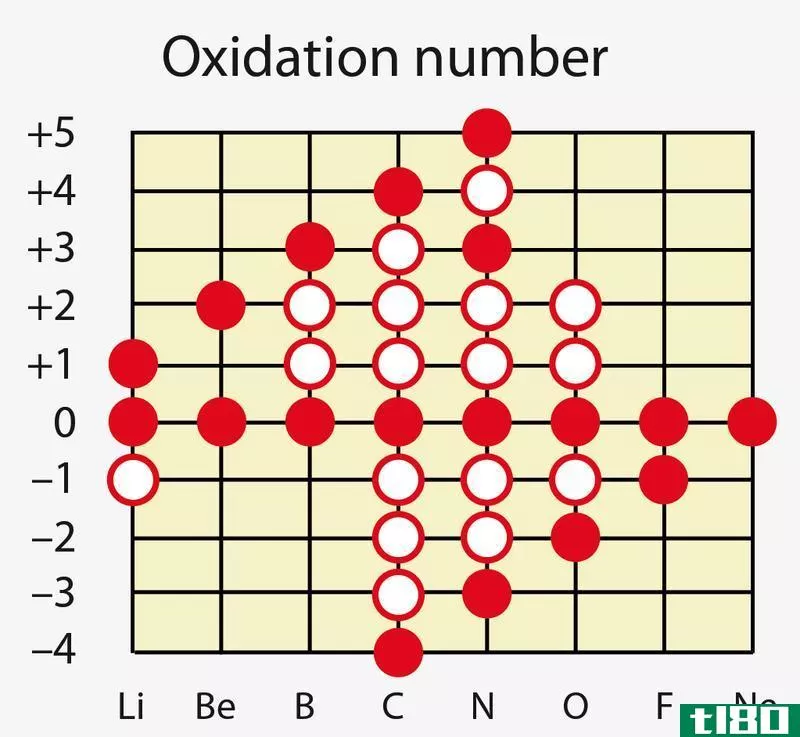
价(valency)和氧化值(oxidation number)的区别
价态和氧化数之间的关键区别在于,价态是一个原子为稳定所能失去、获得或共享的最大电子数,而氧化数是一个原子为了与另一个原子形成键而可以失去或获得的电子数。 氧化数和价电子与原子的价电子有关。价电子是占...
- 发布于 2020-10-15 12:44
- 阅读 ( 302 )
价带(valence band)和导带(conduction band)的区别
...导带的表格形式 5. 摘要 什么是价带(valence band)? 价带是原子被激发时电子能从中跃出的电子带。在这里,电子跃迁到导带。因此,基本上,它是任何有电子的物质原子的最外层电子轨道。此外,这一术语与“价电子”一词密切...
- 发布于 2020-10-17 00:55
- 阅读 ( 1567 )
激进的(radical)和价(valency)的区别
...。价是一种元素的结合力,特别是用它能置换或结合的氢原子数来衡量的。 目录 1. 概述和主要区别 2. 什么是激进的 3. 什么是价 4. 并列比较-自由基与价的表格形式 5. 摘要 什么是激进的(radical)? 自由基是一种具有不成对电子的...
- 发布于 2020-10-17 02:38
- 阅读 ( 404 )
原子氧(atomic oxygen)和分子氧(molecular oxygen)的区别
原子氧和分子氧的关键区别在于,原子氧具有很高的活性,不存在于大气中,而分子氧的活性较小,以其存在于大气中。此外,原子氧是具有符号O(**)的自由基,而分子氧是具有符号O2的双原子氧。 氧是原子序数为8的化学...
- 发布于 2020-10-18 03:34
- 阅读 ( 498 )
原子价(valence)和核心电子(core electrons)的区别
...参与化学键的形成,而核心电子不参与化学键的形成。 原子是所有现存物质的组成部分。它们太小了,我们甚至不能用肉眼观察它们。一般来说,原子在埃范围内。原子是由原子核组成的,原子核有质子和中子。有电子绕着原...
- 发布于 2020-10-22 12:42
- 阅读 ( 1129 )
价(valency)和指控(charge)的区别
...。价是一种元素的结合力,特别是用它能置换或结合的氢原子数来衡量的。另一方面,原子的电荷是质子数减去原子中的电子数。 目录 1. 概述和主要区别 2. 什么是价 3. 什么是电荷 4. 并列比较-以表格形式表示的价与电荷 5. 摘...
- 发布于 2020-10-23 02:08
- 阅读 ( 350 )
价(valency)和价电子(valence electrons)的区别
...配置。正是最外层的电子通常有助于形成化学键。在某些原子中,价电子的数目等于价电子的数目。 什么是价电子(valence electr***)? The number of electr*** in the outermost shell of an atom is called “valence electr***”. Because of this reason, the outer...
- 发布于 2020-10-24 18:09
- 阅读 ( 991 )
分子轨道理论(molecular orbital theory)和价键理论(valence bond theory)的区别
...轨道理论描述的是分子轨道的形成,而价键理论描述的是原子轨道的形成。 不同的分子具有不同的化学和物理性质,不同的原子连接起来形成这些分子。为了了解原子和分子性质之间的这些差异,有必要了解几个原子之间形成...
- 发布于 2020-11-03 20:05
- 阅读 ( 460 )