电子亲和力(electron affinity)和电离能(ionization energy)的区别
主差电子亲和性(main difference electron affinity) vs. 电离能(ionization energy)
电子是原子的亚原子粒子。有许多化学概念可以解释电子的行为。电子亲和能和电离能是化学中两个这样的概念。电子亲和力是中性原子或分子获得电子时释放的能量。电子亲和力也可以被称为电子增益焓的意义时,考虑到,但他们是不同的术语,因为电子增益焓描述的能量吸收周围的原子时,获得一个电子。另一方面,电离能是从原子中除去电子所需的能量。电子亲和能和电离能之间的主要区别在于,电子亲和能给出原子获得电子时释放的能量,而电离能是从原子中除去电子所需的能量。
覆盖的关键领域
1.什么是电子亲和力-定义,吸热和放热反应2.什么是电离能-定义,第一电离,第二电离3.电子亲和力和电离能之间有什么相似之处-共同特征概述4.电子亲和力和电离能之间有什么区别-主要区别比较
关键词:原子,电子,电子亲和性,电子增益焓,第一电离能,电离能,第二电离能

什么是电子亲和力(electron affinity)?
电子亲和力是中性原子或分子(在气相中)从外部获得电子时释放的能量。这个电子的加成导致一种带负电荷的化学物质的形成。这可以用如下符号表示。
X+e–→ X–+能量
把电子加到中性原子或分子上释放能量。这叫做放热反应。这个反应产生负离子。但是如果另一个电子要加入到这个负离子中,为了继续这个反应,应该给它能量。这是因为入射电子被其他电子排斥。这种现象称为吸热反应。
因此,同一物种的第一电子亲和性为负值,第二电子亲和性为正值。
第一电子亲和性:X(g)+e–→ X(克)-
第二电子亲和性:X(g)–+e–→ X(g)-2个
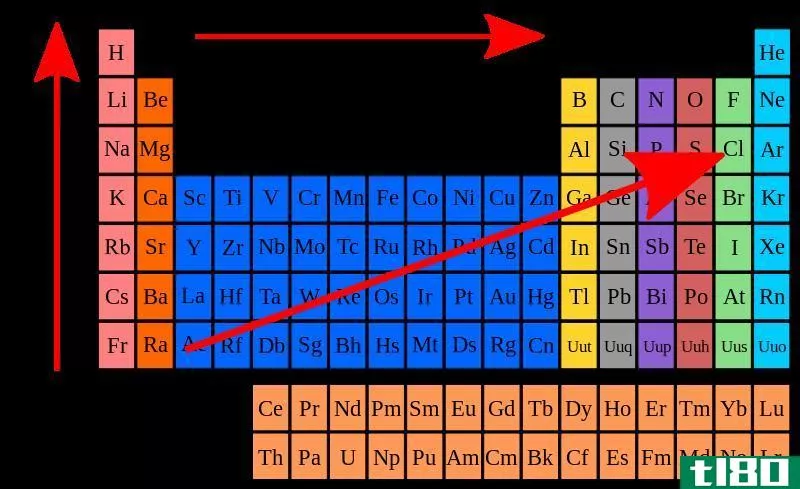
电子亲和力在周期表中显示出周期性的变化。这是因为入射电子被加到原子的最外层轨道上。元素周期表的元素是按照原子序数的升序排列的。当原子序数增加时,它们最外层轨道上的电子数增加。

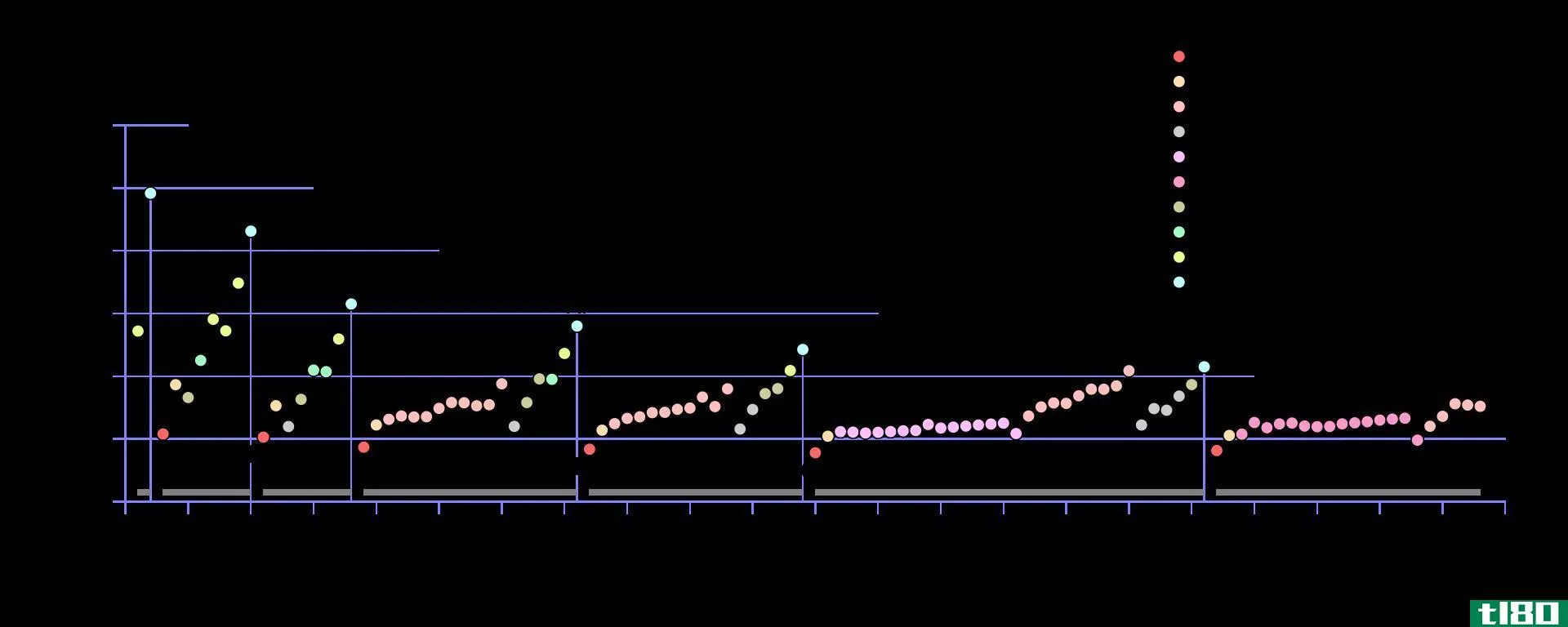
Figure 1: Variation of Electron Affinity along a Period of Periodic Table
一般来说,电子亲和力应该沿着从左到右的周期增加,因为电子的数量沿着一个周期增加;因此,很难添加新的电子。当实验分析时,电子亲和势值显示出之字形图案而不是显示出逐渐增加的图案。
什么是电离能(ionization energy)?
电离能是一个气态原子从其最外层轨道上除去一个电子所需要的能量。这被称为电离能,因为原子在除去一个电子后得到一个正电荷,变成一个带正电荷的离子。每个化学元素都有一个特定的电离能值,因为一个元素的原子不同于另一个元素的原子。例如,第一电离能和第二电离能分别描述原子去除一个电子和另一个电子所需的能量。
第一电离能
第一电离能是气态中性原子除去最外层电子所需的能量。这个最外层的电子位于原子的最外层轨道上。因此,这个电子在该原子的其他电子中能量最高。因此,第一电离能是从原子中放出最高能量电子所需的能量。这个反应本质上是吸热反应。
这一概念与带中性电荷的原子有关,因为带中性电荷的原子只由元素应包含的原始数量的电子组成。然而,这一目的所需的能量取决于元件的类型。如果一个原子中所有的电子都是成对的,它就需要更高的能量。如果有一个未配对的电子,它需要一个较低的能量。然而,价值还取决于其他一些事实。例如,如果原子半径很大,则需要较低的能量,因为最外层的电子离原子核较远。那么这个电子和原子核之间的吸引力就很低了。因此,它很容易被移除。但是如果原子半径很小,那么电子就会被原子核吸引,很难从原子中除去电子。

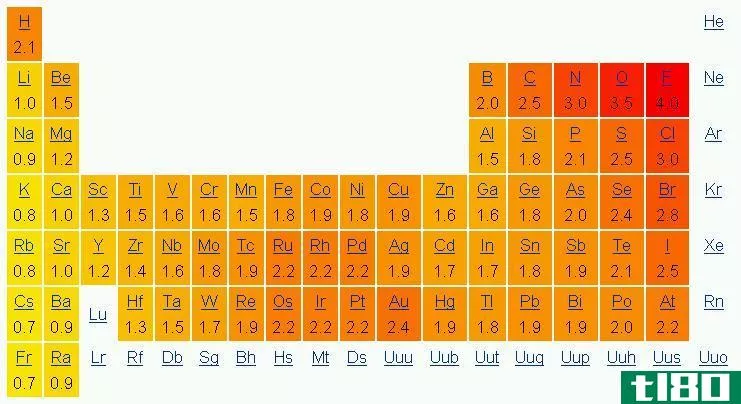
Figure 2: Pattern of Varying First Ionizing Energies of Some Chemical Elements
二次电离能
第二电离能可以定义为从带正电的气态原子中除去最外层电子所需的能量。从带中性电荷的原子中去掉一个电子会产生一个正电荷。这是因为没有足够的电子来中和原子核的正电荷。从这个带正电的原子中取出另一个电子需要很高的能量。这个能量叫做第二电离能。
第二电离能总是比第一电离能高,因为从带正电荷的原子中除去电子比从带中性电荷的原子中除去电子非常困难;这是因为从中性原子中去掉一个电子后,其余的电子被原子核高度吸引。
电子亲和能与电离能的相似性
- 两者都是与能源有关的术语。
- 电子亲和能和电离能的值取决于被测原子的电子构型。
- 两者在周期表中都显示出一种模式。
电子亲和力(electron affinity)和电离能(ionization energy)的区别
定义
电子亲和性:电子亲和性是中性原子或分子(气相中)从外部获得电子时释放的能量。
电离能:电离能是一个气态原子从其最外层轨道上除去一个电子所需要的能量。
能量
电子亲和性:电子亲和性描述能量释放到周围环境。
电离能:电离能描述从外部吸收能量。
电子能
电子亲和性:电子亲和性用来描述电子的获得。
电离能:电离能用来描述电子的去除。
结论
电子亲和能和电离能是用来定量描述电子和原子行为的两个化学术语。电子亲和能和电离能之间的主要区别在于,电子亲和能给出原子获得电子时释放的能量,而电离能是从原子中除去电子所需的能量。
引用
1.“电子亲和性”,《化学文集》,文集,2017年11月14日,可在此处查阅。2。电子亲和性,化学指南,可在这里获得。赫尔曼斯汀,安妮·玛丽。”电离能的定义和趋势〉,ThoughtCo,2017年2月10日,可在此查阅。 2.电子亲和性,化学指南, 3.赫尔曼斯汀,安妮·玛丽。”电离能定义与趋势〉,《思想》,2017年2月10日,
- 发表于 2021-06-30 00:27
- 阅读 ( 661 )
- 分类:科学
你可能感兴趣的文章
电离(ionization)和电解(electrolysis)的区别
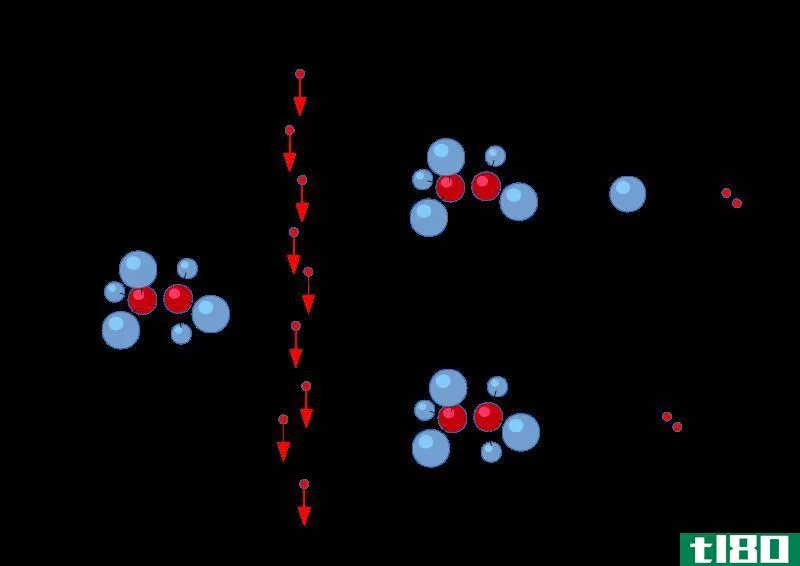
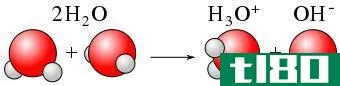
...了+1电荷(它是质子的电荷)。所需的能量是原子的第一电离能。 此外,在液体溶液中发生的电离是溶液中离子的形成。例如,当HCl分子溶解在水中时,会形成氢离子(H3O+)。在这里,HCl与水分子反应,形成带正电荷的氢离子...
- 发布于 2020-10-15 10:13
- 阅读 ( 558 )
积极的(positive)和质谱中的负电离(negative ionization in mass spectrometry)的区别
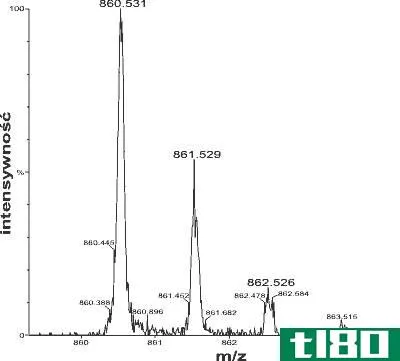
质谱中正、负电离的关键区别在于正电离形成带正电荷的离子,而负电离形成带负电荷的离子。 质谱法是分析化学中测量离子质量电荷比的一种技术。这项技术的最终结果是形成一个以强度图形式出现的质谱图。此外,该图...
- 发布于 2020-10-15 13:49
- 阅读 ( 719 )
酸电离常数(acid ionization constant)和碱基电离常数(base ionization constant)的区别
关键区别-酸电离常数与碱电离常数 酸离子化常数(Ka,也称为酸离解常数)定量测量了酸分子与其电离形式之间的平衡。同样,碱离解常数(Kb,或碱离解常数)可定量测量碱分子与其电离形式之间的平衡。酸电离常数和碱...
- 发布于 2020-10-19 03:06
- 阅读 ( 426 )
溶剂化能(solvation energy)和晶格能(lattice energy)的区别
...下方程给出。 生成热=原子化热+离解能+电离能之和+电子亲和力之和+晶格能 然后通过重新排列这个方程,可以得到化合物的晶格能,如下所示。 晶格能=生成热–{原子化热+离解能+电离能之和+电子亲和力之和} 溶剂化能(solvation e...
- 发布于 2020-10-20 03:46
- 阅读 ( 776 )
电离(ionization)和离解(dissociation)的区别
...子组成。因此,离子化和离解的关键区别在于电离是通过电子的获得或损失而产生新的离子,而离解是化合物中已经存在的离子的分裂或分离。 内容1。概述和主要区别2。什么是电离3。什么是分离4。并排比较——电离与解离5。...
- 发布于 2020-10-25 04:34
- 阅读 ( 300 )
激发(excitation)和电离势(ionization potential)的区别
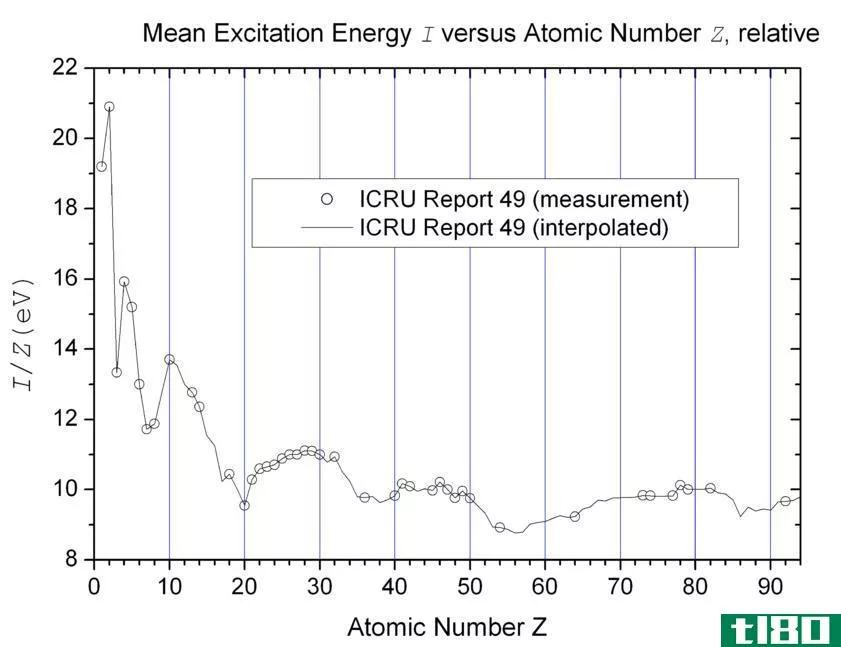
...子或分子移到无限远的地方。这个过程所需的能量称为“电离能”或“电离势”。 换言之,这是电子束缚在原子核上的初始状态和电子不再附着在原子核上的最终状态之间的势能差。 电离能(IE)与质子数的周期趋势 激发(excita...
- 发布于 2020-10-28 16:52
- 阅读 ( 427 )
第一(first)和二次电离能(i1e vs i2e)(second ionization energy (i1e vs i2e))的区别
第一(first)和二次电离能(i1e(second ionization energy (i1e)的区别 在分析第一电离能和第二电离能的区别之前,让我们先讨论电离能是什么。一般来说,电离能是指从气态原子或离子中除去电子所需的能量。由于电子被吸引到正原...
- 发布于 2020-10-28 20:50
- 阅读 ( 547 )
电离能(ionization energy)和结合能(binding energy)的区别
电离能和结合能的关键区别在于,电离能是除去孤立的中性气体原子或分子中最松散束缚的电子所需的最小能量,而结合能是从粒子系统中移除粒子所需的最小能量。 化学体系的电离能和结合能是两个不同的术语,描述了两...
- 发布于 2020-11-02 08:19
- 阅读 ( 1192 )
电负性(electronegativity)和电离能(ionization energy)的区别
电负性和电离能的关键区别在于,电负性解释了电子的吸引力,而电离能是指从原子中移除电子。 原子是所有现存物质的组成部分。它们太小了,我们甚至不能用肉眼观察它们。原子由原子核组成,原子核有质子和中子。除...
- 发布于 2020-11-04 14:49
- 阅读 ( 935 )
电子亲和力(electron affinity)和电子增益焓(electron gain enthalpy)的区别
电子亲和力和电子增益焓的关键区别在于,电子亲和力是指孤立原子获得电子的趋势,而电子增益焓是指孤立中性原子获得一个额外电子时释放的能量。 电子亲和力和电子增益焓是两个相关的术语,因为电子增益焓是关于电...
- 发布于 2021-03-04 15:37
- 阅读 ( 645 )