关键区别–八位体与二位体
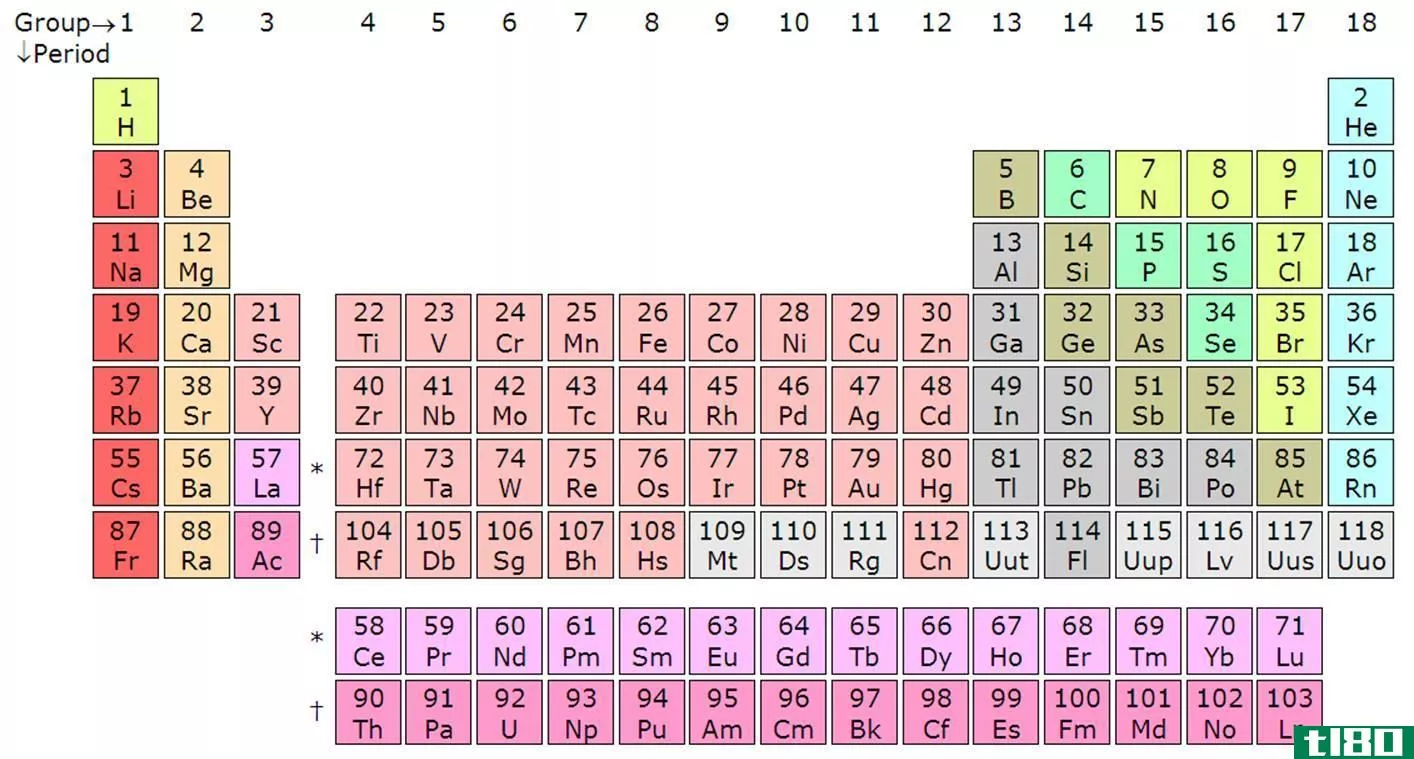
自然界中存在化学活性和非活性原子或化合物。这个特性主要取决于原子最外层的电子数。具有不完整壳层的原子可能会变得活跃,以完成它们的电子构型,从而变得稳定。不活泼的原子有一个完整的电子构型;因此,这些原子不与任何其他原子发生反应,除非在特殊条件下。惰性气体在自然界中总是不活泼的。因此,它们被称为惰性气体。惰性气体在元素周期表的第八列。在同一周期(row)中的其他元素往往在该周期结束时获得惰性气体的电子组态,这是自然界中最稳定的形式。活性原子倾向于根据八位规则或二位规则完成电子数。八重态和双原子态的关键区别在于,八重态是一个原子或一个离子,它在最外层的壳层中最多有八个电子,而双原子则是在最外层最多有两个电子的原子。
内容1。概述和主要区别2。什么是八位元3。什么是双重4。并排比较-八位字节与双字节5。摘要
什么是八重奏(an octet)?
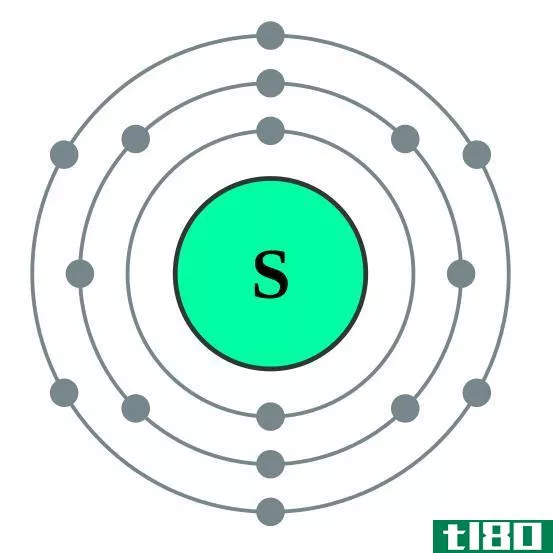
八重态是一个原子或一个离子,它的最外层有八个电子。除了氦以外,所有的惰性气体都有八个电子,在性质上是惰性的。惰性气体的电子组态总是以如下方式结束。
ns2 np6
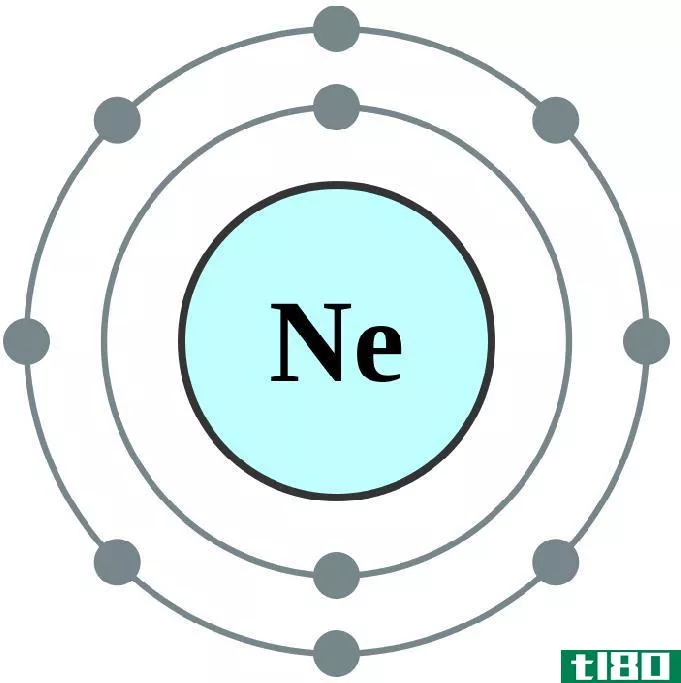
例如,氖的电子组态是1s22s22p6。氖是一种惰性气体。
在最外层轨道上有七个、六个等电子的其他元素,通过从外部获得电子,倾向于遵守八位元规则;其他一些元素有一个、两个等。电子往往丢失电子,并获得最近的惰性气体的电子组态。但元素周期表中间的其他元素会与有多余电子的元素形成新的键,从而共享这些电子并成为八位元。

图01:霓虹灯,八位体
什么是小鸡(a duplet)?
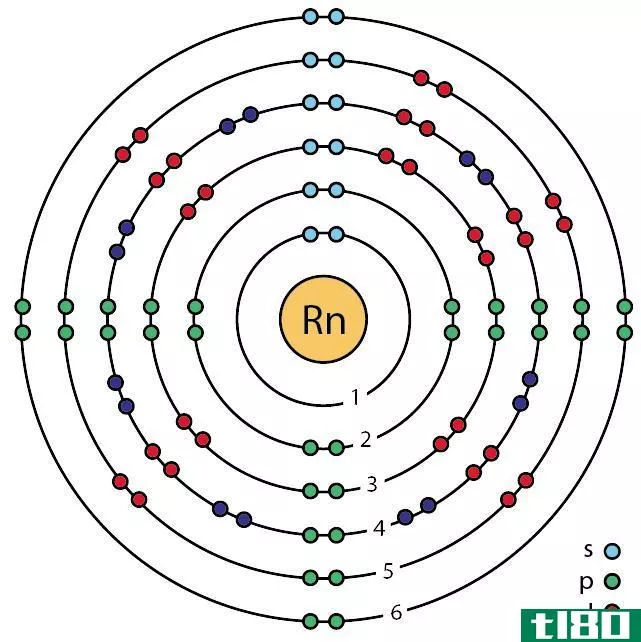
氢原子和氦原子是自然界中最小的元素,它们的原子核只有一个轨道。这个轨道叫做1s轨道。这个轨道最多可以包含两个电子。氢原子有一个电子,氦有两个电子。因此,氦被称为双星。氦有它能拥有的最大数量的电子,因此它在自然界中是一种稳定的元素。因此,氦也是一种惰性气体。但是氢只有一个电子,它唯一的轨道是不完整的。因此,氢原子本身是非常活泼的,它倾向于与另一个氢原子形成共价键,共享它们仅有的电子。然后这些氢原子变成了双星,因为它们的最外层轨道上有两个电子。但是锂也可以通过把电子从最外层的轨道上移除而起到双粒子的作用。锂的电子构型是1s22s1。通过移除2s1电子,它可以变成双星。在这种情况下,He,H-和Li+是可以作为稳定的二元体存在的二元体。
所有的二元体都有如下的电子组态结束。
ns2型

图02:氦,一个双星
八位元(octet)和二分体(duplet)的区别
| 八位对双绞线 | |
| 八电子在最外层有八个电子。 | 杜普勒在最外层有两个电子。 |
| 共电子构型 | |
| 八位元体末端具有ns2 np6型电子构型。 | Duplet在末尾具有ns2类型配置。 |
| 轨道数 | |
| 八位位元的轨道至少有两个。 | 一只双唇只有一个轨道。 |
| 轨道类型 | |
| 八位体可以有各种轨道,如s、p、d、f等。 | 杜普利只有s轨道。 |
总结 - 八位元(octet) vs. 二分体(duplet)
所有元素趋于稳定。但在电子构型不完整的情况下,原子是不稳定的;因此,它们变得非常活跃,以便通过获得、丢失或共享电子来填充壳层中的电子。遵守八重态或双原子规则的原子或分子是稳定的。八重态和二重态的关键区别在于八重态在它的最外层轨道上有八个电子,而双原子态在它的轨道上有两个电子。
R参考文献:1。Nema,P.,2011年。顶级学习。[在线]网址:http://www.topperlearning.com/forums/home-work-help-19/what-is-octet-duplet-valency-and-i***-chemistry-structure-of-the-atom-46317/reply[访问日期:2017年5月29日].2.Chang,R.,2010年。化学。第10版,纽约:麦格劳·希尔,第3版,2015年。坡度堆垛机。[在线]网址:http://gradestack.com/NTSE-Complete-Course/Chemical-Bonding/Chemical-Activity-of-An/19176-3853-37737-study-wtw[访问日期:2017年5月29日]。