为什么水是极性分子?
水是极性分子,也是极性溶剂。当一种化学物质被称为“极性”时,这意味着正负电荷分布不均匀。正电荷来自原子核,而电子提供负电荷。电子的运动决定了极性。以下是它对水的作用方式。

水分子的极性
由于分子的弯曲形状,水(H2O)是极性的。形状是指分子一侧氧原子的大部分负电荷和分子另一侧氢原子的正电荷。这是极性共价化学键的一个例子。当溶质加入水中时,它们可能会受到电荷分布的影响。
分子的形状不是线性和非极性(例如,像二氧化碳)的原因是氢和氧之间电负性的差异。氢的电负性值为2.1,而氧的电负性值为3.5。电负性值之差越小,原子形成共价键的可能性就越大。离子键的电负性值之间存在很大差异。通常情况下,氢和氧都是非金属的,但氧的电负性比氢大,所以两个原子形成共价化学键,但它是极性的。
高电负性氧原子吸引电子或负电荷,使氧周围的区域比两个氢原子周围的区域更负。分子的正电荷部分(氢原子)从两个充满氧的轨道上弯曲开。基本上,两个氢原子都被吸引到氧原子的同一侧,但它们之间的距离尽可能远,因为氢原子都带有正电荷。弯曲构象是吸引和排斥之间的平衡。
请记住,尽管水中的氢和氧之间的共价键是极性的,但水分子总体上是电中性分子。每个水分子有10个质子和10个电子,净电荷为0。
为什么水是极性溶剂
每个水分子的形状影响它与其他水分子和其他物质相互作用的方式。水作为极性溶剂,因为它可以被溶质上的正电荷或负电荷吸引。氧原子附近的轻微负电荷从水或其他分子的正电荷区域吸引附近的氢原子。每个水分子稍微正的氢侧吸引其他氧原子和其他分子的负电荷区域。一个水分子的氢和另一个水分子的氧之间的氢键将水结合在一起,并赋予它有趣的性质,然而氢键不如共价键强。虽然水分子通过氢键相互吸引,但其中约20%在任何给定时间都可以自由地与其他化学物质相互作用。这种相互作用称为水合作用或溶解作用。
- 发表于 2021-09-23 20:23
- 阅读 ( 1445 )
- 分类:科学
你可能感兴趣的文章
极地的(polar)和非极性溶剂(nonpolar solvents)的区别
...得到部分负电荷,而两个氢原子得到部分正电荷。 图01:水是极性溶剂 此外,我们还将极性溶剂分为极性质子溶剂和极性非质子溶剂两大类。极性质子溶剂含有不稳定的H+离子。这意味着这些溶剂的分子可以提供氢原子。然而,...
- 发布于 2020-10-12 14:40
- 阅读 ( 492 )
可溶的(soluble)和不溶性盐(insoluble salts)的区别
...盐在室温下不能溶于水。此外,可溶盐是极性的,这就是为什么它们能溶于水,水是一种极性溶剂。相反,不溶性盐是非极性的。所以,这是可溶盐和不溶盐的另一个显著区别。 除此之外,水分子可与可溶盐离子形成分子间吸...
- 发布于 2020-10-15 09:54
- 阅读 ( 1459 )
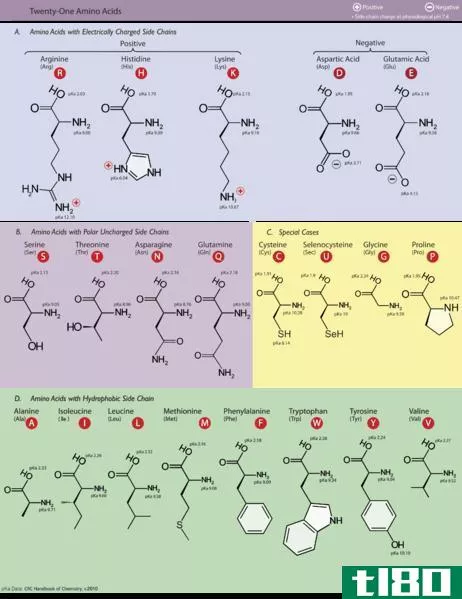
疏水的(hydrophobic)和亲水性氨基酸(hydrophilic amino acids)的区别
...名字的由来是因为它不与水相互作用(“hydro”–水)。水是极性溶剂。由于这些氨基酸是非极性的,它们不能溶于水。 图01:必需氨基酸 因此,这些化合物的疏水性质是由于它们的化学结构中含有侧链。氨基酸的通式是一个中...
- 发布于 2020-10-21 13:31
- 阅读 ( 2029 )
水(water)和冰(ice)的区别
...覆盖了地球表面70%以上的面积。从这一点来看,大部分的水是在海洋中,约占97%。河流、湖泊和池塘有0.6%的水,约2%存在于极地冰盖和冰川中。地下有一定量的水,还有一小部分是以气体形式存在的蒸汽和云中。其中,人类直接...
- 发布于 2020-10-26 16:29
- 阅读 ( 361 )
极地的(polar)和非极性(non-polar)的区别
...其上的大量电荷。具有极性分子的物质的一个例子是水。水是由极性分子组成的,因为原子的排列,加上有大量的正电荷和负电荷。气体类别下的其他例子有:氨、硫,特别是二氧化硫,最后是硫化氢。 非极性物质的例子是碳...
- 发布于 2021-06-23 19:30
- 阅读 ( 397 )
物相(phase of matter)和物质状态(state of matter)的区别
...子松散。分子间的距离刚好足够使它们彼此滑动。这就是为什么液体,虽然没有一个明确的形状,但仍然采取其持有容器的形式。所以它们有一个特定的体积。气态物质有更多的松散分子,它们彼此自由地分散开来。这就是为什...
- 发布于 2021-06-23 20:15
- 阅读 ( 194 )
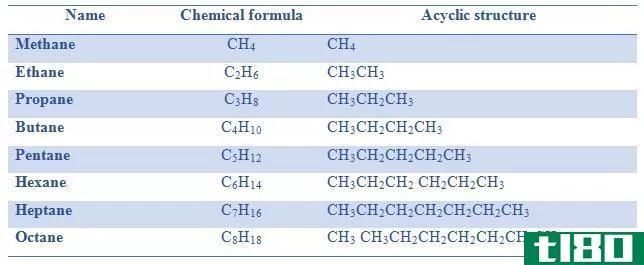
什么是烷烃的性质(the properties of alkanes)
...子量软固体烷烃 溶解度 烷烃是一种非极性有机化合物。水是极性溶剂,所以烷烃不溶于水。它们被称为“憎水”化合物。它们溶解在非极性或弱极性有机溶剂中。烷烃被用作金属的良好润滑剂和防腐剂,因为它们保护金属表面...
- 发布于 2021-06-27 01:54
- 阅读 ( 652 )
共价的(covalent)和氢键(hydrogen bonds)的区别
...生在HF原子之间。 Figure 2: Hydrogen Bonds between Water Molecules 水是具有氢键的化合物最常见的例子。在这里,一个水分子的氧原子可以吸引另一个分子的氢原子,这是由于该分子中的电荷分离。 共价键和氢键的相似性 共价键和氢键...
- 发布于 2021-06-29 11:01
- 阅读 ( 613 )
溶剂(solvent)和溶质(solute)的区别
...在这里,茶是解决办法。糖和奶粉溶于热水中。因此,热水是这里的溶剂。在有机化学实验室中,通过重结晶来纯化化合物是一种常见的实验。在这个实验中,不纯的化合物在溶剂中,溶剂只溶解混合物中需要纯化的化合物,通...
- 发布于 2021-06-29 11:15
- 阅读 ( 917 )
疏水的(hydrophobic)和亲水分子(hydrophilic molecules)的区别
...rence hydrophobic) vs. 亲水分子(hydrophilic molecules) 众所周知,水是溶解我们所知道的大多数化合物的溶剂。但自然界中的所有化合物都不会与水混合。能与水混合的物质称为亲水性物质;不能与水混合的物质称为疏水物质。这主要是...
- 发布于 2021-06-29 14:28
- 阅读 ( 288 )