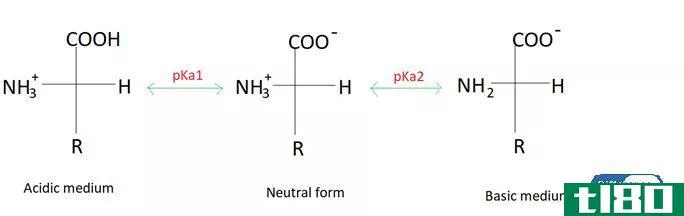
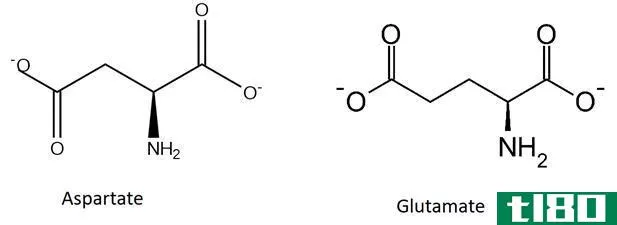
解释了ph、pka、ka、pkb和kb
化学中有一些相关的刻度,用来测量溶液的酸性或碱性以及酸和碱的强度。虽然pH标度是最常见的,但pKa、Ka、pKb和Kb是常见的计算方法,可以深入了解酸碱反应。下面是对这些术语的解释,以及它们之间的区别。

“p”是什么意思?
每当你在一个值前面看到一个“p”,比如pH、pKa和pKb,这意味着你在处理一个在“p”后面的-log值。例如,pKa是Ka的-log。由于log函数的工作方式,较小的pKa意味着较大的Ka。pH值是氢离子浓度的对数,依此类推。
ph和平衡常数的公式和定义
pH和pOH是相关的,就像Ka、pKa、Kb和pKb一样。如果你知道pH值,你可以计算pOH。如果你知道一个平衡常数,你可以计算其他的。
关于ph值
pH值是水(水)溶液中氢离子浓度[H+]的量度。pH值范围为0至14。pH值低表示酸度,pH值7表示中性,pH值高表示碱性。pH值可以告诉你是处理酸还是碱,但它提供的值有限,表明碱中酸的真实强度。计算pH和pOH的公式如下:
pH=-log[H+]
pOH=-log[OH-]
25摄氏度时:
pH+pOH=14
理解ka和pka
Ka、pKa、Kb和pKb在预测一个物种是否会在特定pH值下捐献或接受质子时最有帮助。它们描述了酸或碱的电离程度,是酸或碱强度的真实指示器,因为向溶液中加水不会改变平衡常数。Ka和pKa与酸有关,而Kb和pKb与碱有关。与pH和pOH一样,这些值也说明了氢离子或质子浓度(对于Ka和pKa)或氢氧化物离子浓度(对于Kb和pKb)。
Ka和Kb通过水的离子常数(Kw)相互关联:
- 千瓦=Ka×Kb
Ka是酸离解常数。pKa只是这个常数的-log。类似地,Kb是碱基离解常数,而pKb是该常数的-log。酸碱离解常数通常以摩尔每升(mol/L)表示。酸和碱根据一般方程式离解:
- HA+H2O⇆ A-+H3O+
- 血红蛋白+H2O⇆ B++哦-
在公式中,A代表酸,B代表碱。
- Ka=[H+][A-]/[HA]
- pKa=-log Ka
- 在一半的等效点处,pH=pKa=-log Ka
较大的Ka值表示强酸,因为这意味着酸在很大程度上分解为离子。较大的Ka值也意味着有利于在反应中形成产物。一个小的Ka值意味着很少的酸离解,所以你们有一个弱酸。大多数弱酸的Ka值范围为10-2至10-14。
pKa提供了相同的信息,只是方式不同。pKa值越小,酸性越强。弱酸的pKa范围为2-14。
理解kb和pkb
Kb是碱基离解常数。碱离解常数是衡量碱在水中离解成其组成离子的程度。
- Kb=[B+][OH-]/[BOH]
- pKb=-log Kb
较大的Kb值表示强碱的离解程度较高。pKb值越低,说明基础越强。
pKa和pKb通过简单关系进行关联:
- pKa+pKb=14
什么是圆周率(pi)?
另一个重要点是pI。这是等电点。它是蛋白质(或其他分子)电中性(无净电荷)的pH值。
- 发表于 2021-10-07 23:30
- 阅读 ( 646 )
- 分类:化学
你可能感兴趣的文章
等电性(isoelectric)和等离子点(isoionic point)的区别
...别-等电点与等离子点 等电点和等离子点这两个术语描述了关于氨基酸的相同的生化概念;等电点或等离子点是指氨基酸的正电荷等于同一氨基酸的负电荷的pH值。因此,等电点和等离子点没有区别。 目录 1. 概述和主要区别 2. ...
- 发布于 2020-10-19 01:29
- 阅读 ( 755 )
酸的(acidic)和碱性氨基酸(basic amino acids)的区别
...部分。一个氨基酸链被称为多肽,几个多肽链的结合形成了一个蛋白质分子。酸性氨基酸和碱性氨基酸的主要区别在于酸性氨基酸有酸性侧链,而碱性氨基酸在中性pH下有碱性侧链。 氨基酸分子有四部分:羧酸基、胺基、氢原子...
- 发布于 2020-10-19 01:54
- 阅读 ( 426 )
酸电离常数(acid ionization constant)和碱基电离常数(base ionization constant)的区别
...离常数 酸离子化常数(Ka,也称为酸离解常数)定量测量了酸分子与其电离形式之间的平衡。同样,碱离解常数(Kb,或碱离解常数)可定量测量碱分子与其电离形式之间的平衡。酸电离常数和碱电离常数的关键区别在于,酸电...
- 发布于 2020-10-19 03:06
- 阅读 ( 435 )
酸度(acidity)和碱度(basicity)的区别
...电负性的原子可以吸引电子。电负性越高,碱度越低。为了释放氢氧化离子,氧原子和分子其余部分之间的键电子应完全被氧原子吸引(氢氧化基团中的氧原子应比它所连接的另一个原子更具电负性)。例:如果ROH的碱度高,R...
- 发布于 2020-10-19 11:23
- 阅读 ( 386 )
pka公司(pka)和巴基斯坦卢比(pkb)的区别
...一种比苯酚更强的酸,因为它比硝基苯酚的pKa值小。 除了比较酸强度外,还利用pKa值来选择合适的缓冲液。根据Henderson-Hasselbalch方程,体系的pH值与pKa之间存在一定的关系。 pH=pKa+log10([A–]/[AH]) 用于腐植酸的分解。这个等式...
- 发布于 2020-10-19 14:31
- 阅读 ( 513 )
如何计算缓冲容量(calculate buffer capacity)
...冲液 缓冲液的制备 当我们准备缓冲溶液时,我们取, pKa值与所需pH值最接近的酸及其结合碱或, 与所需pH值最接近的14 pKb的碱及其结合酸盐。 缓冲比 两组分的缓冲比由著名的亨德森-哈塞尔-巴赫方程求得 pH=pKa+对数B/A(B=碱...
- 发布于 2021-06-27 00:24
- 阅读 ( 1018 )
巴基斯坦航空公司(pka)和酸碱度(ph)的区别
...或非常小的量的最简单方法是取它们的对数值。对数给出了一个很容易处理的简单值。pKa和pH的主要区别在于pKa表示酸的离解,而pH表示体系的酸碱度。 覆盖的关键领域 1.什么是pKa–定义、价值观、关系2.什么是pH–定义、价值观...
- 发布于 2021-06-28 20:09
- 阅读 ( 331 )
酸碱度(ph)和酸度(acidity)的区别
...差异ph值(main difference ph) vs. 酸度(acidity) pH和酸度是相互解释的相关术语。酸度是溶液中氢离子的量。pH是用来测量溶液中氢离子含量的刻度。因此,pH可以量化系统的酸度。这些术语通常用于解释水体行为和性质的水化学。pH和...
- 发布于 2021-06-29 08:16
- 阅读 ( 487 )
坚强的(strong)和弱碱(weak bases)的区别
...做平衡常数Kb。对于弱碱基,Kb值非常低。换言之,如果pKb值非常高,它就具有弱碱的特征。但如果pKb值很低,则可归类为强基而不是弱基。 坚强的(strong)和弱碱(weak bases)的区别 定义 强碱:强碱是一种能在水溶液中完全分解成阳...
- 发布于 2021-06-29 13:55
- 阅读 ( 469 )
坚实的基础(strong base)和弱碱(weak base)的区别
...碱是好的电解质,弱碱则不是。结论离解离子的倾向决定了碱的强度。每个强碱有一个共轭弱酸,弱碱有它的共轭强酸。在酸碱反应中,强碱与酸作用强烈,而弱碱与酸作用温和。这两个基础都有其重要性,不能相互取代。参考...
- 发布于 2021-07-10 21:02
- 阅读 ( 207 )