滴定和中和的关键区别在于滴定是一种分析技术,而中和是一种化学反应。
滴定和中和是化学中非常重要的术语。滴定法是一种需要特定仪器的技术,它是在中和反应的基础上进行的。中和反应是一种化学反应,通过添加碱来平衡酸度,反之亦然,从而得到中性溶液。
目录
1. 概述和关键区别
2. 什么是滴定
3.什么是中和
4. 并列比较-滴定法与表格中和法
5. 摘要
什么是滴定法(titration)?
滴定法是一种用于测量某种化学溶液浓度的分析技术。我们可以用已知浓度的溶液来做。滴定过程需要特定的仪器。
在滴定仪器中,有一个滴定管,它通常含有已知浓度的标准溶液。如果滴定管中的溶液不是标准溶液,则应使用一级标准溶液对其进行标准化。将含有未知浓度化学成分的样品装入滴定瓶中。如果标准溶液(滴定管中)不能作为自指示剂,则应在滴定瓶中的样品中添加合适的指示剂。
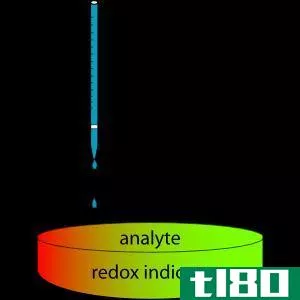
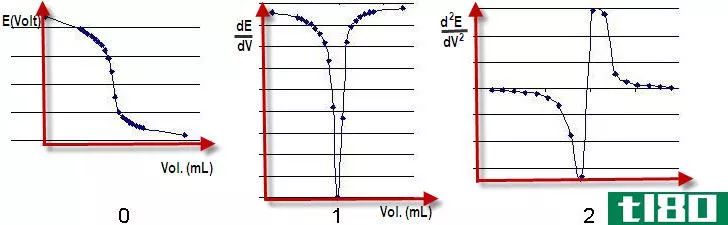
图01:滴定反应
在滴定过程中,将标准溶液缓慢添加到烧瓶中,直到颜色发生变化。分析物溶液的颜色变化表明滴定终点。虽然它不是滴定结束的确切点,但我们可以假设它是等效点,因为只有一点差别(等效点是反应实际停止的点)。
滴定管读数有助于确定与样品反应的标准溶液的量。然后利用化学反应和化学计量关系,计算出未知物质的浓度。
什么是中和(neutralization)?
中和是指酸和碱之间的化学反应,产生中性溶液。中性溶液的pH值为pH=7。中和反应包括H+离子和OH-离子结合形成水分子。

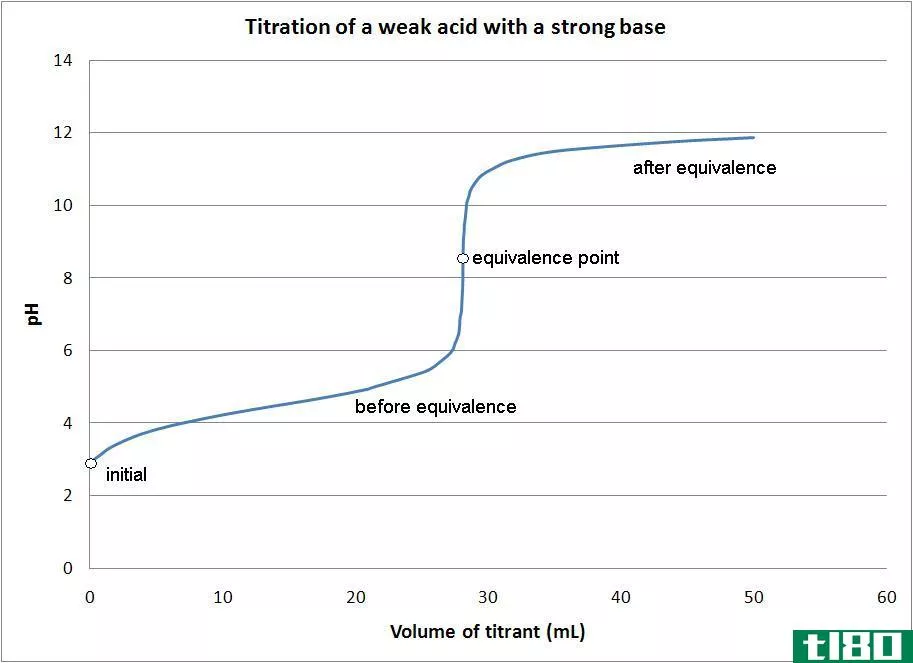
图02:氢氧化钠和盐酸的中和
反应的最后一个反应是,与一个氢离子和一个碱基离子反应。酸可以是强碱,也可以是弱碱。根据酸和碱的性质,有几种类型的中和反应,如下所示:
- 强酸强碱反应
- 强酸弱碱反应
- 弱酸弱碱反应
- 弱酸强碱反应
在这四种类型中,只有强酸和强碱之间的反应才能得到pH值为7的中和溶液。其他反应产生的中和溶液由于酸碱的pH值变化而变化。
滴定法(titration)和中和(neutralization)的区别
滴定和中和是化学中非常重要的术语。滴定法是一种需要特定仪器的技术,它是在中和反应的基础上进行的。滴定和中和的关键区别在于滴定是一种分析技术,而中和是一种化学反应。
下面的信息图以表格形式比较了滴定法和中和法之间的差异。

总结 - 滴定法(titration) vs. 中和(neutralization)
滴定和中和是化学中非常重要的术语。滴定法是一种需要特定仪器的技术,它是在中和反应的基础上进行的。滴定和中和的关键区别在于滴定是一种分析技术,而中和是一种化学反应。
引用
1.“滴定。”化学歌词,歌词,2019年6月23日,可在此处查阅。