均衡和中和的关键区别在于,均衡是指化学反应方程式中原子的平衡,而中和是平衡酸碱度以获得中性溶液。
虽然“均衡”和“中和”这两个词听起来很相似,但它们在含义和应用上却各不相同。然而,这两个术语都指化学成分的平衡过程。
目录
1. 概述和主要区别
2. 什么是均衡
3. 什么是中和
4. 并列比较——表格形式的均衡与中和
5. 摘要
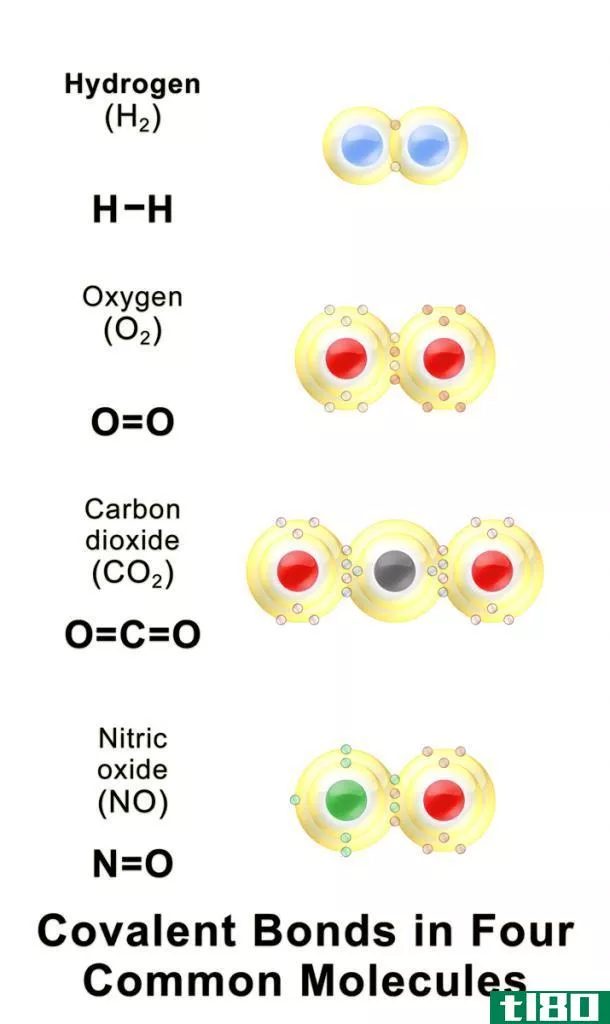
什么是均衡(equalization)?
均衡是平衡化学反应方程式中的原子的技术。这里,我们必须使反应物侧的原子数与产物侧的原子数相等。这意味着化学反应前后的原子数必须相等。为此,我们可以在反应物和产物前面使用化学计量系数(化学计量系数是指在化学反应方程式中化学物种符号之前出现的数字)。这些值是无单位值)。
以下步骤帮助我们平衡一个简单化学反应的化学方程式。
- 写下不平衡方程式。(例如C3H8+O2⟶CO2+H2O)
- 测定反应物和产物中每个原子的数目。(反应物侧有8个氢原子,3个碳原子和2个氧原子。在产品侧,有2个氢原子、3个氧原子和1个碳原子)。
- 把氢和氧原子留到最后。
- 使用化学计量系数来平衡单个元素。(在CO2前面使用化学计量系数“3”)例如C3H8+O2⟶3CO2+H2O
- 平衡氢原子的数量。(反应物侧有8个氢原子,而产物侧只有2个氢原子,因此,在H2O前面应使用化学计量系数4),例如C3H8+O2⟶3CO2+4H2O
- 平衡氧原子的数量。E、 g.C3H8+5O2⟶3CO2+4H2O
什么是中和(neutralization)?
中和反应是酸和碱之间的化学反应,产生中性溶液。中性溶液的pH值始终为7。这个反应包括H+离子和OH-离子结合形成水分子。
如果酸碱反应混合物的最终pH值为7,则意味着在此处反应了等量的H+和OH-离子(为了形成水分子,需要一个H+离子和一个OH-离子)。酸可以是强碱,也可以是弱碱。根据这一事实,反应各不相同。

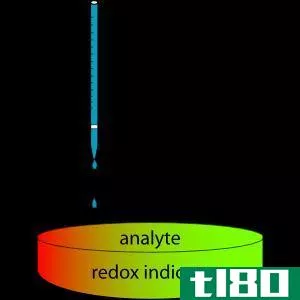
图01:强酸-强碱中和滴定
中和反应有四种不同类型:强酸强碱反应、强酸弱碱反应、弱酸弱碱反应和弱酸弱碱反应。根据酸和碱的强度,这些反应在不同程度上经历中和。
均衡(equalization)和中和(neutralization)的区别
均衡和中和的关键区别在于,均衡是指化学反应方程式中原子的平衡,而中和是平衡酸碱度以获得中性溶液。此外,均衡包括使用反应物和产物中的原子数和原子的氧化状态,而中和则涉及到确定反应中涉及的酸和碱的强度。
下面的信息图总结了均衡和中和之间的区别。
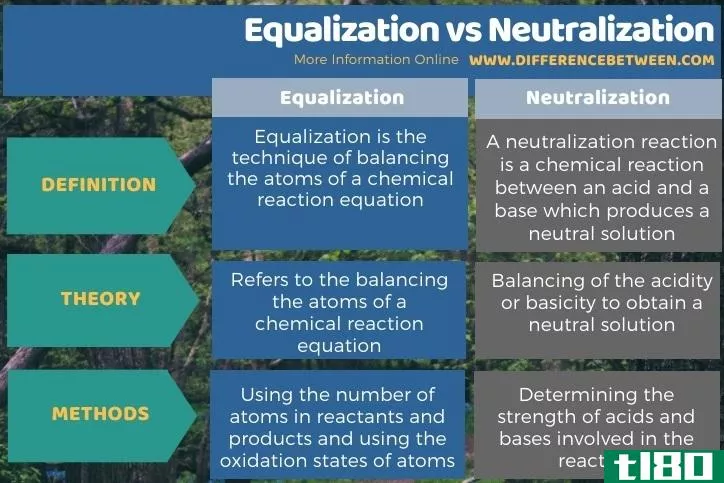
总结 - 均衡(equalization) vs. 中和(neutralization)
虽然“均衡”和“中和”这两个词听起来很相似,但它们在定义和应用上却各不相同。均衡与中和的关键区别在于,均衡是指平衡化学反应方程式中的原子,而中和则是平衡酸碱度以获得中性溶液。