酯化和中和的关键区别在于酯化反应从酸和醇中生成酯,而中和反应从酸和碱中生成盐。
酯化反应和中和反应是两个重要的化学反应。酯化,顾名思义,是一种在反应结束时生成酯的化学反应。中和是指酸碱平衡。
目录
1. 概述和主要区别
2. 什么是酯化反应
3. 什么是中和
4. 并列比较-酯化与中和的表格形式
5. 摘要
什么是酯化(esterification)?
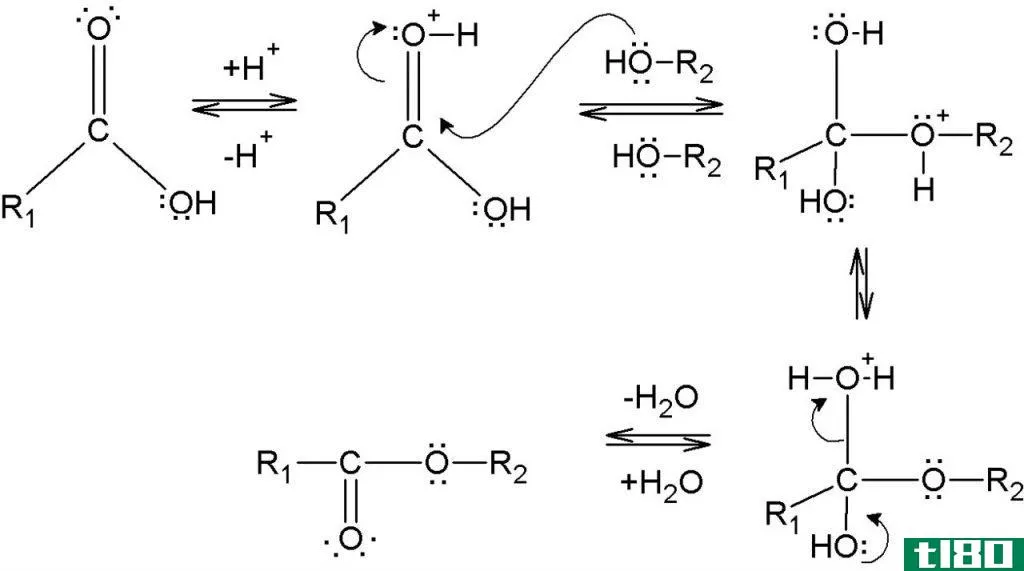
酯化是由酸和醇形成酯的过程。酸通常是一种羧酸,而酒精必须是一级或二级醇。反应发生在酸性环境中。因此,我们用硫酸作为反应的强酸。它作为反应的催化剂,因为如果介质不酸性,羧酸和酒精的混合物不会产生任何反应。作为副产品,水分子形成了。因此,这是一个缩合反应。
由于氧原子和碳原子的电负性不同,电子发生畸变,羧酸羰基中的π键可以起到碱的作用。π键中的电子给了硫酸分子中的一个氢原子。因此,这将-C=O键转换成-C-OH。

图01:酯化反应示例
在这里,碳原子带正电荷,因为它周围只有三个化学键。我们称之为碳阳离子。在乙醇存在的情况下,酒精氧原子中的孤电子对可以给碳阳离子的碳原子提供电子。因此,酒精起到亲核的作用。然后,重排发生并形成酯和水分子。
什么是中和(neutralization)?
中和是一种化学反应,其中酸与碱反应生成盐和水。因此,这个反应涉及到H+离子和OH-离子的结合,并产生水。因此,在反应完成后,反应混合物中没有过量的氢离子或氢氧化物离子。

如果强酸与强碱反应,则最终反应混合物的pH值为7。除此之外,反应混合物的pH值取决于反应物的酸强度。在考虑中和的应用时,在确定未知的酸或碱浓度、废水处理工艺、用抗酸片中和过量胃酸等方面都很重要。
酯化(esterification)和中和(neutralization)的共同点
- 这两种反应都产生水作为副产品
- 这两种反应都涉及到H+离子和OH-的结合
酯化(esterification)和中和(neutralization)的区别
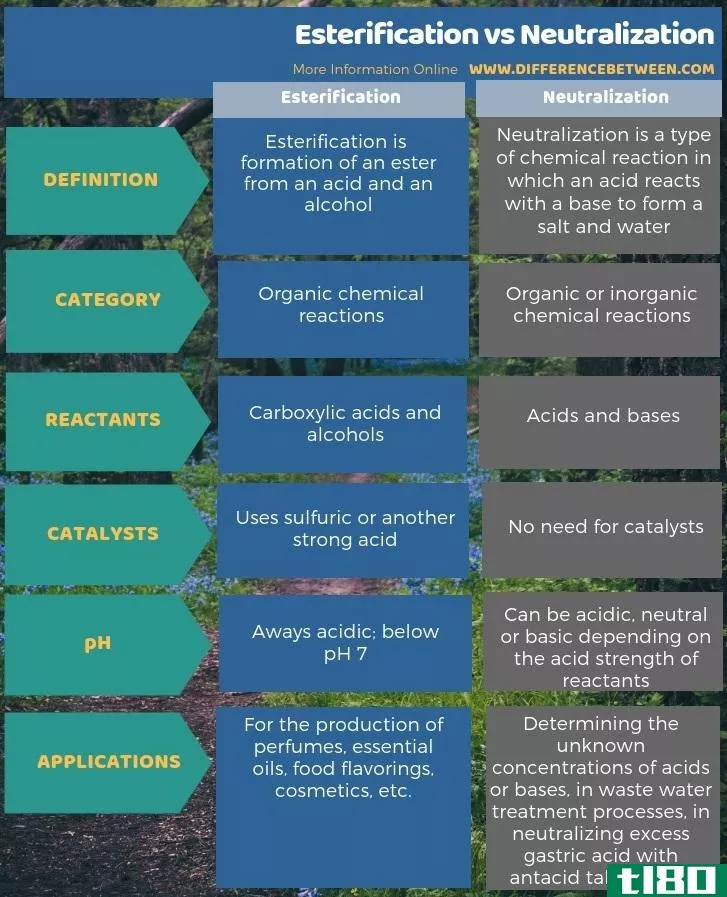
酯化反应和中和反应是化学中的重要反应。酯化和中和的关键区别在于酯化反应从酸和醇中生成酯,而中和反应从酸和碱中生成盐。酯化反应物为羧酸和醇类,中和反应物为酸和碱。
此外,酯化和中和的另一个区别是酯化需要硫酸等催化剂,而中和不需要任何催化剂。
总结 - 酯化(esterification) vs. 中和(neutralization)
酯化反应和中和反应是化学中的重要反应。总之,酯化和中和的关键区别在于酯化反应从酸和醇中生成酯,而中和反应从酸和碱中生成盐。
引用
1“酯化机理(有机化学)–ChemistryScore.”学习化学,2018年9月19日,可在此处获取。管理员。“酯——具有结构、性质和用途的酯化过程”,BYJUS,Byju's,2018年7月25日,可在此处查阅。
2管理员。“酯-酯化过程及其结构、性质和用途”,BYJUS,Byju,2018年7月25日,