共价性(covalency)和氧化态(oxidation state)的区别
不同化学元素的原子相互结合形成不同的化合物。在化合物的形成过程中,原子通过离子键或共价键相互结合。共价态和氧化态是描述化合物中这些原子状态的两个术语。共价性是原子能形成的共价键的数目。因此,共价性取决于原子能与其他原子共享的电子数。当某个原子或某个原子的某个化学键被氧化而失去时。共价态和氧化态的关键区别在于,原子的共价性是原子能形成的共价键的数目,而原子的氧化态则是原子在形成化学键时丢失或获得的电子数。
目录
1.概述和主要区别
2. 什么是共价性
3. 什么是氧化状态
4. 并列比较-共价性与氧化状态的表格形式
5. 摘要
什么是共价性(covalency)?
共价性是一个原子能与其他原子形成共价键的数目。因此,共价性是由原子最外层轨道上的电子数决定的。但是,不应混淆“价”和“共价性”,因为它们有不同的含义。价是原子的结合力。有时,共价性等于价。然而,这并不总是发生。
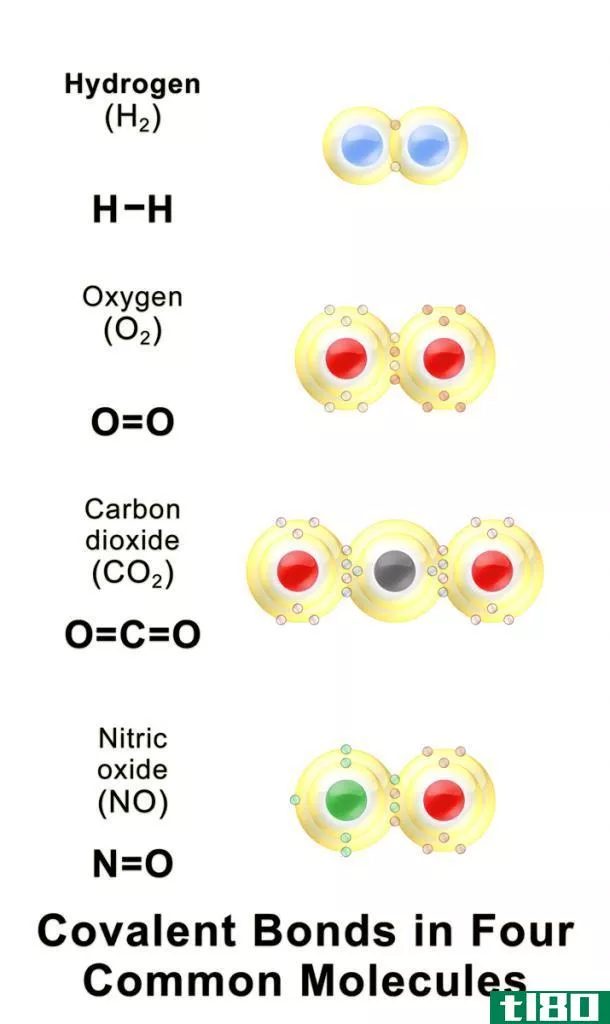
图01:一些常见的共价化合物
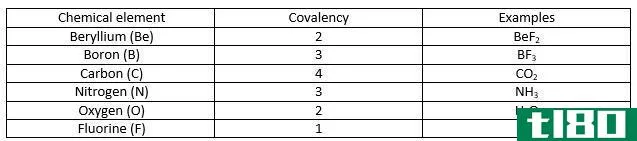
共价键是两个原子共享其最外层未成对电子以完成电子组态时形成的化学键。当一个原子有不完整的电子壳层或轨道时,由于不完整的电子构型是不稳定的,该原子会变得更加活跃。因此,这些原子要么获得/释放电子,要么共享电子以填充电子壳层。下表显示了具有不同共价值的化学元素的一些示例。
什么是氧化态(oxidation state)?
一个原子的氧化态是该原子与另一个原子失去、获得或共享的电子数。如果电子丢失或获得,原子的电荷也随之改变。电子是带负电的亚原子粒子,其电荷被原子中质子的正电荷中和。当电子丢失时,原子得到正电荷,而当获得电子时,原子得到净负电荷。这是由于原子核中质子的正电荷不平衡造成的。这个电荷可以算作那个原子的氧化态。
原子的氧化状态用一个带正负号的整数来表示。或者表示原子失去了电子。这个整数表示原子间交换的电子数。
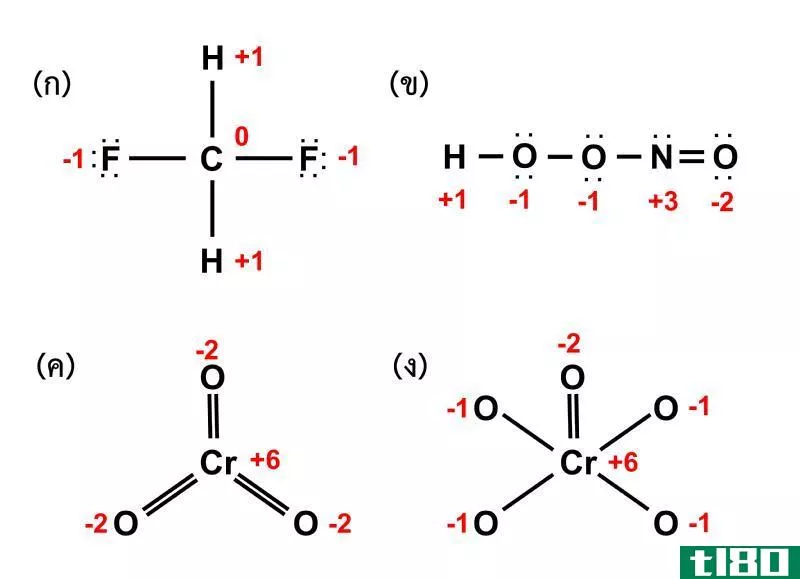
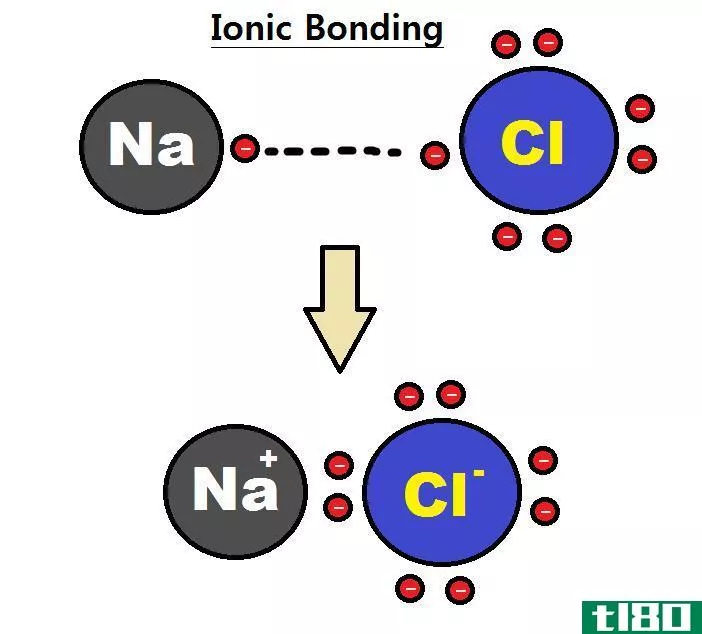
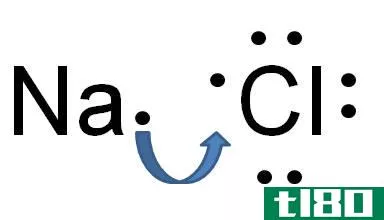
图02:不同化合物的氧化状态
原子氧化态的测定
一个特定原子的氧化状态可以用下面的规则来确定。
- The oxidation state of a neutral element is always zero. Ex: Oxidation state of sodium (Na) is zero.
- The total charge of the compound should equal to the sum of the charges of each atom present in that compound. Ex: The total charge of KCl is zero. Then the charges of K and Cl should be +1 and -1.
- The oxidation state of group 1 element is always +1. The group 1 elements are Lithium, Sodium, Potassium, Rubidium, Cesium and Francium.
- The oxidation state of group 2 elements is always +2. The group 2 elements are Beryllium, Magnesium, Calcium, Strontium, Barium and Radium.
- The negative charge is given to the atom having a higher electronegativity than that of the other atoms bonded to it.
- The oxidation state of hydrogen is always +1 except when hydrogen is bonded to a group 1 metal.
- The oxidation state of oxygen is -2 except when it is in the form of peroxide or superoxide.
共价性(covalency)和氧化态(oxidation state)的区别
| 共价性与氧化态 | |
| 共价性是一个原子能与其他原子形成共价键的数目。 | 一个原子的氧化态是该原子与另一个原子失去、获得或共享的电子数。 |
| 电荷 | |
| 共价性并不表示原子的电荷。 | 氧化态产生原子的电荷。 |
| 化学键合 | |
| 共价性表示一个特定原子可以有多少化学键(共价键)。 | 氧化态不提供原子形成的化学键的细节。 |
| 元素的状态 | |
| 纯元素的共价性取决于该元素原子最外层电子壳层中的电子数。 | 纯元素的氧化态总是零。 |
总结 - 共价性(covalency) vs. 氧化态(oxidation state)
原子的共价性和氧化态描述了化合物中原子的化学性质。共价态和氧化态的区别在于,原子的共价性是原子能形成的共价键的数目,而原子的氧化态则是原子在形成化学键时丢失或获得的电子数。
引用
1.“共价性”com,Dictionary.com网站. 可在这里查阅2.“氧化状态”,维基百科,维基媒体基金会,2018年3月5日。可在这里查阅3.“化学共价性和分子结构”。com。此处提供
2.“氧化状态”,维基百科,维基媒体基金会,2018年3月5日
化学共价性和分子结构。