关键区别-亚铜与铜
d嵌段元素铜形成的稳定阳离子为亚铜阳离子和铜阳离子。亚铜和铜离子根据它们的电子构型而不同。铜和铜的主要区别在于,亚铜是铜1+阳离子,而铜是铜+2阳离子。
目录
1.概述和主要区别
2. 什么是铜
3. 铜是什么
4. 铜与铜的相似性
5. 并列比较-亚铜与亚铜的表格形式
6. 摘要
什么是亚铜(cuprous)?
铜的名字是由铜原子形成的+1阳离子。用Cu+1表示。铜原子的电子构型为[Ar]3d104s1。当亚铜离子形成时,电子构型为[Ar]3d10 4s0。因此,当一个电子从铜原子中移除时,就形成了亚铜阳离子。由于亚铜阳离子只能与一种具有-1氧化状态的阴离子结合,因此亚铜阳离子被称为单价阳离子。铜离子的电子构型非常稳定。因此,有许多由这种阳离子形成的化合物。示例如下:
- 氧化亚铜(Cu2O)
- 碘化亚铜
- 硫化亚铜(Cu2S)
分子或离子的水化能是一摩尔化合物水合(溶解于水)时释放的能量。
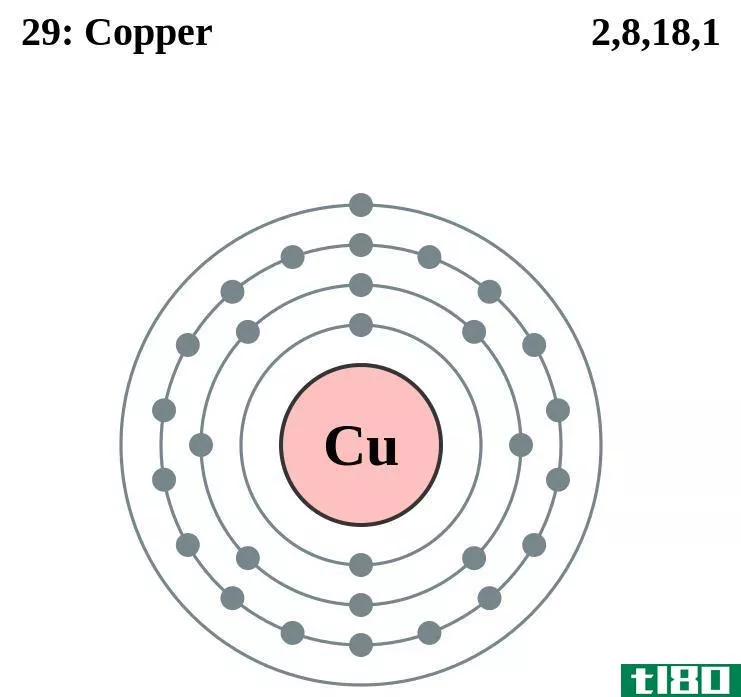
图01:铜的原子结构
与铜离子相比,亚铜离子具有较低的水合能,因为亚铜离子中的d10电子构型比铜离子中的d9电子构型稳定。
什么是铜(cupric)?
铜原子是铜原子形成的+2阳离子。用Cu2+表示。铜原子的电子构型为[Ar]3d104s1。当铜离子形成时,电子构型为[Ar]3d9 4s0。铜离子是当两个电子从一个铜原子上移除时形成的,给这个原子带上2+的电荷。铜离子可与两个具有-1氧化状态的阴离子或一个具有-2氧化状态的阴离子结合。因此,铜离子是二价阳离子。由该阳离子形成的化合物包括:
- 氧化铜(CuO)
- 碘化铜
- 硫化铜(CuS)
亚铜(cuprous)和铜(cupric)的共同点
- 铜和铜都是铜原子失去电子而形成的阳离子。
- 它们都是稳定的阳离子。
- 两者都带有正电荷。
- 两者的原子质量相同(因为电子的质量可以忽略不计)。
亚铜(cuprous)和铜(cupric)的区别
| 亚铜vs铜 | |
| 铜的名字是由铜原子形成的+1阳离子。 | 铜原子是铜原子形成的+2阳离子。 |
| 类别 | |
| 亚铜离子是一价阳离子。 | 铜离子是二价阳离子。 |
| 电子组态 | |
| 亚铜离子的电子构型为[Ar]3d104s0。 | 铜离子的电子构型为[Ar]3d9 4s0。 |
| 形成铜原子所损失的电子 | |
| 当铜原子失去一个电子时,就会形成亚铜离子。 | 铜离子是在铜原子失去两个电子时形成的。 |
| 稳定性 | |
| 由于d10电子组态,亚铜离子的稳定性很高。 | 由于d9电子组态,铜离子的稳定性较低。 |
| 表示 | |
| 亚铜离子用Cu+1表示。 | 铜离子用Cu2+表示。 |
| 电荷 | |
| 亚铜离子有+1电荷。 | 铜离子有+2电荷。 |
| 水化能 | |
| 与铜离子相比,亚铜离子的水化能较低。 | 铜离子的水化能比铜离子高。 |
总结 - 亚铜(cuprous) vs. 铜(cupric)
铜离子和铜离子是铜原子由于电子的丢失而形成的阳离子。铜与铜的区别在于,铜是铜1+阳离子,铜是铜+2阳离子。
引用
1“铜”,维基百科,维基媒体基金会,2018年4月3日。这里有2个。国家生物技术信息中心。公共化学化合物数据库,美国国家医学图书馆。此处提供
2国家生物技术信息中心。公共化学化合物数据库,美国国家医学图书馆。















