主要区别
电离和离解的主要区别在于电离总是产生带电粒子,而离解可能产生也可能不产生带电粒子。
电离(ionization) vs. 离解(dissociation)
电离是分子或原子获得负电荷或正电荷的过程,而离解是将化合物分解成更小的粒子,如分子、离子或原子。电离给出了离子形成的概念,而离解则讨论了大分子化合物中小组分的形成。当一个分子或一个原子失去或获得一个电子(或几个电子)时,就会发生电离;另一方面,离解是由于以热的形式增加能量和溶剂的加入而发生的。最终,电离总是形成离子;相反,最终,离解的产物,总是产生比初始物质更小的原子、离子或分子。电离包括在贡献物种之间产生电荷;相反,由于物种之间的弱键,会发生离解。电离包括极性共价化合物或金属作为初始化合物,而离解包含离子化合物。电离是一个不可逆的过程,而离解是一个可逆的过程。电离包含原子间的共价键;相反,离解涉及其化合物中的离子键。
比较图
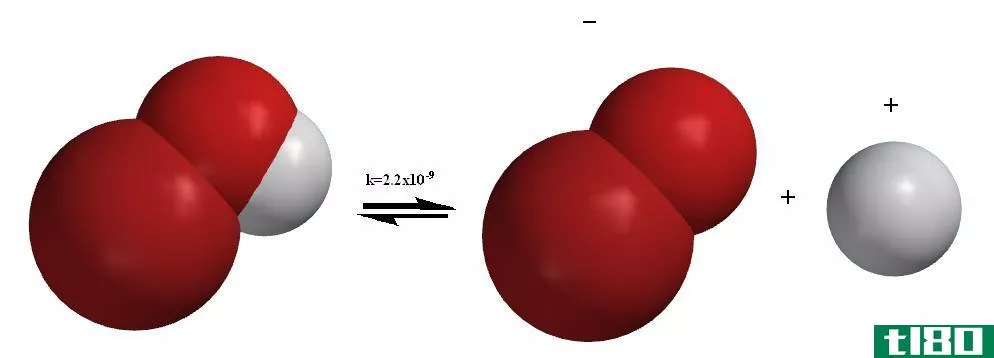
什么是电离(ionization)?
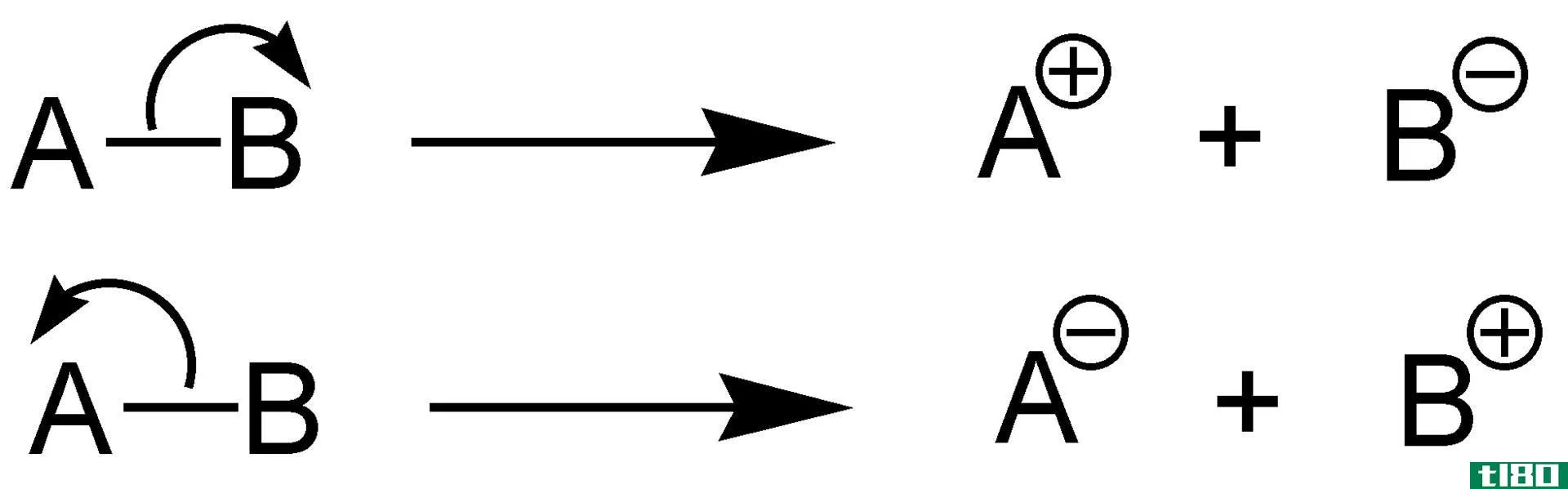
电离是一种分子或原子通过失去或获得电子而获得正电荷或负电荷的方法,这种方法通常与其他化学变化相结合,由此产生的带电分子或原子称为离子。电离通常是由于一个电子在与其他原子碰撞后,在与亚原子粒子、分子和离子碰撞后损失的。电离是通过内部转换过程发射辐射来实现的,在这个过程中,被激发的原子核将其能量传递给一个内壳层电子,使其发射出去。电离是一个不可逆的过程。日常使用电离是在荧光灯或其他电放电灯。它也可用于盖革-穆勒计数器或电离室,即辐射探测器。
电离过程广泛应用于工业或基础科学的各种设备中。当一个自由电子与一个原子相撞,然后被困在势垒内,释放出多余的能量,就形成了带负电荷的离子。整个过程被称为电子俘获电离。正电荷离子是在与光子或带电粒子碰撞时将一定量的能量传递给束缚电子而形成的。所需能量的起始量称为电离势。绝热电离是一种电离形式,在这种电离中,由于处于最低能量状态的离子,电子被添加或移除到处于最低能量状态的原子或分子中。
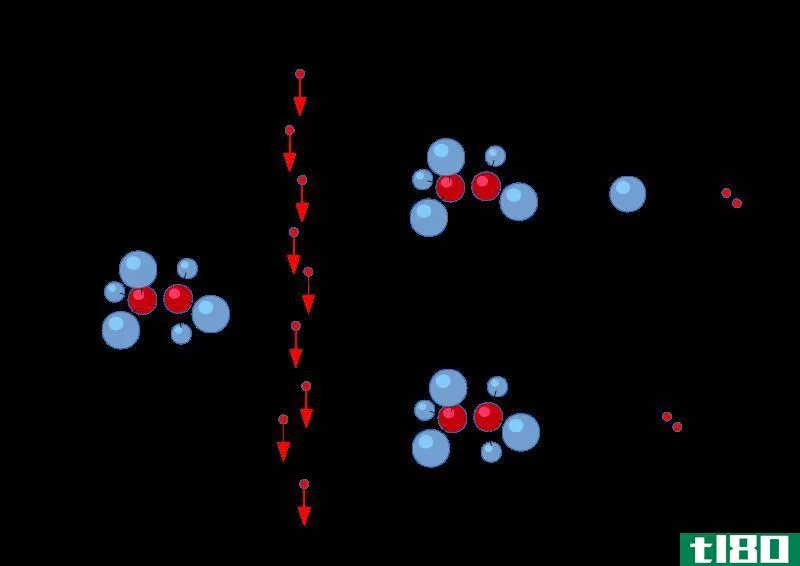
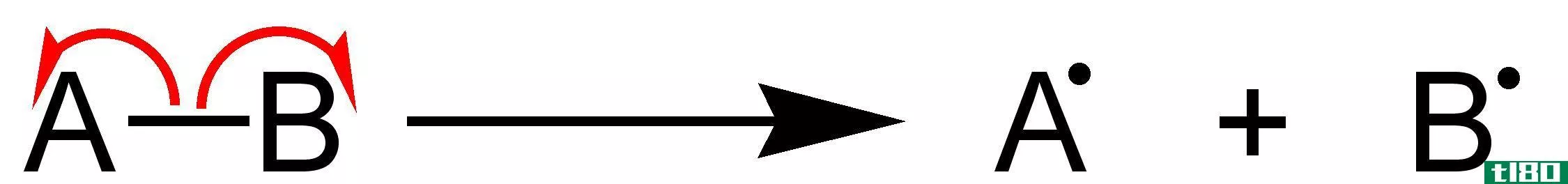
什么是离解(dissociation)?
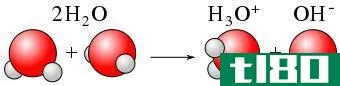
离解是一个普遍的过程,分子分裂或分离成更小的粒子,如离子、原子或自由基,通常是以可逆的方式,因为这些较小的粒子通常能够在给定的条件下重新组合在一起。解离的主要原因是以热的形式增加能量和溶剂的加入。当离子络合物溶解在水中时,它会分解成离子元素。例如,当NaCl溶解在水中时,得到的溶液含有Cl-阴离子和Na+阳离子。
离解相关术语
- 离解常数:离解常数通常是离解后反应物浓度与产物浓度之比。如果温度不变,这种离解就有一个定值。
- 离解度:离解度是原始溶质分子已经离解的片段,通常用希腊语符号α表示。解离度是指每摩尔解离的分子量。较弱的酸的离解程度较低,对于非常强的酸和碱,离解度将接近1。
主要区别
- 电离是分子或原子获得带电粒子的方法,而离解是将化合物分解成更小的粒子,如分子、离子或原子。
- 离子化是离子的产生,而离解是大分子化合物中小组分的形成。
- 当一个分子或一个原子失去或获得一个电子(或几个电子)时,就会发生电离;另一方面,解离是由于以热的形式增加能量和溶剂的加入而发生的。
- 电离的最终产物总是离子;相反,离解的最终产物总是产生比初始物质更小的原子、离子或分子。
- 电离包含极性共价化合物或金属,而离解则包含离子化合物。
- 电离是一个不可逆的过程,而离解是一个可逆的过程。
- 电离包含原子间的共价键;相反,离解涉及其化合物中的离子键。
结论
以上讨论得出结论:电离是在原化合物中不存在的新的带电粒子的形成,而离解是化合物中已经存在的带电粒子的分离。