键能和键离解能的关键区别在于键能是一个平均值,而键离解能是一个特定键的特定值。
正如美国化学家G.N.Lewis提出的那样,当原子的价壳层中含有8个电子时,原子是稳定的。大多数原子的价壳层中的电子少于8个(周期表第18组中的稀有气体除外);因此,它们是不稳定的。因此,这些原子趋向于相互反应,变得稳定。根据原子的电负性,它可以通过形成离子键、共价键或金属键来实现。当两个原子具有相似或极低的电负性差时,它们一起反应,通过共享电子形成共价键。键能和键离解能是共价化学键的两个概念。
目录
1. 概述和主要区别
2. 什么是键能
3. 什么是键离解能
4. 并列比较-键能与键离解能的表格形式
5. 摘要
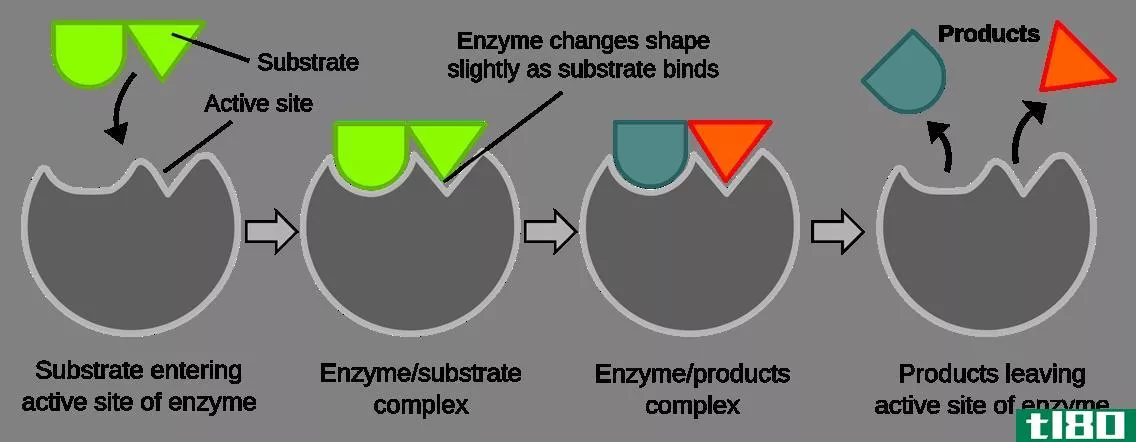
什么是键能(bond energy)?
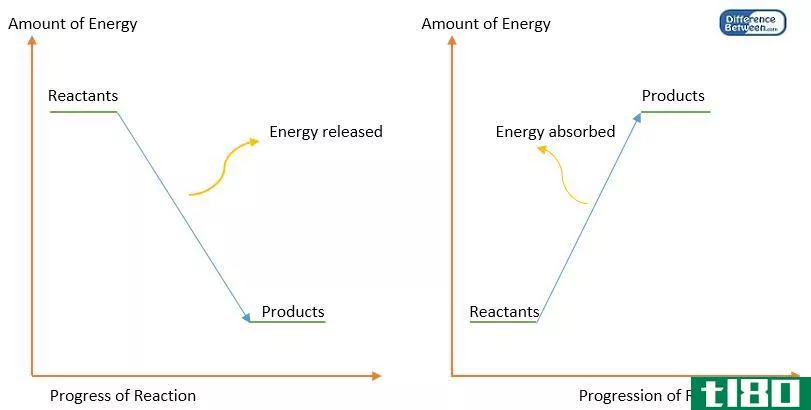
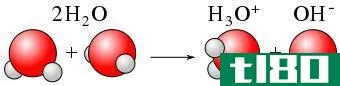
当键形成时,释放出一定量的能量。相反,键断裂需要一些能量。对于某种化学键,这个能量是恒定的。我们称之为能量和能量。因此,键能是将一摩尔分子分解成相应的原子所需的热量。
此外,我们可以观察到化学键的各种形式的能量,如化学能、机械能或电能。然而,最终,所有这些能量转化为热。因此,我们可以用千焦耳或千卡来测量键能。
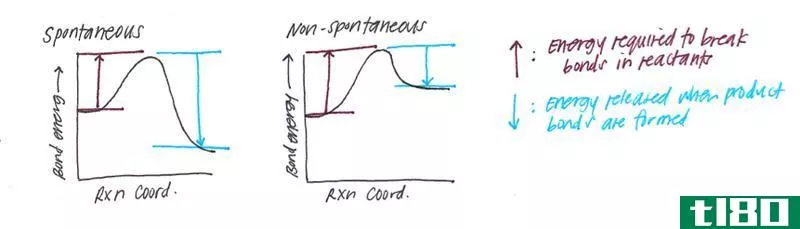
图01:键能
此外,键能是键强度的一个指标。例如,更牢固的键很难分裂。因此,它们的键能更大。另一方面,弱键的键能很小,很容易断裂。键能也表示键的距离。较高的键能意味着键距较低(因此,键强度较高)。此外,当键能较低时,键间距较大。如导言所述,电负性在键的形成中起作用。因此,原子的电负性也对键能有贡献。
什么是键离解能(bond dissociation energy)?
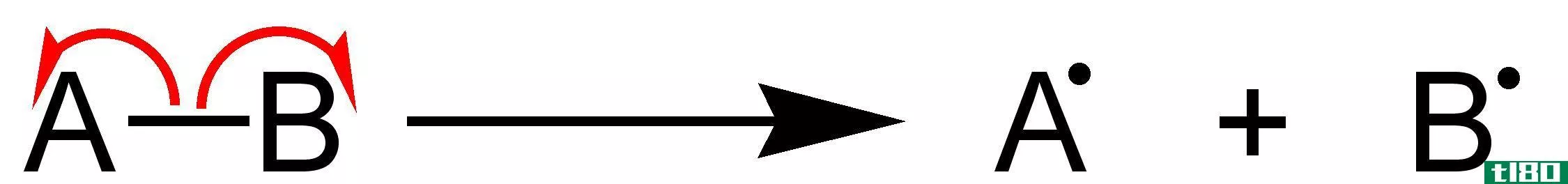
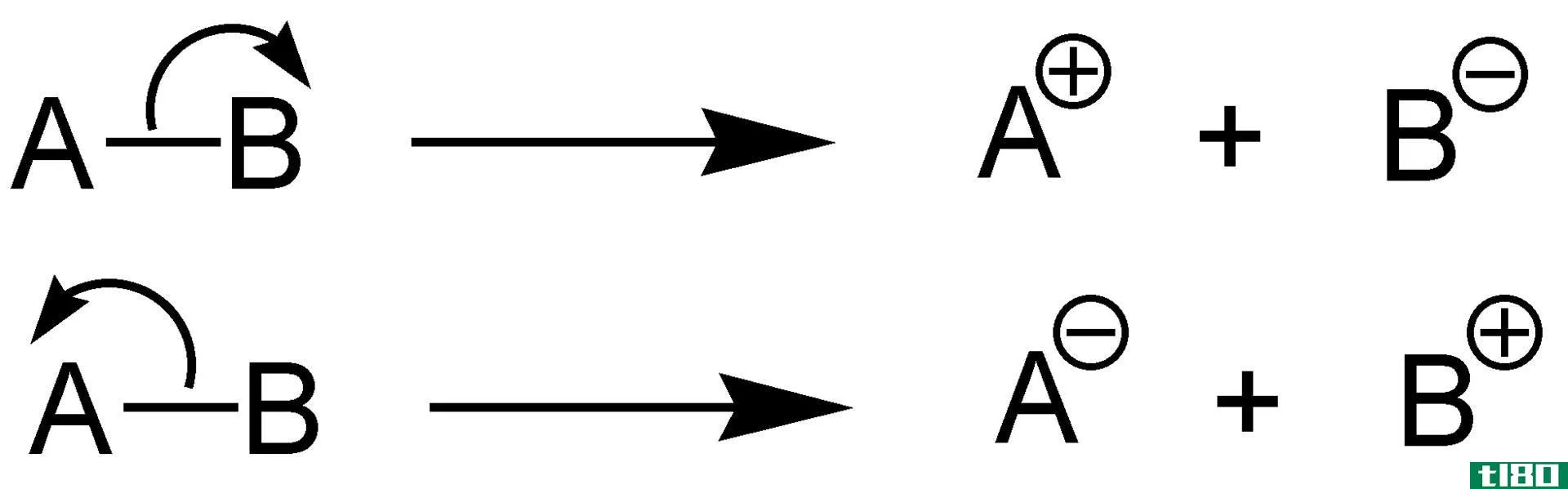
键离解能也是衡量键强度的指标。我们可以把它定义为,当一个键通过均裂而发生的焓变。键离解能是单键特有的。
在这种情况下,同一个键可以有不同的键离解能,这取决于情况。例如,甲烷分子中有四个C-H键,而所有C-H键的键离解能并不相同。

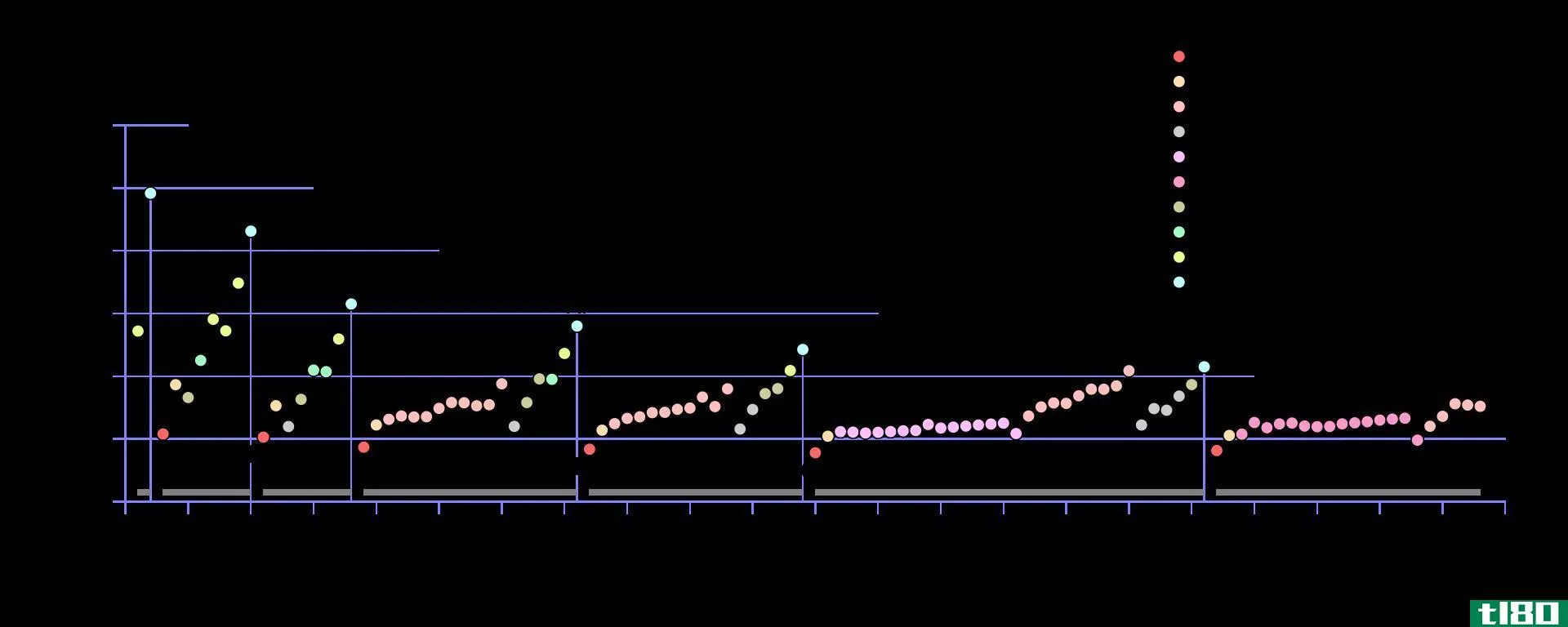
图02:配位络合物的一些键离解能
因此,在甲烷分子中,C-H键的键离解能分别为439 kJ/mol、460 kJ/mol、423 kJ/mol和339 kJ/mol,这是因为第一个键断裂通过均裂形成自由基物种,因此第二个键断裂发生在自由基物种上,比第一个需要更多的能量。同样,键离解能也会一步一步地改变。
键能(bond energy)和键离解能(bond dissociation energy)的区别
键能是同一化学物种中同一类型的所有键的气相键离解能(通常在298 K的温度下)的平均值。然而,键能和键离解能是不同的。键离解能是共价键被均裂而产生碎片时的标准焓变化;碎片通常是自由基物种。因此,键能和键离解能的关键区别在于键能是一个平均值,而键离解能是一个特定键的特定值。
例如,在甲烷分子中,C-H键的键离解能分别为439kj/mol、460kj/mol、423kj/mol和339kj/mol,而甲烷的C-H键能为414kj/mol,是四个值的平均值。此外,对于一个分子,键离解能不一定等于键能(如上面给出的甲烷例子)。对于双原子分子,键能和键离解能是相同的。
下面的信息图显示了键能和键离解能之间的区别。
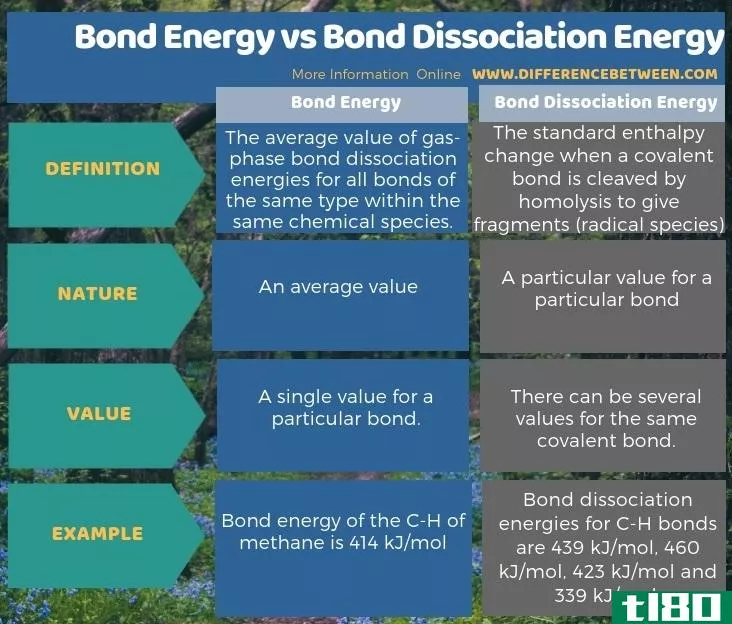
总结 - 键能(bond energy) vs. 键离解能(bond dissociation energy)
键离解能与键能不同。键能是分子所有键离解能的平均值。因此,键能和键离解能的关键区别在于键能是一个平均值,而键离解能是一个特定键的特定值。
引用
1“键离解能量”,维基百科,维基媒体基金会,2019年1月5日。可在此处查阅。歌词。“键能”,化学剧本,国家科学基金会,2018年11月26日。此处提供
2歌词。“键能”,化学剧本,国家科学基金会,2018年11月26日。