离解和溶剂化的关键区别在于,离解是一种物质分解成构成该物质的原子或离子,而溶剂化是由于溶剂分子和物质组分之间的引力而在溶剂中溶解的过程。
离解和溶剂化经常出现在分析化学和无机化学中,即在一种物质中原子和离子之间的不同相互作用下化学物质的分解。
目录
1. 概述和主要区别
2. 什么是分离
3. 什么是溶剂化
4. 并列比较-解离与溶剂化的表格形式
5. 摘要
什么是离解(dissociation)?
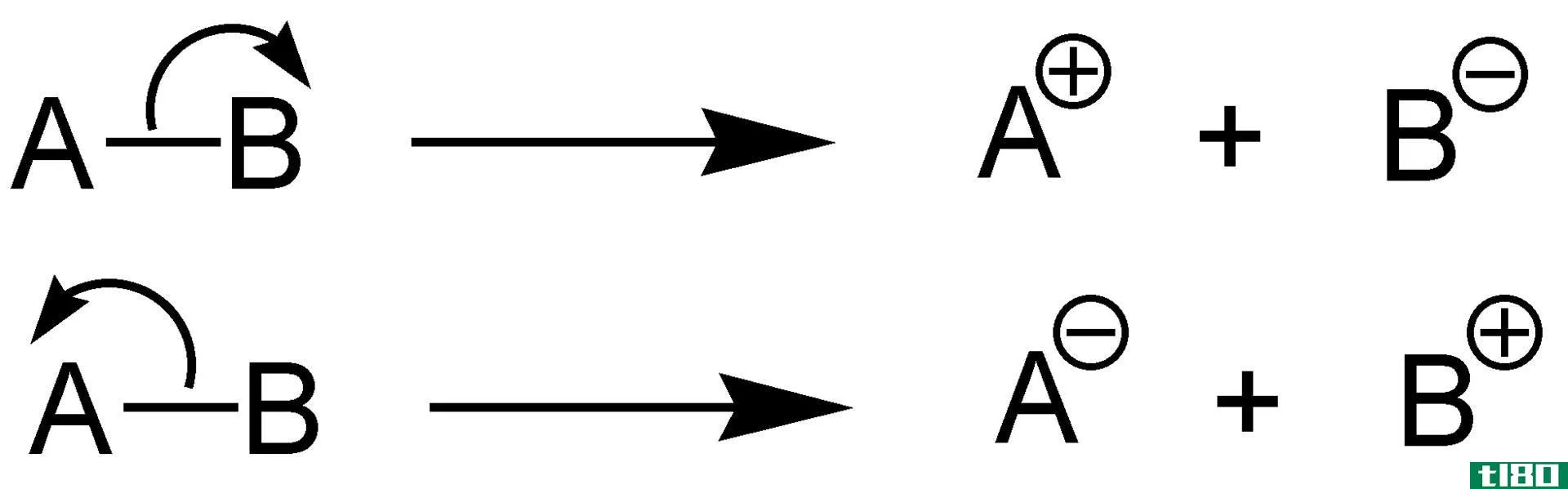
离解是指化合物分解或分裂成更小的粒子。解离过程形成带电或中性的产物。也就是说,离解产物可以是离子的,也可以是非离子的。然而,这并不涉及原子获得或失去电子。
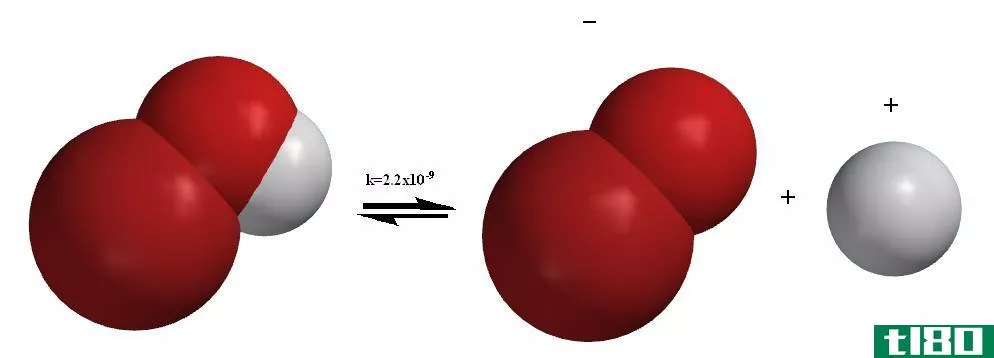
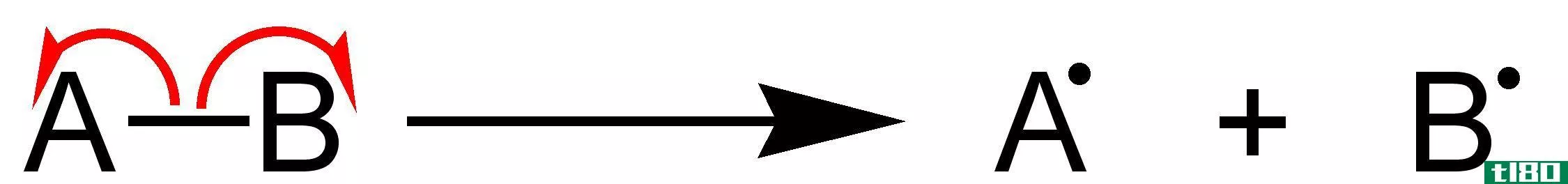
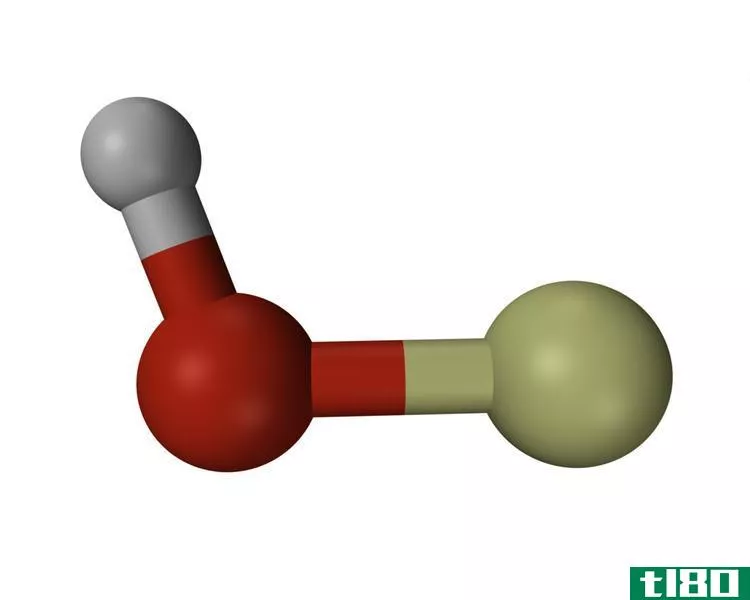
图01:BrOH分子的解离
与电离过程不同,离解是指化合物中已经存在的离子的分离。有时,离解也会产生中性粒子,例如,N2O4的分解会产生两个NO2分子。解离过程在大多数情况下是可逆的。这就是说,分离的离子可以重新排列以产生前一种化合物。例如,如上所述,氯化钠的溶解是一个离解过程,它产生两个带电粒子。但是,在一定的条件下,可以再次得到固体NaCl,证明了解离是可逆的。与电离不同,离解发生在离子化合物中。
什么是溶剂化(solvation)?
溶剂化是物质在特定溶剂中的溶解。溶剂化是由于溶剂分子和溶质分子之间的吸引力而发生的。通常,在这个过程中所涉及的吸引力是离子偶极键和氢键吸引力。这些吸引力导致溶质在溶剂中溶解。
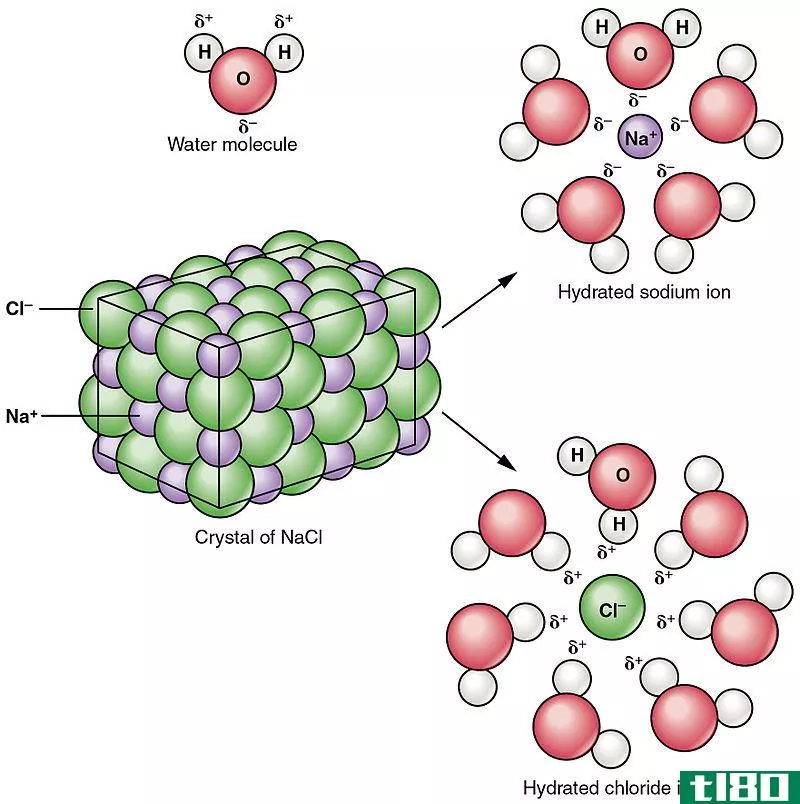
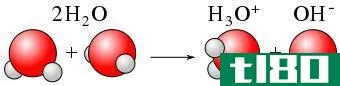
图02:氯化钠离子化合物在水中的溶剂化
离子化合物与极性溶剂之间存在离子-偶极相互作用。E、 水是极性溶剂。当氯化钠加入水中时,极性水分子分别吸引钠离子和氯离子,导致钠离子和氯离子分开。这导致氯化钠离子化合物分解。
离解(dissociation)和溶剂化(solvation)的区别
离解和溶剂化是描述不同物质如何根据相互作用分解成小块或原子/离子的术语。离解和溶剂化的关键区别在于,离解是一种物质分解成构成该物质的原子或离子,而溶剂化是由于溶剂分子和物质组分之间的引力而在溶剂中溶解的过程。
下表显示了离解和溶剂化之间的更多差异。
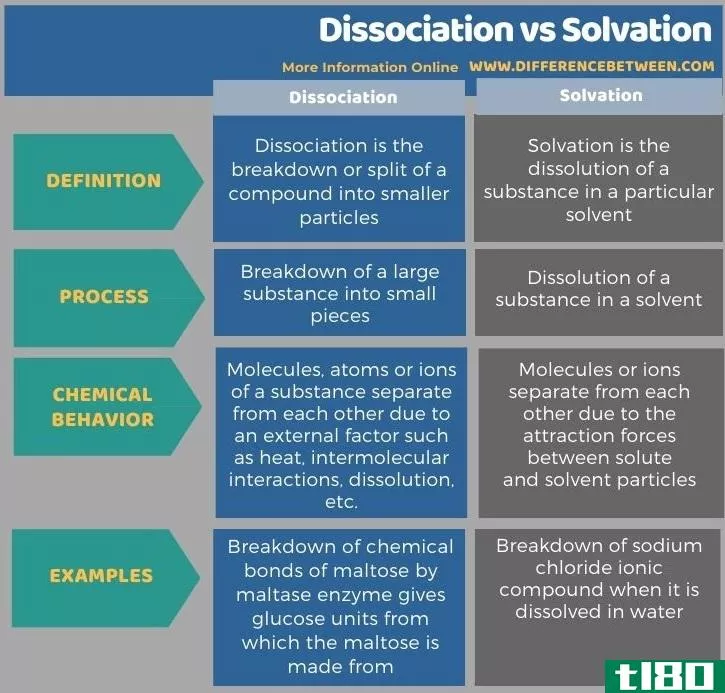
总结 - 离解(dissociation) vs. 溶剂化(solvation)
离解和溶剂化的关键区别在于,离解是一种物质分解成构成该物质的原子或离子,而溶剂化是由于溶剂分子和物质组分之间的引力而在溶剂中溶解的过程。
引用
1“溶液、溶剂化和解离”,化学剧本,剧本,2019年6月5日,
2“溶剂化和解离。”苏格拉底网,