氧化数(oxidation number)和氧化态(oxidation state)的区别
主差氧化数(main difference oxidation number) vs. 氧化态(oxidation state)
氧化次数和氧化状态通常被认为是相同的。这是因为氧化状态可以等于特定原子的氧化数,根据它所处的化合物类型。但是,氧化次数与氧化状态之间存在着细微的差异。氧化数与氧化态的主要区别是,如果周围的键都是离子键,氧化数是配位配合物中心原子的电荷,而氧化态则是特定原子可能丢失、增益或与另一个原子共享的电子数。
覆盖的关键领域
1.什么是氧化数-定义,规则,示例2.什么是氧化状态-定义,规则,示例3.氧化数和氧化状态之间的区别-主要区别的比较
Key Terms: Arabic Numbers, Bidentate, Coordination Bonds, Coordination Complex, Coordination Number, Ionic Bonds, Ligands, Monodentate, Oxidation Number, Oxidation State, Roman Numbers
什么是氧化数(oxidation number)?
如果配位络合物周围的所有键都是离子键,则氧化数可以定义为配位络合物中心原子的电荷。配位络合物是由一个中心金属原子与几个配体结合而成的化学结构。由于中心金属原子的存在,这些化合物也被称为金属络合物。这个中心金属原子叫做配位中心。配体是通过配位键(配位共价键)与金属原子相连的化学基团。一种配位化合物含有几种配位络合物。
大多数情况下,中心金属原子是过渡金属(d-块元素)。当富电子物种将其电子对(一对或两对)贡献给中心原子时,形成配位键。这些供体被称为配体。配体可以是中性分子,也可以是带负电荷的离子。这种配位键是共价键,因为它是由于两个原子之间的电子共享而形成的。与中心原子结合的施主原子数称为配位数。
可以有单齿或双齿配体。单齿配体通过一个配位键与中心原子结合,而双齿配体通过两个配位键与中心原子结合。配位数决定了配位复合体的几何形状。然而,配位数不是中心原子的氧化数。但有时,配位数可能等于氧化数。

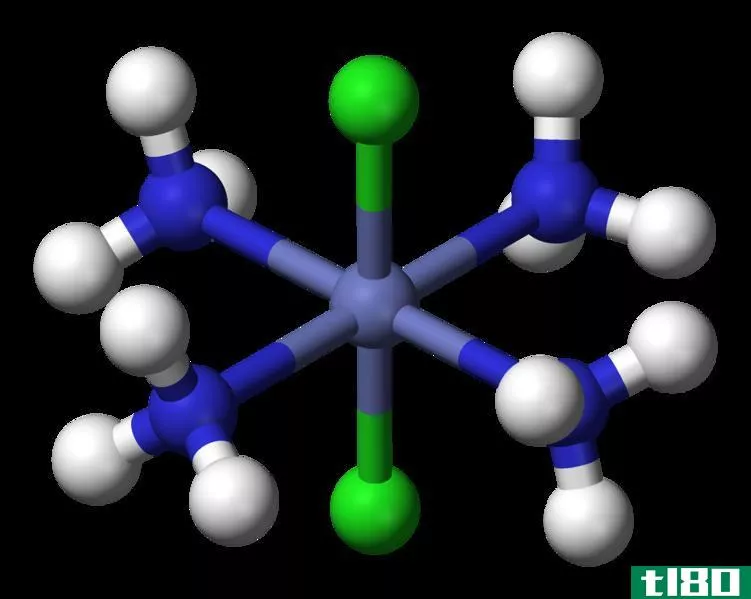
Figure 01: A coordination complex of cobalt
上图显示了[Co(NH3)6]Cl3络合物。钴的配位数是6,因为有6个氨配体与钴原子结合。但是钴的氧化数是3,因为如果除去配位络合物周围的所有配体,氧化数就是配位络合物中心原子的电荷。由于三个氯原子产生-3电荷,而氨分子是带中性电荷的,所以钴原子应该带+3电荷,以便中和来自氯原子的电荷。因此,钴的氧化数写为Co(III)。
什么是氧化态(oxidation state)?
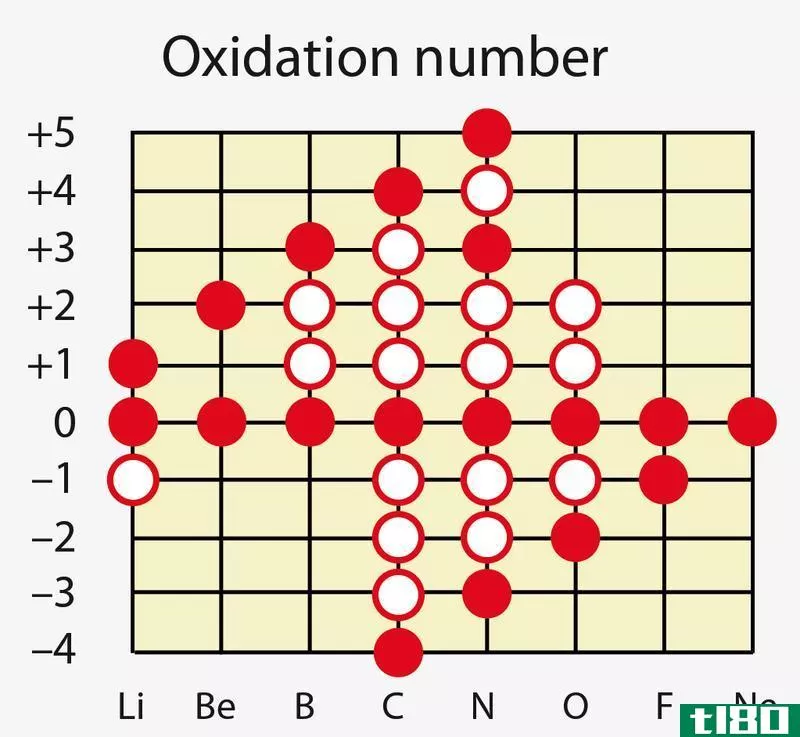
氧化态可以定义为一个特定原子可以失去、获得或与另一个原子共享的电子数。这个术语不仅限于配位络合物。氧化态实际上给出了化合物中原子的氧化程度。氧化态总是以整数形式给出,用印度教阿拉伯数字表示,包括原子的电荷。
确定氧化状态的规则
原子的氧化态是根据七条规则给出的。
规则1
单个元素和由单个元素组成的化合物每个原子的氧化态为零。
例如,化合物N2中氮(N)的氧化状态为零。
规则2
化合物的总电荷是每个元素电荷的总和。
例如,在中性物质如NaCl中,总电荷为零。因此,每种元素的氧化状态应分别表示为Na(+1)和Cl(-1)。
在离子物种中,如NH4+,N和H原子的氧化态之和应等于总电荷。
(N+4H)=(-3)+(1 x 4)=+1
规则3
第1组金属(1A)的氧化状态始终为+1,第2组金属(2A)的氧化状态始终为+2。
例如,锂(Li)的氧化状态总是+1,镁(Mg)的氧化状态总是+2。
规则4
氟(F)的氧化态总是-1。
记住,根据第一条规则,氟在F2中的氧化状态为零。
规则5
与其他原子相比,电负性最强的原子被赋予负电荷。
例如,氟的电负性比氢强。因此,在HF中,氢的氧化态是-1,但通常氢的氧化态是+1。
规则6
氢的氧态(H)通常为+1。
氢原子很容易失去一个电子,形成它的阳离子。但当氢与1A族或2A族金属结合时,氢的氧化态为-1,例如NaH。
规则7
氧的氧化状态通常为-2。
氧的电负性更强,能吸引电子。因此,很容易形成-2氧化态。但是在过氧化物中,氧化数是-1,因为两个氧原子在那里以单键结合。
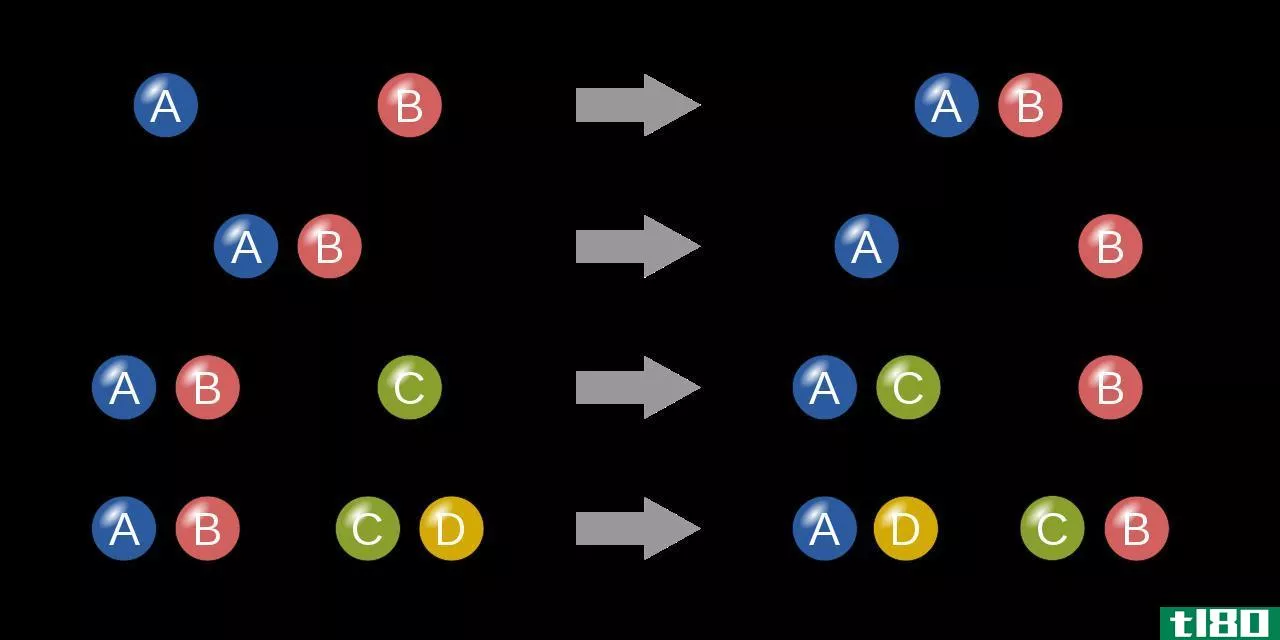
氧化态对氧化还原反应产物的测定非常有用。氧化还原反应是包括原子间电子交换的化学反应。在氧化还原反应中,两个半反应平行发生。一个是氧化反应,另一个是还原反应。氧化反应涉及原子氧化态的增加,而还原反应涉及原子氧化态的减少。

Figure 02: Redox Reaction between Mg and H2
在上述反应中,Mg是具有零(0)氧化状态的单一元素。但与H2反应后生成MgCl2,Mg的氧化态为+2,此时Mg的氧化态增加。因此,这是氧化还原反应中的氧化半反应。H在HCl中的氧化态为+1,而产物H2处于零(0)氧化态。氧化态降低。因此,它是这个氧化还原反应中的还原半反应。
氧化数(oxidation number)和氧化态(oxidation state)的区别
定义
氧化数:如果配位络合物周围的所有键都是离子键,则氧化数可以定义为配位络合物中心原子的电荷。
氧化态:氧化态可以定义为一个特定原子可以失去、获得或与另一个原子共享的电子数。
应用
氧化数:配合物采用氧化数。
氧化态:氧化态可用于任何元素或化合物。
数的表示
氧化数:用罗马数字表示氧化数。
氧化状态:印度教阿拉伯数字用来表示氧化状态。
指控的陈述
氧化数:氧化数没有给出中心原子电荷的细节。
氧化状态:氧化状态用带负(-)或正(+)符号的电荷表示。
结论
对于正常元素或化合物(而不是配合物),氧化状态和氧化数是相同的。但考虑到所有化合物,包括配位化合物,则略有不同。氧化数和氧化态之间的主要区别在于,如果配位络合物周围的所有键都是离子键,则氧化数是配位络合物中心原子的电荷,而氧化态是特定原子可以失去、获得或与另一个原子共享的电子数。
引用
1.“氧化状态(氧化数)”。氧化状态(氧化数)N.p.,N.d.网络。这里有。2017年7月5日。 2.“元素氧化数分配规则。”假人。N.p.,N.d.网站。这里有。2017年7月5日。3.“配合物。”配合物帮助页。N.p.,N.d.网站。这里有。 2017年7月5日。 2.“元素氧化数分配规则。”假人。N.p.,N.d.网站。 3.“配合物。”配合物帮助页。N.p.,N.d.网站。
- 发表于 2021-06-28 20:14
- 阅读 ( 587 )
- 分类:科学
你可能感兴趣的文章
锌(zinc)和氧化锌(zinc oxide)的区别
锌和氧化锌的主要区别在于锌是一种化学元素,而氧化锌是一种化合物。 锌是元素周期表d区的一种金属化学元素。它形成许多化合物,如氧化物、硫化物等。氧化锌是一种含有锌和氧原子的化合物。它以白色固体存在。下面...
- 发布于 2020-09-15 21:05
- 阅读 ( 924 )
离子电子法(ion electron method)和氧化数法(oxidation number method)的区别
离子电子法和氧化数法的关键区别在于,在离子电子法中,反应是根据离子的电荷来平衡的,而在氧化数法中,反应是根据氧化剂和还原剂的氧化数的变化来平衡的。 离子电子法和氧化数法是平衡化学方程式的重要方法。对...
- 发布于 2020-09-27 07:28
- 阅读 ( 991 )
氧化加成(oxidative addition)和还原消去(reductive elimination)的区别
氧化加成和还原消除的关键区别在于,氧化加成是指将两个阴离子配体加入到金属络合物中,而还原消除是指从金属络合物中除去两个阴离子配体。 氧化加成和还原消除是相互对立的化学反应。这两个过程与含有过渡金属及...
- 发布于 2020-10-03 08:21
- 阅读 ( 676 )
正式指控(formal charge)和氧化态(oxidation state)的区别
形式电荷和氧化态的关键区别在于,形式电荷是分子中一个原子的电荷,我们假设化学键中的电子在原子之间平均分配,而氧化态是一个原子失去或获得或与另一个原子共享的电子数。 形式电荷和氧化态是不同的,尽管我们...
- 发布于 2020-10-14 15:36
- 阅读 ( 1103 )
价(valency)和氧化值(oxidation number)的区别
价态和氧化数之间的关键区别在于,价态是一个原子为稳定所能失去、获得或共享的最大电子数,而氧化数是一个原子为了与另一个原子形成键而可以失去或获得的电子数。 氧化数和价电子与原子的价电子有关。价电子是占...
- 发布于 2020-10-15 12:44
- 阅读 ( 300 )
氧化值(oxidation number)和指控(charge)的区别
氧化数和电荷之间的关键区别在于,我们可以根据原子除去或获得的电子数来确定原子的氧化数,而电荷是根据原子中电子和质子的总数来确定的。 元素周期表中的不同元素表现出不同的化学和物理特性。当它们结合形成分...
- 发布于 2020-10-15 23:21
- 阅读 ( 376 )
协调数(coordination number)和氧化值(oxidation number)的区别
配位数和氧化数的关键区别在于,配位数是附着在配位化合物金属中心的配位体的数目,而氧化数则是中心原子的电荷,如果我们去掉它周围的所有配体和电子对。 在配位化学中,我们遇到了配位数和氧化数这两个术语。在...
- 发布于 2020-10-16 19:45
- 阅读 ( 820 )
氧化亚铜(cuprous oxide)和氧化铜(cupric oxide)的区别
氧化亚铜和氧化亚铜之间的关键区别在于氧化亚铜的颜色为深红色,而氧化亚铜的颜色为黑色。 氧化亚铜和氧化铜都是化学元素铜的化合物。这些氧化物含有铜的不同氧化状态。此外,在氧化亚铜中,有一个+1氧化状态,在...
- 发布于 2020-10-17 04:38
- 阅读 ( 1062 )
金属(metal)和非金属氧化物(nonmetal oxides)的区别
金属氧化物和非金属氧化物的主要区别在于金属氧化物是碱性化合物,而非金属氧化物是酸性化合物。 “氧化物”是一大类化合物,其化学元素基本上与氧原子结合。然而,惰性气体由于其惰性和较高的稳定性而不形成这些...
- 发布于 2020-10-18 07:21
- 阅读 ( 547 )
氧化数法(oxidation number method)和半反应法(half reaction method)的区别
关键区别-氧化数法与半反应法 氧化数法和半反应法是平衡氧化还原反应化学方程式的两种方法。氧化还原反应是由两个平行的化学反应组成的化学反应:氧化反应和还原反应。这些被称为氧化还原反应的半反应。因此,氧化...
- 发布于 2020-10-19 09:49
- 阅读 ( 836 )