价性和共价性的关键区别在于,价态是一个原子在形成离子时获得或损失的电子数,而共价性是一个原子可以与另一个原子共享的电子数。
尽管电价和共价这两个术语听起来很相似,但根据它们的定义,它们是不同的。主要是,电价解释了离子的形成,而共价则解释了共价键的形成。
目录
1. 概述和主要区别
2. 什么是电价
3. 什么是共价性
4. 并列比较-以表格形式表示的电价与共价性
5. 摘要
什么是电价(electrovalency)?
价态是在原子形成离子的过程中获得或丢失的电子数。因此,它是指一个原子在形成一个电子价键时获得或损失的电子数,我们称之为离子键。根据这个解释,它给出了离子的净电荷。此外,如果一个原子在形成离子键时失去了电子,则表明该原子具有正的电价;如果原子在形成离子键时获得了电子,则表明该原子具有负的电价。有价原子的化合物是离子化合物。
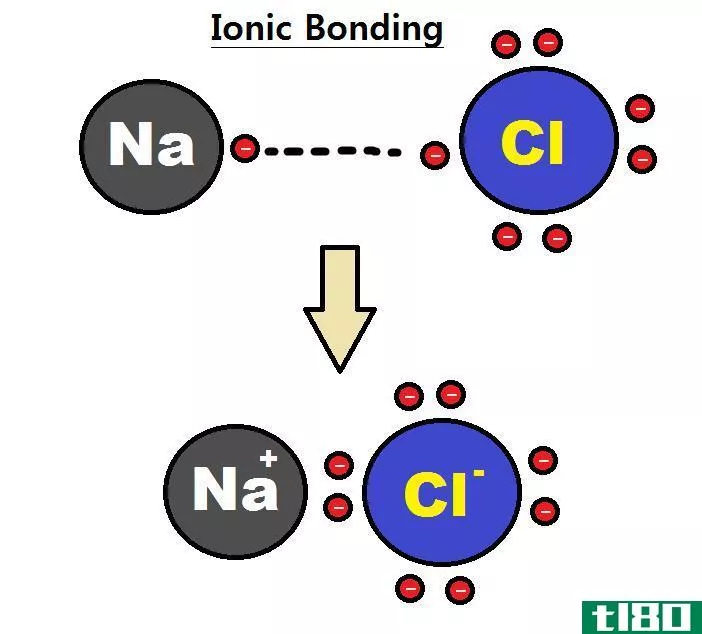
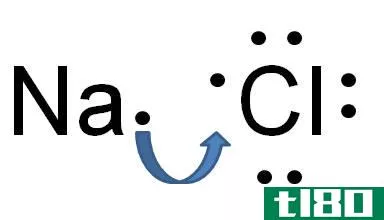
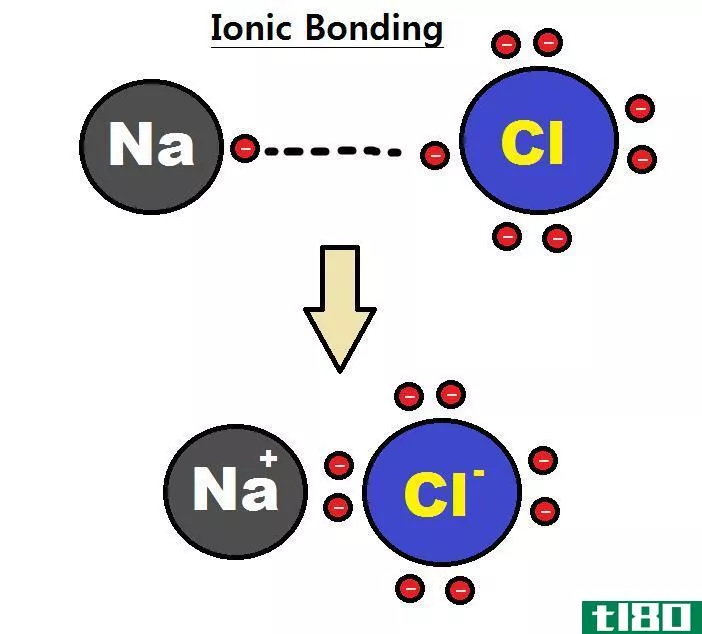
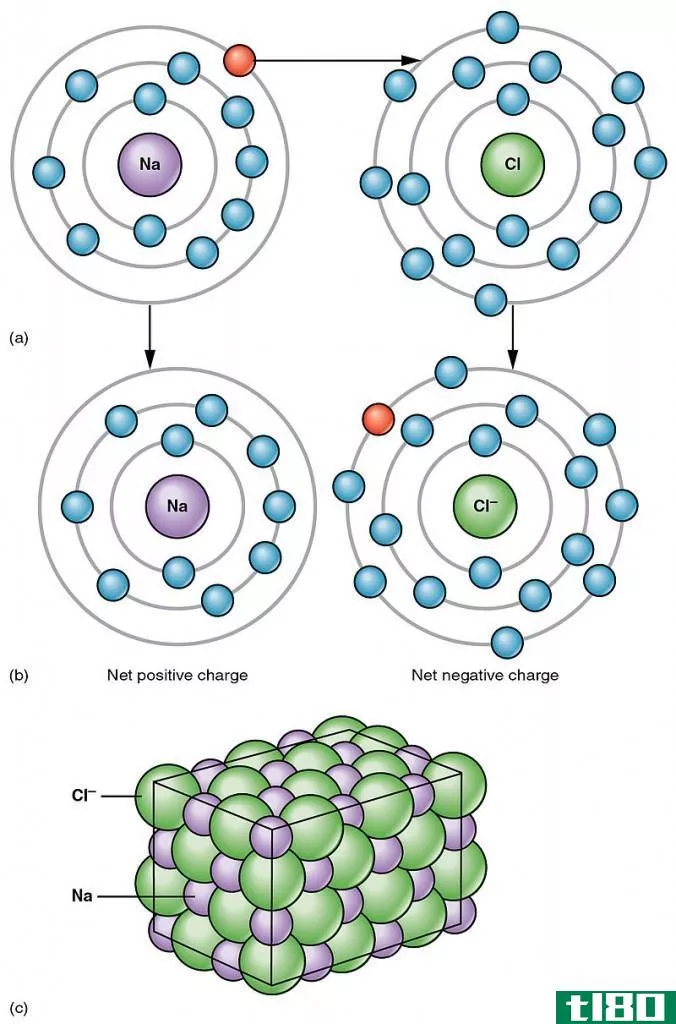
图01:离子键的形成
例如,让我们考虑氯化钠(NaCl)的形成。在那里,钠原子失去一个电子,因此它有一个正的电价。氯原子得到那个电子。因此,它有一个负的电价。但是,钠的电子数,要么是电子价,要么是失去的。我们应该用适当的符号给出电价,以表明它是正电价还是负电价。
- 钠=正价态钠可以取+1。
- 氯=氯的负电价可以表示为-1。
什么是共价性(covalency)?
共价是它能与另一个原子共享的最大电子数。因此,它指示原子可以利用其空轨道形成的共价键的最大数目。这个参数的值取决于原子的价电子数和原子中存在的空轨道的数目。
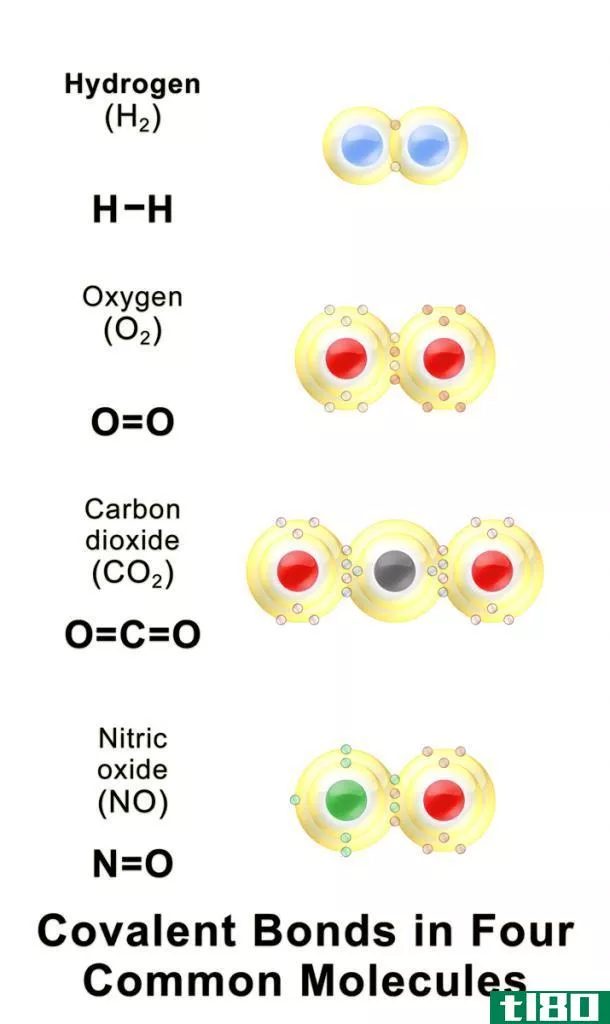
例如,氢原子只有一个电子;因此,它可以与另一个原子共用一个电子。因此,氢的共价性为1。与电价不同,我们不需要加号或减号,因为没有电子的损失或增加;只有电子是彼此共享的。

图02:共价键的形成
如前所述,在决定共价性时,不仅价电子的数目,而且原子的空轨道数也很重要。例如,如果我们以碳为例,它在最外层的电子壳层中有4个电子。在那里,它有2s22p2电子组态。因此,有一个空的2p轨道。因此,2s轨道上的两个成对电子可以分离,一个电子被包含在空的2p轨道中。然后有4个不成对的电子。碳可以与另一个原子共用四个电子。因此,的共价性变为4。这是因为当我们写下碳的电子构型时,我们看到只有2个不成对的电子,所以我们认为碳的共价性是2,而实际上它是4。
电价(electrovalency)和共价性(covalency)的区别
价态是在原子形成离子的过程中获得或丢失的电子数。它解释了离子键的形成。此外,具有此参数的原子的化合物是离子型化合物。另一方面,共价性是它能与另一个原子共享的最大电子数。它解释了共价键的形成。此外,具有共价原子的化合物是共价化合物。
下面的信息图以表格形式展示了电价和共价性之间的差异。

总结 - 电价(electrovalency) vs. 共价性(covalency)
虽然电价和共价这两个术语听起来很相似,但它们有不同的定义和特点。电子价和共价的区别在于,电子价是一个原子在形成离子时获得或损失的电子数,而共价性是一个原子可以与另一个原子共享的电子数。
引用
1“2。键合的基本概念〉,PH在日常生活化学中的作用。这里有2个。化学共价性与分子结构〉,生物-神经系统反应时研究。此处提供
2化学共价性与分子结构〉,生物-神经系统反应时研究。