电子几何(electron geometry)和分子几何学(molecular geometry)的区别
电子几何的主要区别(main difference electron geometry) vs. 分子几何学(molecular geometry)
分子的几何形状决定了该分子的反应性、极性和生物活性。分子的几何结构可以用电子几何结构或分子几何结构来表示。VSEPR理论(价壳层电子对排斥理论)可以用来确定分子的几何结构。电子几何包括分子中存在的孤电子对。分子的几何结构可以由特定分子所具有的键的数目来决定。电子几何和分子几何的主要区别在于,电子几何是通过分子中的孤电子对和键来发现的,而分子几何是通过分子中的键来发现的。
覆盖的关键领域
1.什么是电子几何-定义,识别,示例2.什么是分子几何-定义,识别,示例3.什么是分子几何-解释图4.电子几何和分子几何之间的区别是什么-关键区别的比较
Key Terms: Electron Geometry, Lone Electron Pair, Molecular Geometry, VSEPR Theory
什么是电子几何(electron geometry)?
电子几何是通过考虑键电子对和孤电子对来预测分子的形状。VSEPR理论指出,位于某个原子周围的电子对相互排斥。这些电子对可以是键合电子,也可以是非键合电子。
电子几何给出了分子中所有键和孤对的空间排列。利用VSEPR理论可以得到电子的几何构型。
如何确定电子几何
以下是本次测定所采用的步骤。
- 预测分子的中心原子。它应该是最负电的原子。
- 确定中心原子中价电子的数量。
- 确定其他原子捐赠的电子数。
- 计算中心原子周围的电子总数。
- 把这个数除以2,这给出了电子基团的数目。
- 从上面得到的位数中扣除中心原子周围存在的单键数。这给出了分子中存在的孤电子对的数目。
- 确定电子几何。
示例
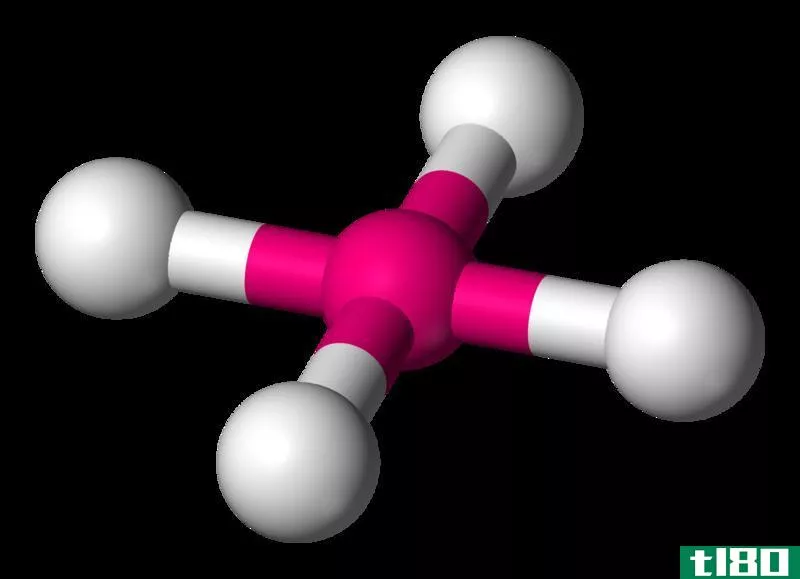
ch4的电子几何
分子中心原子=C
C=4的价电子数
氢原子提供的电子数=4 x(H)=4 x 1=4
C=4+4=8周围的电子总数
电子基团数=8/2=4
单键数=4
孤电子对数=4–4=0
因此,电子几何=四面体

Figure 1: Electron Geometry of CH4
氨(nh3)的电子几何
分子的中心原子=N
N=5价电子数
氢原子提供的电子数=3 x(H)=3 x 1=3
N=5+3=8周围的电子总数
电子基团数=8/2=4
单键数=3
孤电子对数=4–3=1
因此,电子几何=四面体

Figure 2: Electron Geometry of Ammonia
alcl3的电子几何
分子的中心原子=铝
Al的价电子数=3
Cl原子提供的电子数=3 x(Cl)=3 x 1=3
N=3+3=6周围的电子总数
电子基团数=6/2=3
单键数=3
孤电子对数=3–3=0
因此,电子几何=三角平面

Figure 3: Electron Geometry of AlCl3
有时,电子几何和分子几何是相同的。这是因为在没有孤电子对的情况下,在确定几何结构时只考虑成键电子。
什么是分子几何学(molecular geometry)?
分子几何是通过只考虑键电子对来预测分子的形状。在这种情况下,不考虑孤电子对。此外,双键和三键被认为是单键。这种几何结构是基于孤电子对比键电子对需要更多的空间这一事实来确定的。例如,如果一个分子由两对成键电子和一对孤电子组成,那么分子的几何结构就不是线性的。那里的几何结构是“弯曲的或有角度的”,因为孤立的电子对比两个成键的电子对需要更多的空间。
分子几何学的例子
h2o的分子几何
分子的中心原子=O
O的价电子数=6
氢原子捐赠的电子数=2 x(H)=2 x 1=2
N=6+2=8周围的电子总数
电子基团数=8/2=4
孤电子对数=2
单键数=4–2=2
因此,电子几何=弯曲

Figure 4: Molecular geometry of H2O
氨(nh3)的分子几何
分子的中心原子=N
N=5的价电子数
氢原子提供的电子数=3 x(H)=3 x 1=3
N=5+3=8周围的电子总数
电子基团数=8/2=4
孤电子对数=1
单键数=4–1=3
因此,电子几何=三角金字塔

Figure 5: Ball and stick structure for ammonia molecule
氨的电子几何形状是四面体。但是氨的分子几何是三角金字塔。
分子几何
下表显示了分子的一些几何结构,这些几何结构是根据所存在的电子对的数目而定的。
| 电子对数 | 键合电子对数 | 孤电子对数 | 电子几何 | 分子几何学 |
| 2 | 2 | 0 | 线性的 | 线性的 |
| 三 | 三 | 0 | 平面三角形 | 平面三角形 |
| 三 | 2 | 1 | 平面三角形 | 弯曲的 |
| 4 | 4 | 0 | 四面体 | 四面体 |
| 4 | 三 | 1 | 四面体 | 三角金字塔 |
| 4 | 2 | 2 | 四面体 | 弯曲的 |
| 5 | 5 | 0 | 三角锥 | 三角锥 |
| 5 | 4 | 1 | 三角锥 | 跷跷板 |
| 5 | 三 | 2 | 三角锥 | T形 |
| 5 | 2 | 三 | 三角锥 | 线性的 |
| 6 | 6 | 0 | 八面体 | 八面体 |

Figure 6: Basic Geometries of Molecules
上表显示了分子的基本几何结构。几何图形的第一列显示了电子几何图形。其他列显示分子几何结构,包括第一列。
电子几何(electron geometry)和分子几何学(molecular geometry)的区别
定义
电子几何:电子几何是考虑键电子对和单电子对的分子的形状。
分子几何学:分子几何学是通过只考虑键电子对来预测分子的形状。
孤电子对
电子几何:寻找电子几何时考虑孤电子对。
分子几何:寻找分子几何时不考虑孤电子对。
电子对数
电子几何:总的电子对的数目应该被计算出来以找到电子几何。
分子几何学:为了找到分子几何学,应该计算成键电子对的数目。
结论
当中心原子上没有孤电子对时,电子几何和分子几何是相同的。但如果中心原子上有孤电子对,则电子的几何结构总是不同于分子的几何结构。因此,电子几何和分子几何的区别取决于分子中存在的孤电子对。
引用
1.“分子几何学”。N.p.,N.d.网站。这里有。2017年7月27日。2.“VSEPR理论”,维基百科。维基媒体基金会,2017年7月24日。这里有。 2017年7月27日。 2.“VSEPR理论”,维基百科。维基媒体基金会,2017年7月24日。
- 发表于 2021-06-29 09:25
- 阅读 ( 345 )
- 分类:科学
你可能感兴趣的文章
正方形平面(square planar)和四面体配合物(tetrahedral complexes)的区别
...e electron configuration ending d8 form coordination complexes having this molecular geometry. For example, Rh(I), Ir(I), Pd(II), etc. The coordination number for a square planar complex is four. 我们可以用晶体场理论来描述这些配合物的结构。根据这个理论,一个正方形...
- 发布于 2020-10-15 00:12
- 阅读 ( 557 )
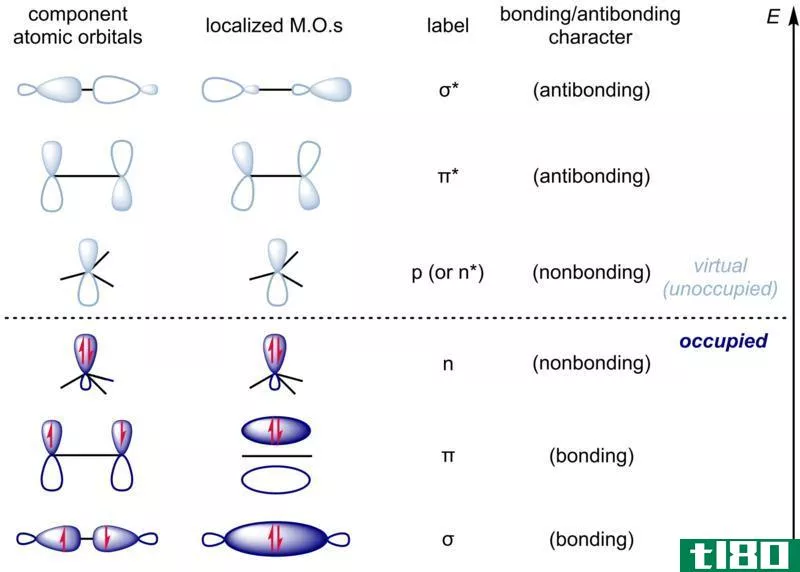
分子轨道理论(molecular orbital theory)和杂交理论(hybridization theory)的区别
...-分子轨道理论与杂交理论 5. 摘要 什么是分子轨道理论(molecular orbital theory)? 分子轨道理论是用量子力学描述分子电子结构的技术。这是解释分子中化学键的最有效的方法。让我们详细讨论一下这个理论。 首先,我们需要知道...
- 发布于 2020-10-15 22:50
- 阅读 ( 842 )
反键合(antibonding)和非键合(nonbonding)的区别
...示为σ*。 什么是非键合(nonbonding)? Nonbonding orbital is the molecular orbital in which addition or removal of electr*** neither increases or decreases the bond order between atoms. We often designate this orbital by “n”. These orbitals resemble the lone electron pairs in Lewis struc...
- 发布于 2020-10-16 03:12
- 阅读 ( 1268 )
形状(shape)和分子几何学(geometry of a molecule)的区别
... 概述和主要区别 2. 分子的形状是什么 3. 什么是分子的几何学 4. 并列比较-表格形式的分子形状与几何结构 5. 摘要 什么是分子的形状(shape of a molecule)? 分子的形状是用中心原子上的键-电子对预测的分子结构。换句话说,除...
- 发布于 2020-11-02 15:58
- 阅读 ( 511 )
电子几何(electron geometry)和分子几何学(molecular geometry)的区别
...,了解分子化学的第一步是了解分子的几何结构。 分子几何学只是指构成分子的原子的三维排列。在某种意义上,“结构”一词只是用来表示原子的连接性。分子的形状是由结合在一起的原子核之间的距离决定的。分子的几何...
- 发布于 2021-06-25 21:13
- 阅读 ( 363 )
碳阳离子(carbocation)和碳负离子(carbanion)的区别
...。 负碳离子:负电荷的碳原子被sp3杂化在负碳离子中。 几何学 碳正离子:碳正离子中碳原子的几何形状是三角平面的。 碳负离子:碳负离子中碳原子的几何形状是金字塔形的。 磁性 碳阳离子:碳阳离子是顺磁性的。 碳负离...
- 发布于 2021-06-28 20:32
- 阅读 ( 537 )
vsepr公司(vsepr)和价键理论(valence bond theory)的区别
...。 价键理论:价键理论给出了分子中原子轨道的细节。 几何学 VSEPR:VSEPR理论给出了分子的几何结构。 价键理论:价键理论没有给出分子的几何结构。 化学键合 VSEPR:VSEPR理论没有指出原子间存在的键的类型。 价键理论:价键...
- 发布于 2021-06-29 09:45
- 阅读 ( 685 )
乙烯(ethene)和乙炔(ethyne)的区别
...108.7 pm。 乙炔:乙炔中C和H之间的距离约为106.0 pm。 分子几何学 乙烯:乙烯的几何形状是平面的。 乙炔:乙炔的几何形状是线性的。 pi债券数量 乙烯:乙烯中有一个π键。 乙炔:乙炔中有两个π键。 摩尔质量 乙烯:乙烯的摩尔...
- 发布于 2021-06-29 09:59
- 阅读 ( 342 )
硫黄(sulfur)和二氧化硫(sulfur dioxide)的区别
主要差异硫(main difference sulfur) vs. 二氧化硫(sulfur dioxide) 硫是一种非金属,以不同的分子形式存在,称为同素异形体。它以亮黄色固体存在于地壳中。硫不能作为纯元素存在于大气中;它是硫的氧化物。大气中主要的氧化...
- 发布于 2021-06-29 10:12
- 阅读 ( 463 )
价键理论(valence bond theory)和分子轨道理论(molecular orbital theory)的区别
...价键理论(main difference valence bond theory) vs. 分子轨道理论(molecular orbital theory) 原子由电子所在的轨道组成。这些原子轨道可以在不同的形状和不同的能级上找到。当一个原子与其他原子结合在分子中时,这些轨道以不同的方式排...
- 发布于 2021-06-29 10:32
- 阅读 ( 406 )