主要区别-电解质与非电解质的综合性能
综合性质是溶液的物理性质,它取决于溶质的数量,而不取决于溶质的性质。这意味着相同数量的完全不同的溶质可以以相似的数量改变这些物理性质。因此,综合性质取决于溶质量和溶剂量的比值。三种主要的综合特性是蒸汽压降低、沸点升高和冰点降低。对于给定的溶质-溶剂质量比,所有的综合性质与溶质摩尔质量成反比。电解质是能够形成溶液的物质,能够通过这种溶液导电。这种溶液被称为电解溶液。非电解质是不能形成电解溶液的物质。这两种类型(电解质和非电解质)都具有结合性质。电解液和非电解液之间的主要区别在于电解液对电解液的综合性能的影响比非电解液高。
目录
1. 概述和主要区别
2. 电解液的综合性质是什么
3. 非电解质的结合性质是什么
4. 并列比较-电解液与非电解液在表格中的综合特性
5. 摘要
什么是电解质的综合性质(colligative properties of electrolytes)?
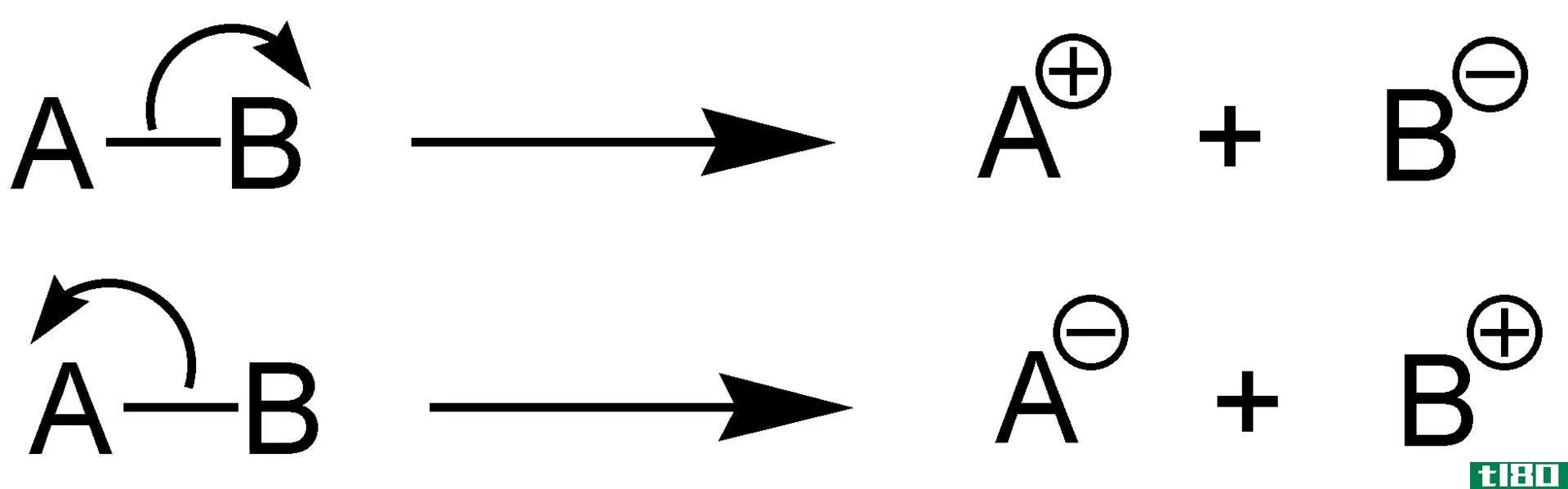
电解液的综合性质是指电解质溶液的物理性质,它取决于溶质的数量,而不考虑溶质的性质。在电解质溶液中,或获得电子,或在电解质溶液中失去电子。
当电解液溶解在像水这样的溶剂中时,电解液会分解成离子(或任何其他导电物质)。因此,溶解一摩尔电解液总是产生两个或更多摩尔的导电物质。因此,当电解液溶解在溶剂中时,电解液的结合性质会发生很大的变化。
例如,描述冰点和沸点变化的一般方程如下:,
ΔTb=Kbm和ΔTf=Kfm
ΔTb为沸点升高,ΔTf为冰点下降。Kb和Kf分别为沸点升高常数和冰点下降常数。m是溶液的摩尔浓度。对于电解溶液,上述方程式修改如下:,
ΔTb=iKbm和ΔTf=iKfm
“i”是一种称为范特霍夫因子的离子倍增器。这个系数等于电解质中离子的摩尔数。因此,范特霍夫因子可以通过计算电解液在溶剂中溶解时释放的离子数来确定。例如,NaCl的Van't Hoff因子值为2,在CaCl2中为3。
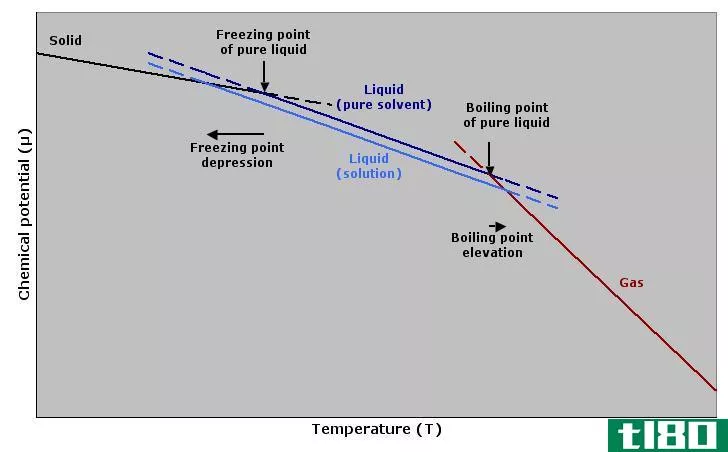
图01:显示化学势与温度的关系图,描述凝固点降低和沸点升高
然而,给出的这些综合性质的值与理论预测值不同。这是因为溶质和溶剂之间的相互作用可以减少离子对这些性质的影响。
对上述方程作了进一步的修正,以适用于弱电解质。弱电解质部分分解成离子,因此一些离子不影响碰撞性质。弱电解质的解离度(α)可计算如下:,
α={(i-1)/(n-1)}x 100
这里,n是弱电解质中每个分子形成的离子的最大数量。
什么是非电解质的碰撞性质(colligative properties of nonelectrolytes)?
非电解质的综合性质是非电解质溶液的物理性质,它取决于溶质的数量,而不考虑溶质的性质。非电解质是溶解在溶剂中时不会产生导电溶液的物质。例如,糖是一种非电解质,因为当糖溶解在水中时,它以分子形式存在(不会分解成离子)。这些糖分子不能在溶液中传导电流。
与电解溶液相比,非电解溶液中存在的溶质数量较少。因此,非电解质对碰撞性质的影响也很小。例如,与向类似溶液中添加糖相比,通过添加NaCl降低蒸汽压的程度更高。
电解质的综合性质(colligative properties of electrolytes)和非电解质(nonelectrolytes)的区别
| 电解质与目标电解液的综合性能 | |
| 电解液的综合性质是指电解质溶液的物理性质,它取决于溶质的数量,而不考虑溶质的性质。 | 非电解质的综合性质是非电解质溶液的物理性质,它取决于溶质的数量,而不考虑溶质的性质。 |
| 溶质 | |
| 电解质通过离解向溶液提供更多的溶质,因此,其结合性质发生了很大的变化。 | 由于没有离解作用,靶向电解液提供低溶质;因此,其结合性质没有明显变化。 |
| 对综合性质的影响 | |
| 与非电解质相比,电解液对碰撞性能的影响非常大。 | 与电解质相比,非电解质对碰撞性能的影响很小。 |
总结 - 电解质的综合性质(colligative properties of electrolytes) vs. 非电解质(nonelectrolytes)
综合性质是溶液的物理性质,不取决于溶质的性质,而是取决于溶质的数量。电解液和非电解液的结合性质的区别在于,电解液对电解液的综合性能的影响比非电解液高。
引用
1.“5.9:电解质溶液的综合性质。”化学图书馆,图书馆,2016年7月21日。此处提供2.“综合属性”,维基百科,维基媒体基金会,2018年3月10日。这里有3。大英百科全书的编辑。《电解液》,大英百科全书,大英百科全书,2017年6月7日。此处提供
2.“综合属性”,维基百科,维基媒体基金会,2018年3月10日。
3.大英百科全书的编辑。《电解液》,大英百科全书,大英百科全书,2017年6月7日。