电解质和非电解质的主要区别在于,电解质在水中溶解时能产生离子,而非电解质则不能产生离子。
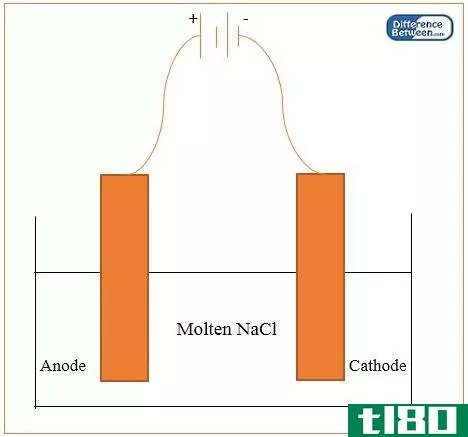
根据它们产生离子和导电的能力,我们可以把所有化合物分为电解质和非电解质两类。将电流通过电解溶液并迫使正负离子向各自的电极移动的过程称为“电解”。然而,非电解质不能参与电解过程。
目录
1. 概述和主要区别
2. 什么是电解质
3. 什么是非电解质
4. 并列比较-电解液和非电解液的表格形式
5. 摘要
什么是电解质(electrolytes)?
电解质是产生离子的物质。这些化合物在熔融阶段或溶解在溶剂(水)中时会产生离子。因为有离子,电解质可以导电。还有固态电解质。此外,一些气体如二氧化碳溶解在水中时会产生离子(氢和重碳酸盐离子)。
有两种类型的电解质:强电解质和弱电解质。强电解质在可溶时容易产生离子。例如,离子化合物是强电解质。熔融氯化钠或NaCl水溶液完全分解(形成Na+和Cl-离子),因此它们是良好的导电体。强酸和强碱也是很好的电解质。弱电解质溶于水时产生的离子很少。此外,弱酸如醋酸和弱碱是弱酸电解质。
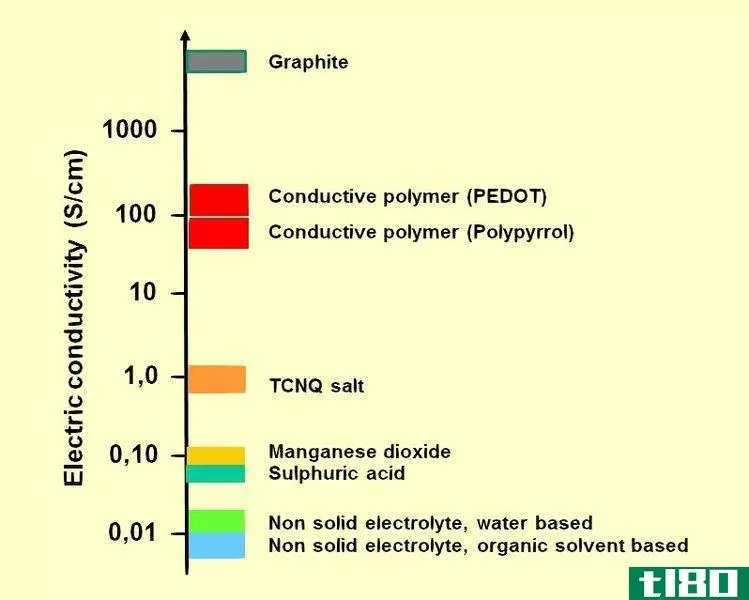
对比图01:一些电解质
体内电解质
电解质也存在于我们体内。我们需要它们来维持健康体内细胞和体液的平衡。电解质平衡是维持体内渗透平衡和血压的关键。Na+、K+、Ca2+在神经冲动传递和肌肉收缩中起重要作用。
体内的各种激素控制电解质的稳态。例如,醛固酮控制着钠离子的数量。降钙素和甲状旁腺激素在维持Ca2+和PO43-平衡中起作用。我们可以测量血液中的电解质水平,以确定某些电解质失衡。大多数情况下,血和尿中的Na+和K+水平对检查肾功能不全很重要。血液中的正常Na+水平为135–145 mmol/L,而正常K+水平为3.5–5.0 mmol/L。体内电解质水平过高可能是致命的。电解质在植物体内也很重要。例如,电解质(K+)通过保卫细胞控制气孔的开闭机制。
什么是非电解质(nonelectrolytes)?
当我们把它们溶解在溶剂中时,没有分裂成正离子和负离子的化合物是非电解质。这些化合物的熔融阶段也不会产生离子。介质中缺少离子使它们不导电。大多数具有非极性共价键的化合物/有机化合物都属于这一类。例如蔗糖、葡萄糖、乙烷等。
电解质(electrolytes)和非电解质(nonelectrolytes)的区别
电解质与非电解质的主要区别在于,电解质在水中溶解时能产生离子,而非电解质则不能产生离子。离子化合物和一些具有极性键的化合物可以是电解质。具有非极性键的化合物大多是非电解质。此外,溶液中的电解质可以与非电解质相反地导电。
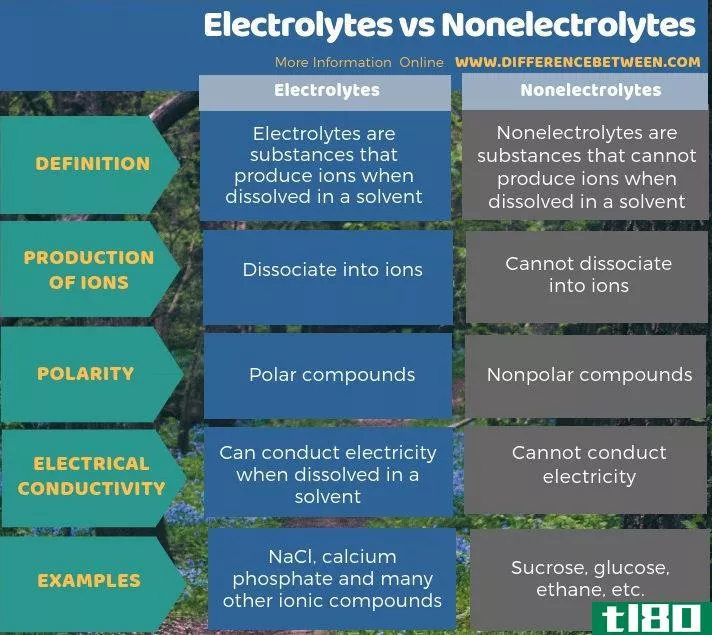
总结 - 电解质(electrolytes) vs. 非电解质(nonelectrolytes)
我们知道的所有化合物都是电解质或非电解质。电解质和非电解质的关键区别在于,电解质在水中溶解时能产生离子,而非电解质则不能产生离子。
引用
1赫尔曼斯汀,安妮·玛丽。“强电解质的定义和示例”,ThoughtCo,2019年7月3日,可在此处查阅。赫尔曼斯汀,安妮·玛丽。“化学示例:强电解质和弱电解质。”ThoughtCo,2019年8月6日,可在此处查阅。
2赫尔曼斯汀,安妮·玛丽。“化学示例:强弱电解质”,ThoughtCo,2019年8月6日,