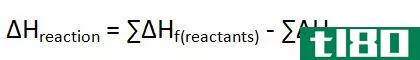主要区别
吸热反应和放热反应的主要区别在于吸热反应是一种从周围吸收热量的反应,而放热反应是将热量释放到周围的反应。
吸热反应(endothermic reacti***) vs. 放热反应(exothermic reacti***)
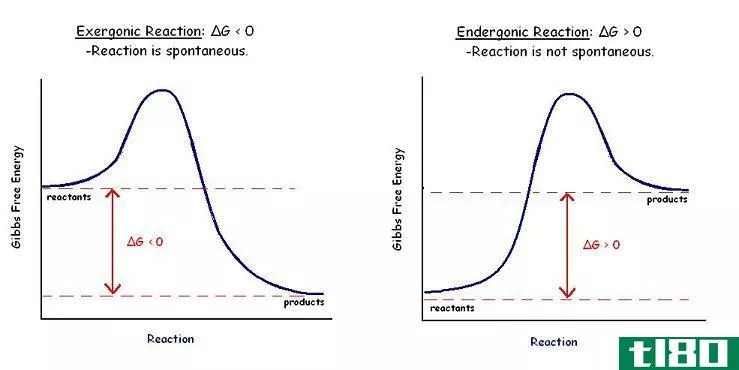
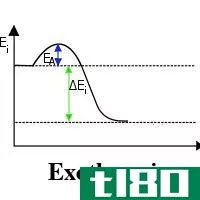
根据能量或热量,化学反应可分为吸热反应和放热反应两大类。吸热反应是指以热量形式从环境中吸收能量,而放热反应将能量释放到周围的反应。因此,在吸热反应的情况下,必须提供能量,但放热反应不需要能量。在吸热反应中,底物的能量比产物少,而在放热反应中,底物比产物具有更多的能量。在不同的反应过程中,能量的这种变化称为反应热,称为焓。用“ΔH”表示,单位为kJ/mol。
比较图
什么是吸热反应(endothermic reacti***)?
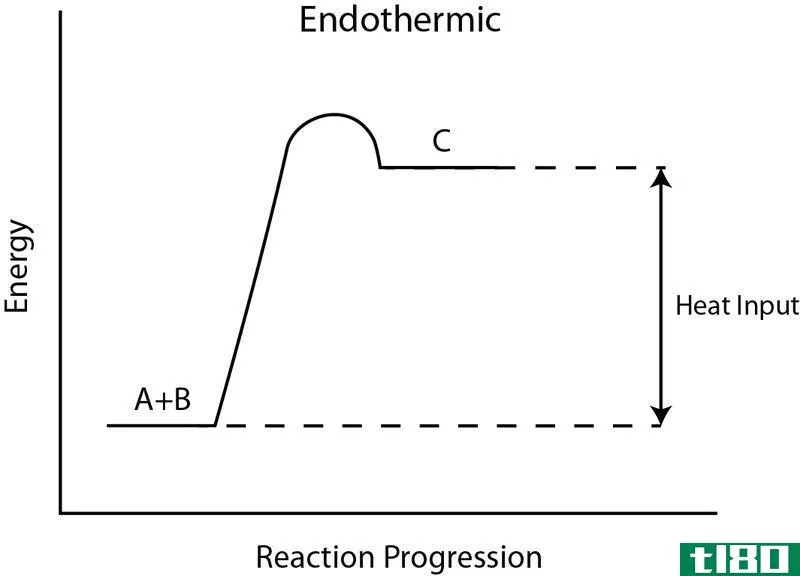
吸热一词来源于希腊语,其中“Endo”表示“inside”,而“Thermic”则指“heat”,因此,吸热反应是指从周围环境中吸收热量的反应。在吸热反应的情况下提供热量。两个或两个以上的分子或反应物在热的存在下反应生成产物。因此,它通过吸收能量来冷却周围的环境。此外,它以产品的化学键的形式储存能量。因此,在吸热反应的情况下,产物比反应物具有更多的能量。它在热力学、物理、化学中有应用。此外,由于反应过程中的吸热,ΔH值始终为正值。
例子
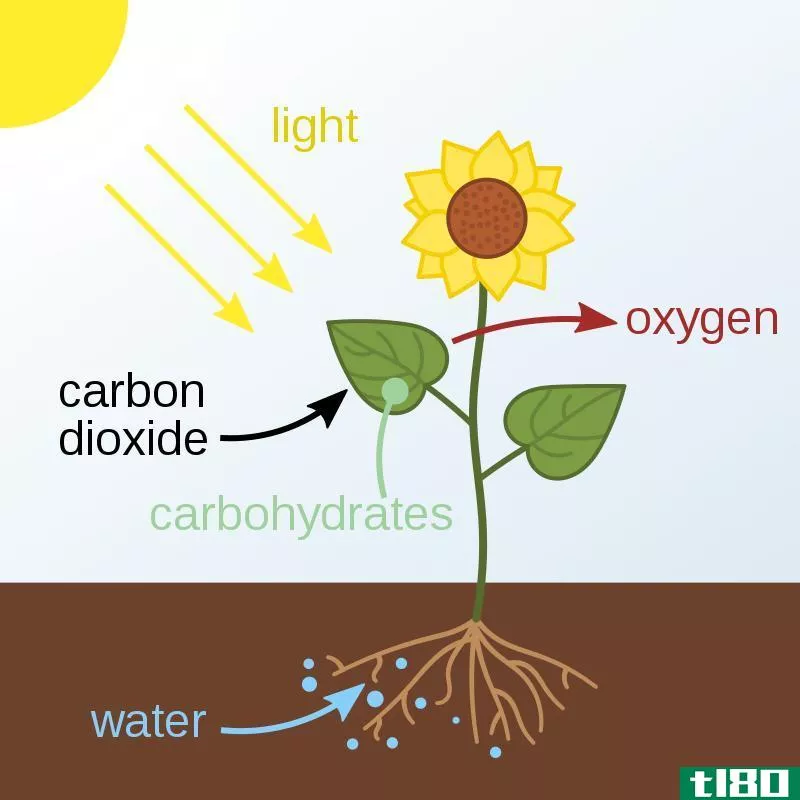
光合作用是一种吸热反应,叶绿素利用二氧化碳、水和来自阳光的能量来产生葡萄糖和氧气。
什么是放热反应(exothermic reacti***)?
“放热”一词来源于希腊语,其中“exo”表示“外部”,而“Thermic”指“热”,因此,放热反应是热量释放到周围环境中的反应。在放热反应的情况下放热。有时,如果反应发生得更快,那是有害的。两个或两个以上的分子通过释放能量反应形成产物。因此,它增加了周围环境的温度。因此,在放热反应的情况下,反应物比产物有更多的能量。它在热力学、物理、化学方面也有应用。在反应过程中,放热值总是负值。
例子
它的例子是一个营火,其中热量以光和热的形式从纸和木头的化学键中释放出来,使周围的人感到温暖。
主要区别
- 系统从环境中吸收能量的反应称为吸热反应,而系统向环境释放能量的反应称为放热反应。
- 在“吸热”一词中,“Endo”的意思是“内部”,而“Thermic”则意味着“热”;另一方面,在“exo”一词中,“exo”表示“外部”,而“Thermic”则指“热”
- 吸热反应需要能量才能完成,而放热反应不需要能量。
- 吸热反应有低能反应物但高能产物相反放热反应有高能反应物但低能产物。
- 吸热反应通过从反面吸收能量使环境变冷;放热反应通过释放温度使环境变热。
- 能量在吸热反应中被吸收,而在放热反应中,能量通常以热的形式释放,但也可以以电、光或声音的形式释放。
- 在吸热反应中,由于吸热反应,ΔH值始终为正值,而在放热反应中,由于能量释放,ΔH值始终为负值。
- 光合作用是吸热反应的例子,而篝火是放热反应的例子。
对比视频
结论
从上面的讨论可以得出结论:吸热反应是吸收热量并将其储存在其产物的化学键中的反应,例如光合作用,而放热反应是将其反应物的储存能量释放到周围环境中的反应,例如篝火