主要区别
肉眼看不见的东西总会引起人们的好奇心。他们不仅想知道更多关于这类事情的知识,而且还假定某些观点可能并不完全准确,但满足了人类求知欲强的本性。化学是这样一门学科,在这门课中,我们讨论了一些我们没有看到的方面,这两个术语是共价键和离子键。它们彼此相反,具有不同的性质,将在下面几行中讨论。债券是将两种东西结合在一起的实体。要了解它们之间的区别,需要定义这两个术语。共价键是原子间共享两个电子对而形成的化学键。另一方面,离子键是一个电子转移到另一个原子的过程。它不会像电子那样产生任何对,而且有将它们捐赠给其他原子的倾向。它们之间的另一个区别是共价键彼此之间的吸引力很低,而离子键的吸引力却很高。主要区别在于,在共价键中,键发生在两种非金属之间,而在离子键中,极性发生在金属和非金属物质之间。离子键没有合适的形状,因为它们在接受或捐赠电子时结构会发生变化,但共价键总是有一个好的形式。共价键被称为分子键,而离子键称为电价键。由于其不规则的结构,离子键具有较高的熔点,但由于共价键中有一个适当的结构,它们的熔点较低。在讨论这两种键的沸点时也是如此。二者的另一个主要区别是,共价键可以在室温下以气态或水态存在,而离子键则始终处于稳定状态。为了更好地理解,下面两段将对这两种类型的化学键进行简要解释。
比较图
共价键的定义
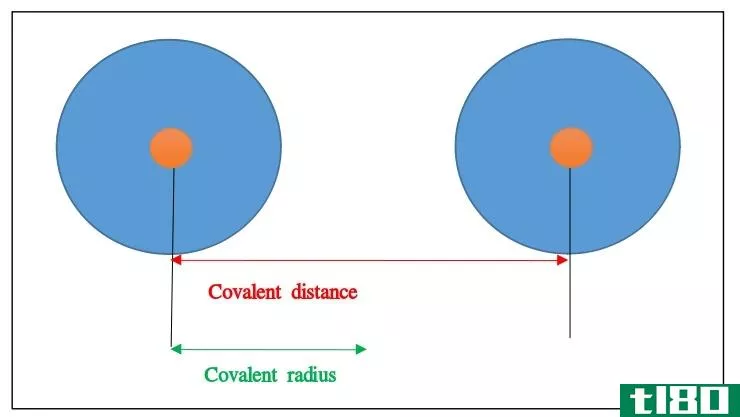
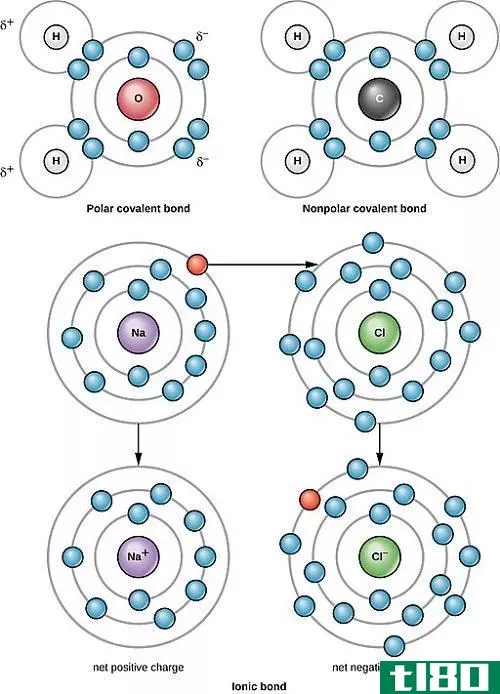
共价键是原子间共享两个电子对而形成的化学键。这些电子对之所以被称为键对,是因为原子间的正、负作用力分布均匀。它们有许多特性,例如有一个明确的结构,使它们能够有一个适当的外观。它们的熔点很低,沸点也很低。这些因素使它们成为电的不良导体。大多数共价键都可以在气体、液体和固体中找到,但在室温下它们不能稳定存在。因为它们是成对的,所以没有电荷,因此,它们不代表任何极性,不溶于水。最好的共价键例子是盐酸和甲烷。
离子键的定义
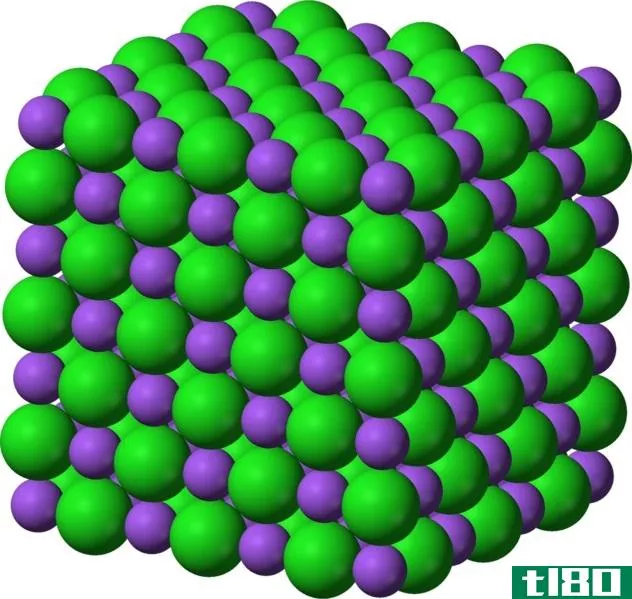
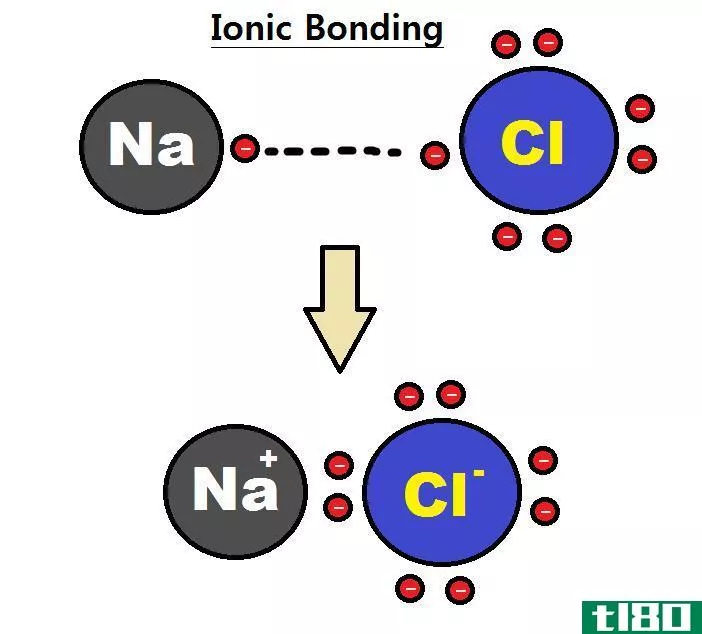
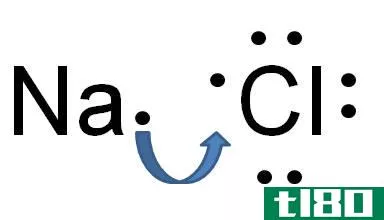
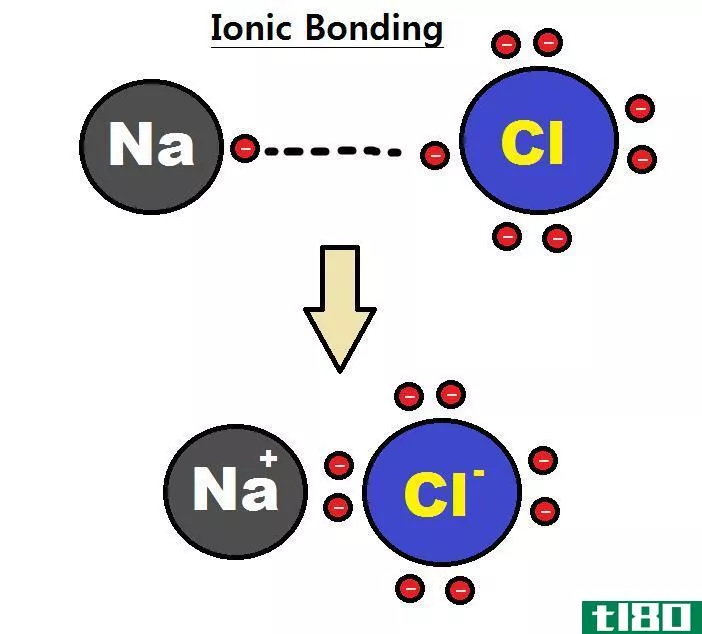
离子键可以解释为一个电子转移到另一个原子的过程。它不会像电子那样产生任何对,而且有将它们捐赠给其他原子的倾向。通常,这个过程产生两个相反的带电离子。当金属产生一个电子时,它就带上了正电荷,而当它获得一个电子时,它就变成了负电荷。它总是在两种金属和非金属物质之间形成。由于非金属比金属更强大,它们可以很快从金属中获得一个电子来完善自己。它们中间带负电荷,而捐电子的金属带正电荷。在不同的带电粒子之间存在着一种吸引力,正因为如此,这种结合发生了。离子键最好的例子是硫酸和氯化钠。由于它们的结构,它们的形状不合适,熔点和沸点都很高。在室温下,它们总是以固体的形式存在,是极好的导电体。另一个特点是它们溶于水。
一言以蔽之
- 当电子以成对的形式连接在一起时形成共价键,而当电子从一个原子共享到另一个原子时形成离子键。
- 共价键总是在两种非金属物质之间形成。离子键总是在一些金属元素和非金属元素之间产生。
- 共价键在室温下的状态要么是气体,要么是液体。在常温下,离子键的状态总是固态的。
- 共价键具有较低的熔点和沸点,而离子键具有较高的熔点和沸点。
- 共价键的极性很低,而离子键更容易吸引电子。
- 共价键中总是有一种特殊的结构,而离子键则缺乏合适的形状。
- 离子键的最好例子是氯化钠,而共价键的最好例子是盐酸。
- 共价键是电的不良导体,而离子键在熔化时导电。
- 离子键溶于水,不溶于其他液体;共价键不溶于水,溶于非极性液体。
结论
化学可能是一门很难理解的学科,而其中涉及的术语可能会成为对这个学科没有太多了解的人的头疼。债券是一个重要因素,因此这里已经正确解释了债券,以便能够形成一个明确的理解,希望本文能够在这方面有所帮助。