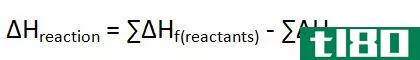化学和物理中的焓定义
焓是一个系统的热力学性质。它是加在系统压力和体积乘积上的内能之和。它反映了做非机械工作的能力和释放热量的能力。

焓表示为H;用h表示的比焓。用于表示焓的常用单位是焦耳、卡路里或BTU(英国热量单位)。节流过程中的焓是恒定的。
焓的变化是计算出来的,而不是焓的变化,部分原因是系统的总焓无法测量,因为不可能知道零点。然而,可以测量一种状态和另一种状态之间的焓差。焓变可在恒压条件下计算。
一个例子是一名消防队员站在梯子上,但浓烟遮住了他的视线。他看不到他下面离地面有多少横档,但可以看到窗户上有三个横档,有人需要被救出。同样,总焓无法测量,但焓的变化(三个阶梯)可以测量。
焓公式
H=E+PV
其中H是焓,E是系统的内能,P是压力,V是体积
DH=TDS+PDV
什么是焓的重要性(the importance of enthalpy)?
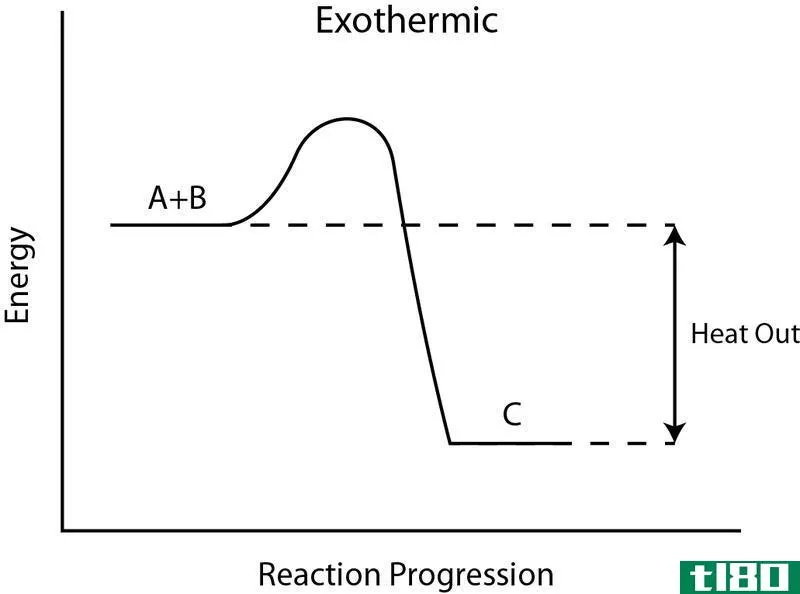
- 通过测量焓的变化,我们可以确定反应是吸热的(吸收的热量,焓的正变化)还是放热的(释放的热量,焓的负变化)
- 它用于计算化学过程的反应热。
- 焓的变化用于量热计中的热流测量。
- 测量它是为了评估节流过程或焦耳-汤姆逊膨胀。
- 焓用于计算压缩机的最小功率。
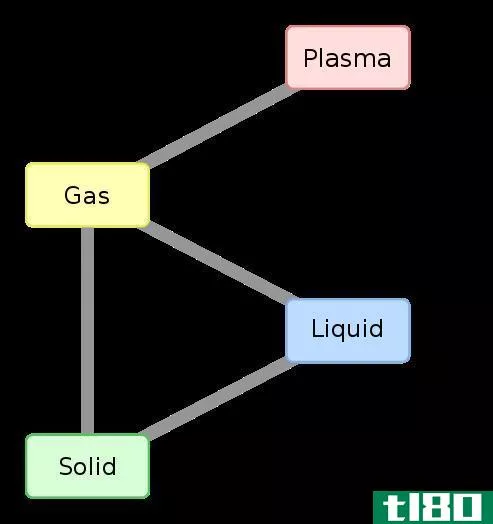
- 焓变发生在物质状态的变化过程中。
- 焓在热工中还有许多其他的应用。
焓计算中的示例变化
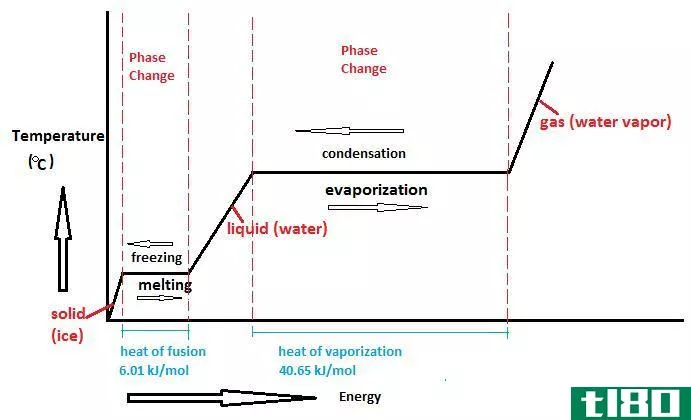
你可以用冰的熔化热和水的蒸发热来计算当冰融化成液体,液体变成蒸汽时的焓变。
冰的熔化热为333 J/g(即当1克冰融化时吸收333 J)。100°C下液态水的蒸发热为2257 J/g。
A部分:计算这两个过程的焓变化ΔH。
H2O(s)→ H2O(l);ΔH=?H2O(l)→ H2O(g);ΔH=?第B部分:使用您计算的值,找出使用0.800 kJ热量可以融化的冰的克数。
解决方案。聚变热和汽化热的单位是焦耳,所以首先要做的是转换成千焦耳。使用周期表,我们知道1摩尔水(H2O)为18.02克。因此:聚变ΔH=18.02 g x 333 J/1 g聚变ΔH=6.00 x 103 J聚变ΔH=6.00 kJ汽化ΔH=18.02 g x 2257 J/1 gvaporizationΔH=4.07 x 104 J汽化ΔH=40.7 kJSo完成的热化学反应为:H2O(s)→ H2O(l);ΔH=+6.00 kJH2O(l)→ H2O(g);ΔH=+40.7 kJB。现在我们知道:1 mol H2O(s)=18.02 g H2O(s)~6.00 kJ使用此转换系数:0.800 kJ x 18.02 g冰/6.00 kJ=2.40 g冰融化
回答
A.H2O(s)→ H2O(l);ΔH=+6.00千焦
H2O(l)→ H2O(g);ΔH=+40.7千焦
B.2.40克融化的冰
- 发表于 2021-09-15 16:34
- 阅读 ( 212 )
- 分类:化学
你可能感兴趣的文章
键焓(bond enthalpy)和晶格焓(lattice enthalpy)的区别
键焓和晶格焓的关键区别在于,键焓是分解化学键所需的能量,而晶格能是从气态的阳离子和阴离子形成一摩尔离子化合物所需的能量。 这两个术语都描述了系统与其周围环境之间的能量交换。键焓与晶格焓相反。键焓解释...
- 发布于 2020-10-15 02:15
- 阅读 ( 437 )
生成热(heat of formation)和反应热(heat of reaction)的区别
...一摩尔物质过程中的焓变化,而反应热是在恒压下发生的化学反应过程中焓的变化。 生成热和反应热是化学反应的重要焓值。我们将这些术语定义为标准条件,即标准压力和标准温度。在这里,热或焓是在化学反应过程中从系...
- 发布于 2020-10-18 06:22
- 阅读 ( 523 )
自由能(free energy)和焓(enthalpy)的区别
...是两个热力学术语,用来解释热能与热力学系统中发生的化学反应之间的关系。自由能或热力学自由能是一个热力学系统能做的功的量。换言之,自由能是热力学系统中进行热力学功的可用能量。另一方面,焓是一个热力学量,...
- 发布于 2020-10-19 11:40
- 阅读 ( 612 )
融合(fusion)和汽化(vaporization)的区别
...蒸汽。 熔合一词在不同的领域有不同的定义,但在物理化学中,我们用它来描述熔化的过程。也就是说,聚变是将固相转化为液相。另一方面,液体转化为固体称为冻结或凝固。如果物质的液相转变为气相,我们称之为汽化。...
- 发布于 2020-10-23 03:09
- 阅读 ( 323 )
热化学(thermochemistry)和热力学(thermodynamics)的区别
热化学(thermochemistry)和热力学(thermodynamics)的区别 热力学是物理科学的一个分支,研究热与其他形式的能量(如机械能、电能或化学能)之间的关系。热化学是热力学的一个分支。热化学也是化学的一个分支,它描述与化学反...
- 发布于 2020-10-24 03:12
- 阅读 ( 549 )
焓(enthalpy)和热(heat)的区别
焓和热之间的关键区别在于,焓是在恒压下化学反应过程中传递的热量,而热是能量的一种形式。 为了研究化学,我们把宇宙分成两个部分:一个系统和一个周围。系统是我们调查的对象,其余的是周围的。热和焓是描述系...
- 发布于 2020-11-05 19:40
- 阅读 ( 881 )
键能(bond energy)和键离解能焓(bond dissociation energy enthalpy)的区别
...解能是共价键(也称为分子键,是两个非金属原子之间的化学键,涉及这些原子之间的电子对共享)被均裂(分解为相等的碎片)裂解产生碎片时的标准焓变;通常是激进的物种。因此,键能和键离解能之间的主要区别是键能是...
- 发布于 2021-06-26 10:13
- 阅读 ( 471 )
焓(enthalpy)和内能(internal energy)的区别
...是动能。焓和内能的主要区别在于,焓是发生在系统中的化学反应中吸收或放出的热量,而内能是系统中势能和动能的总和。 覆盖的关键领域 1.什么是焓-定义、单位、计算公式、性质、示例2.什么是内能-定义、计算公式、性质...
- 发布于 2021-06-29 08:17
- 阅读 ( 934 )
简历(cv)和内容提供商(cp)的区别
...要差异cv(main difference cv) vs. 内容提供商(cp) 热力学是物理化学的一个分支,它描述热能与其他形式能量的关系。CV和CP是热力学中的两个术语。CV是定容比热,CP是定压比热。比热是将物质(单位质量)的温度升高一摄氏度所需的...
- 发布于 2021-06-29 08:29
- 阅读 ( 836 )
吸热的(endothermic)和放热反应(exothermic reactions)的区别
...(exothermic reacti***) 根据环境与反应体系之间的能量传递,化学反应可分为吸热反应和放热反应。为了将一个特定的化学反应分为吸热反应和放热反应,我们可以计算反应物和产物之间的焓变。如果没有,我们可以观察反应混合物...
- 发布于 2021-06-29 08:53
- 阅读 ( 1300 )