键焓和晶格焓的关键区别在于,键焓是分解化学键所需的能量,而晶格能是从气态的阳离子和阴离子形成一摩尔离子化合物所需的能量。
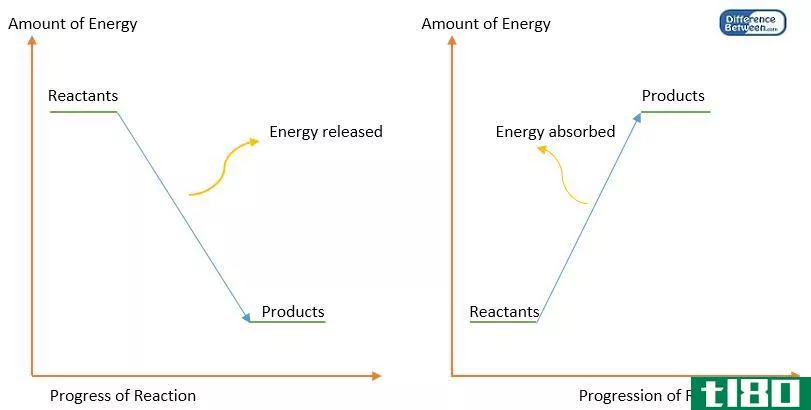
这两个术语都描述了系统与其周围环境之间的能量交换。键焓与晶格焓相反。键焓解释键断裂,晶格焓解释键的形成。这就是为什么它们是对立的现象。
目录
1. 概述和主要区别
2. 什么是键焓
3. 什么是晶格焓
4. 并列比较-键焓与晶格焓的表格形式
5. 摘要
什么是键焓(bond enthalpy)?
键焓是分解化学键所需的能量。如果我们在这里应用标准定义,它说键焓是物质在298 K下一摩尔键被破坏时的焓变。由于这个术语涉及键断裂,我们也可以将其命名为键离解能。其他同义词包括键强度和平均键能。

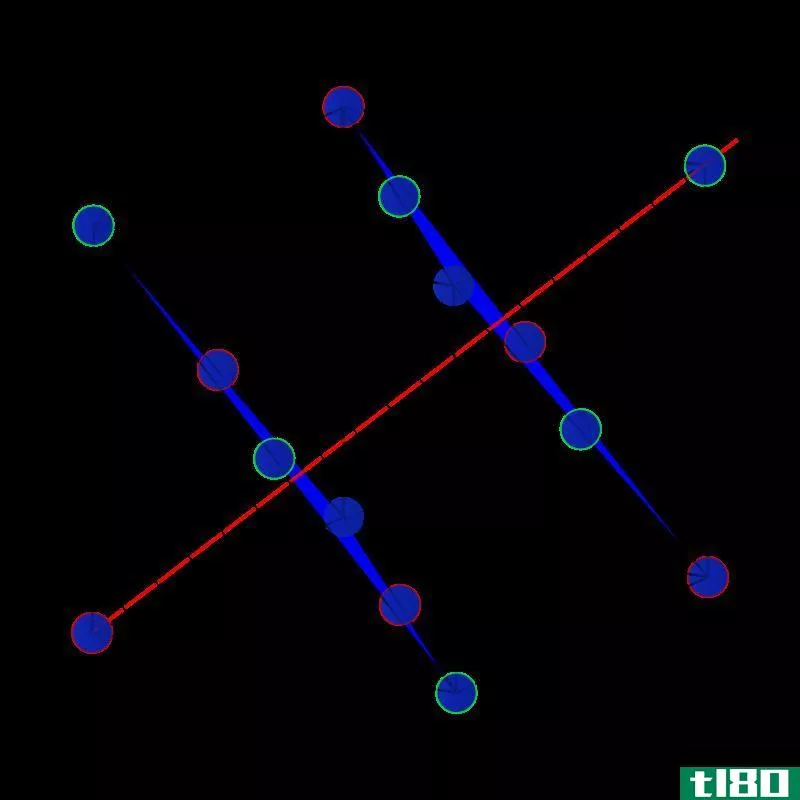
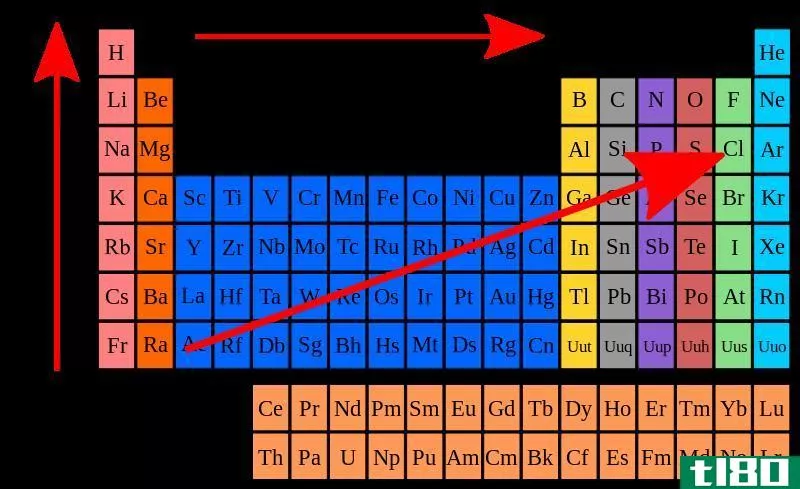
图01:一些化学键的键能
如果键的焓值很高,说明键很强,很难分解。因此,它需要更多的能量来分解这种特殊的键。通常,我们用来确定键焓值的单位是kcal/mol(千卡每摩尔)或kJ/mol(千焦每摩尔)。
什么是晶格焓(lattice enthalpy)?
在标准条件下,阴离子和离子的摩尔数,是离子的摩尔数。因为我们在这里讨论晶格,所以术语晶格焓被用于晶格;换句话说,它适用于固体化合物。凝聚力是一种结合力。

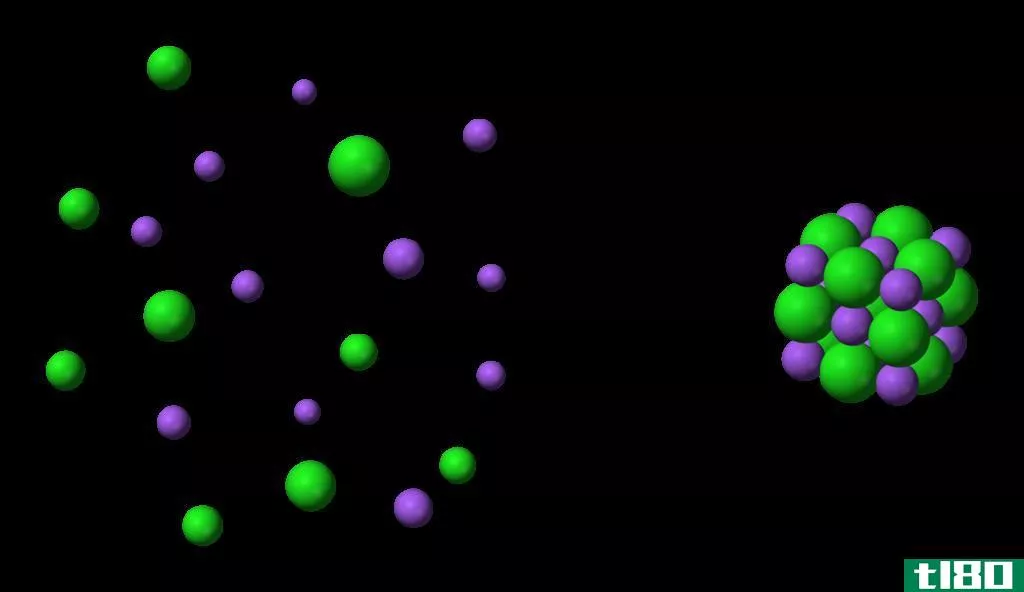
图02:晶格结构
一般来说,晶格能在确定某些物理性质(包括晶体的溶解度、硬度和挥发性)时非常重要。通常,晶格能是负能量,但晶格焓是正值。这是因为当形成晶格时,一摩尔晶体固体的体积减小。
键焓(bond enthalpy)和晶格焓(lattice enthalpy)的区别
键焓是与晶格焓相反的过程,因为键焓处理键断裂,而晶格焓处理键形成。因此,键焓和晶格焓的关键区别在于,键焓是分解化学键所需的能量,而晶格能是从气态的阳离子和阴离子形成一摩尔离子化合物所需的能量。键焓是一种物质在298K温度下,一摩尔键断裂时的焓变,因此也可以称之为键离解焓。
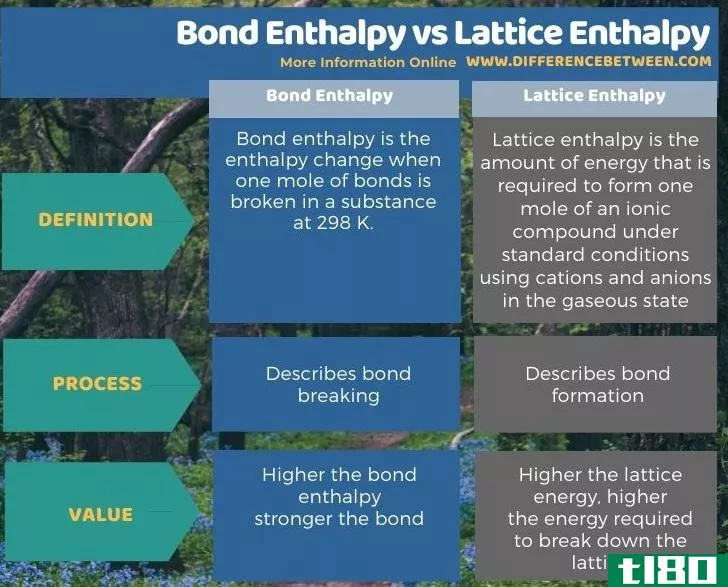
总结 - 键焓(bond enthalpy) vs. 晶格焓(lattice enthalpy)
键焓与键断裂有关,晶格焓与键形成有关。因此,键焓和晶格焓的关键区别在于,键焓是分解化学键所需的能量,而晶格能是从气态的阳离子和阴离子形成一摩尔离子化合物所需的能量。
引用
1赫尔曼斯汀,安妮·玛丽。“化学中的键焓定义”,ThoughtCo,2019年8月8日,可在此处查阅。“邦德能源”,维基百科,维基媒体基金会,2019年11月4日,可在这里查阅。“晶格能量”,维基百科,维基媒体基金会,2019年11月11日,可在这里查阅。
2“邦德能源”,维基百科,维基媒体基金会,2019年11月4日,
三。“晶格能量”,维基百科,维基媒体基金会,2019年11月11日,