终点和化学计量点之间的关键区别在于终点在化学计量点之后,而化学计量点是中和完成的最精确的点。
酸碱滴定包括中和反应,中和反应发生在酸与化学上等量的碱反应的点上。然而,理论上反应结束的点和我们实际检测到的点有一点差别。此外,您还应该注意到,术语等效点是化学计量点更常用的名称。
目录
1. 概述和主要区别
2. 什么是端点
3. 什么是化学计量点
4. 并列比较-以表格形式显示终点与化学计量点
5. 摘要
什么是终结点(endpoint)?
反应似乎完成的点是滴定的终点。我们可以通过实验确定这一点。让我们考虑一个例子来实际理解这一点。假设我们用0.5 M氢氧化钠滴定100毫升0.1 M盐酸(HCl)。
盐酸(aq)+NaOH(aq)⟶H2O+NaCl(aq)
我们将酸保存在滴定瓶中,并以甲基橙为指示剂,用NaOH滴定。在酸性介质中,指示剂无色,在碱性介质中呈粉红色。最初,滴定瓶中只有酸(HCl 0.1 M/100 ml);溶液的pH值等于2。当我们加入NaOH时,溶液的pH值由于介质中一定量的酸被中和而增加。我们必须一滴一滴地不断地加底,直到完成为止。反应完成后,反应的pH值变为7。即使在这一点上,指示器在介质中也不显示颜色,因为它改变了基本介质中的颜色。
在完成一滴NaOH后,我们需要再观察一滴NaOH的变化。此时溶液的pH值急剧变化。这是我们观察反应完成的地方。
什么是化学计量点(stoichiometric point)?
当量点是化学计量点的通用名称。它是酸或碱完成中和反应的点。理论上在这一点上反应已经完成,但实际上我们无法观察到确切的点。如果我们能确定何时达到等效点,那就更好了,因为它正是发生中和的确切点。然而,我们可以在终点观察到反应的完成。
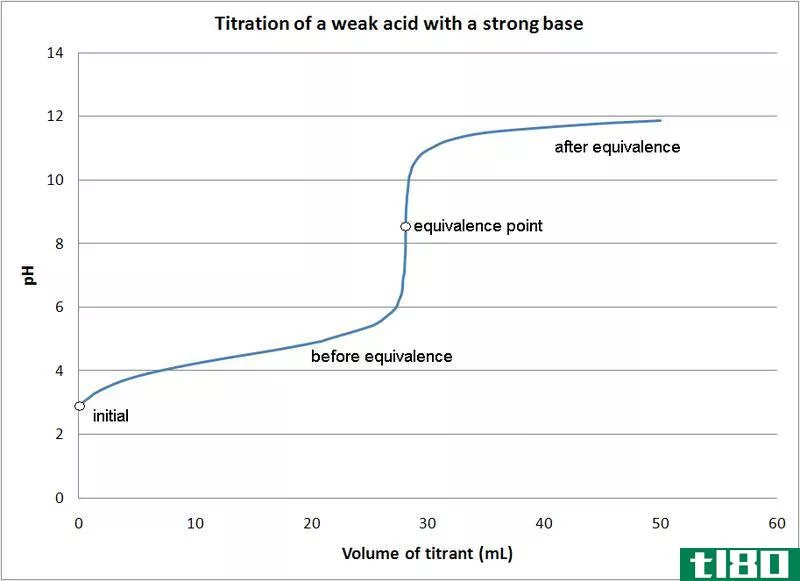
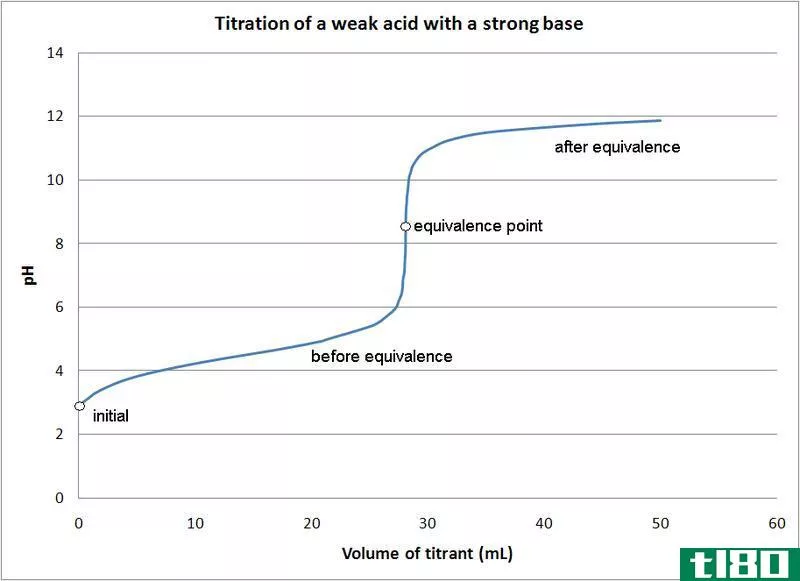
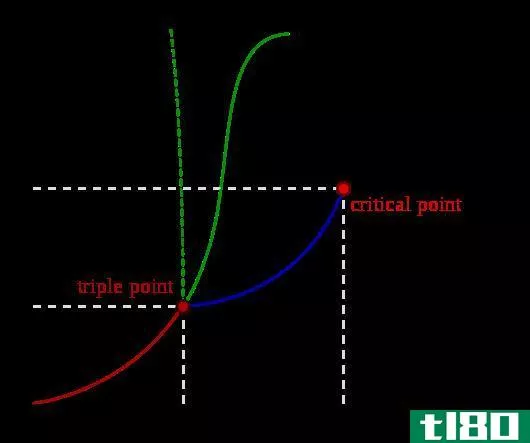
图01:显示当量点的滴定图
如果我们考虑与上述相同的例子,在反应开始时,介质中只有酸(HCl)。在达到当量点之前,加入NaOH,我们得到了未反应的酸并形成了盐(HCl和NaCl)。在等效点,我们只有盐在介质中。在终点,我们有盐和碱(NaCl和NaOH)在培养基中。
终结点(endpoint)和化学计量点(stoichiometric point)的区别
终点和化学计量点(通常,等效点)总是不同的。终点和化学计量点之间的关键区别是终点在化学计量点之后,而化学计量点是中和完成的最精确的点。此外,我们可以观察到终点,但实际上无法观察到化学计量点。

总结 - 终结点(endpoint) vs. 化学计量点(stoichiometric point)
终点和化学计量点(通常,等效点)总是不同的。终点和化学计量点之间的关键区别是终点在化学计量点之后,而化学计量点是中和完成的最精确的点。
引用
1赫尔曼斯汀,安妮·玛丽。“等效点定义”,ThoughtCo,May。2019年7月7日,可在这里购买。