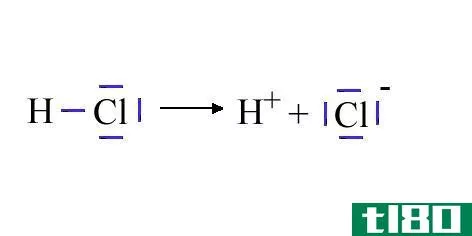主要区别
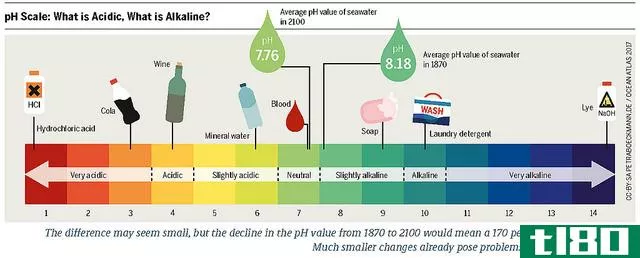
酸和碱的主要区别在于酸的pH值低于ph7,而碱性的pH值高于ph7。
酸的(acid) vs. 碱性(alkaline)
酸是一种低pH值低于ph7的化学品,而碱性溶液是一种高pH值高于ph7的化学品。酸性溶液由H+离子组成,而碱性溶液由OH-离子组成。酸有酸味,而碱性溶液的味道是苦的。酸的质地是粘的;另一方面,碱性的质地是滑的。碱可以中和酸;相反,酸可以中和碱性溶液。酸取决于氢离子的浓度;相反,碱性取决于氢氧化物离子的浓度。酚酞在酸性溶液中保持无色,而酚酞在碱性溶液中呈粉红色。酸使石蕊纸变成红色,而碱性使石蕊纸变成蓝色。酸经常被用作电池的电解液,去除金属上的铁锈,生产肥料,用于矿物加工;另一方面,碱性主要用于清洁洗衣粉、洗碗水和去污剂。一些常见的酸示例包括硫酸、盐酸和乙酸等,而碱性示例包括氢氧化钠、氢氧化钾和氢氧化镁。
比较图
什么是酸的(acid)?
根据阿伦尼乌斯的定义,“酸是一种化学物质,当溶解在水中时,溶液中的氢离子比在纯水中的活性大。”Br***tein Lowry将酸定义为一种能提供质子的物质。酸的pH值较低,低于ph7。它有酸味。根据温度不同,酸可以以固体、液体和气体的形式存在。它是一种能被碱中和的化学物质。在水溶液中,它们能够释放质子或氢离子。通常,能接受施主电子的化合物被称为路易斯酸。路易斯酸是指一些不含H+离子的化合物也被认为是酸。例如,三氯化铝(AlCl3)是一种路易斯酸。酸把石蕊纸变成红色。许多酸与金属发生反应,因为它们对金属有腐蚀作用,形成氢气(H2)和盐。酚酞在酸性溶液中保持无色。酸取决于氢离子的浓度。酸经常被用作电池的电解液、金属除锈、生产肥料和汽油、矿物加工以及食品和饮料的添加剂。
类型
- 强酸:能完全分解成离子。
- 弱酸:部分分解成离子。
示例
硫酸、盐酸、硝酸、乙酸、乳酸、柠檬酸。
什么是碱性(alkaline)?
根据阿伦尼乌斯的定义,“碱是一种能接受氢离子的水性物质。”布朗斯坦·洛里也将碱定义为任何接受质子的物质。碱性溶液的pH值高于ph7。这意味着碱性溶液由于pH值高而表现出基本性质,因此酸可以中和碱性溶液。它有苦味。从质地上看,由于碱和我们手上的油发生反应,碱性物质很滑。有些固体是碱性的,除了氨,是气体。当碱溶于水时,形成碱性溶液。碱是指碱金属或碱土金属的盐。
碱性词来源于第1组和第2组中的金属元素。元素周期表中第1组元素被称为碱金属。第2族元素被称为碱土金属。这两种金属,当加入水中时,由于与水分子反应生成金属氢氧化物和氢气,使其pH值升高。这种金属氢氧化物增加了溶液的pH值;同时,OH-离子的浓度也增加了。由于碱性溶液的碱性指示,红色石蕊纸变成蓝色。有些是腐蚀性的,但有些碱性溶液不是。
示例
氢氧化钠、氢氧化钾和氢氧化镁。
主要区别
- 酸是一种低pH值低于ph7的化学物质,而碱性溶液是一种高pH值高于ph7的化学物质。
- 酸性溶液由H+离子组成,而碱性溶液由OH-离子组成。
- 酸有酸味,而碱性溶液的味道是苦的。
- 酸的质地是粘的;另一方面,碱性的质地是滑的。
- 碱可以中和酸;相反,酸可以中和碱性溶液。
- 酸取决于氢离子的浓度;相反,碱性取决于氢氧化物离子的浓度。
- 酚酞在酸性溶液中保持无色,而酚酞在碱性溶液中呈粉红色。
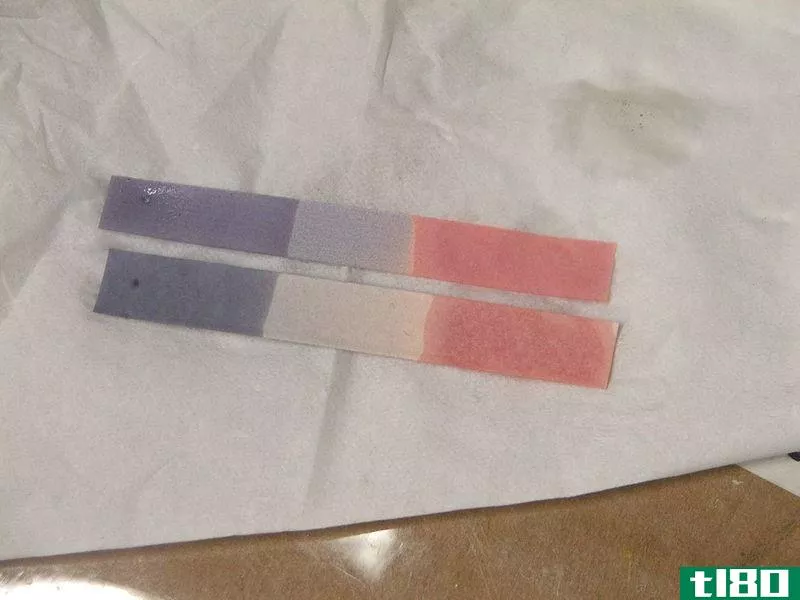
- 酸使石蕊纸变成红色,而碱性使石蕊纸变成蓝色。
- 酸经常被用作电池的电解液,去除金属上的铁锈,生产肥料,用于矿物加工;另一方面,碱性主要用于清洁洗衣粉、洗碗水和去污剂。
- 一些常见的酸示例包括硫酸、盐酸和乙酸等,而碱性示例包括氢氧化钠、氢氧化钾和氢氧化镁。
结论
上述讨论得出结论:酸性溶液的pH值低于pH7,而碱性溶液的pH值高于pH值7。