bradford和lowry蛋白质分析的关键区别在于,bradford蛋白质分析是基于染料考马斯亮蓝G-250的吸光度变化,而lowry蛋白质分析是基于肽键氧化产生的铜离子(Cu+)与Folin–Ciocalteu试剂的反应。
分析是一种分析技术,有助于确定样品的主要功能成分。因此,分析可以是定性或定量测试。包括检验医学、药理学、环境生物学、分子生物学、生物化学和免疫学等许多领域都经常使用这种检测方法。Bradford和Lowry蛋白质测定法是两种测定样品溶液中蛋白质浓度的生化分析方法。两种分析都使用比色技术来提供结果。
目录
1. 概述和主要区别
2. 什么是布拉德福德蛋白质测定法
3. 什么是Lowry蛋白测定法
4. Bradford法与Lowry法的相似性
5. 并列比较-布拉德福德与洛瑞蛋白质分析表形式
6. 摘要
什么是布拉德福德蛋白质测定(bradford protein assay)?
Bradford蛋白质分析法是一种快速的蛋白质光谱分析方法。它在测定溶液中蛋白质浓度时显示出很高的精确度。Marion Bradford在1976年介绍了这个程序。在这项分析中,总反应是基于所测蛋白质的氨基酸组成。换句话说,布拉德福德蛋白质测定法是一种比色法。它使用考马斯亮蓝染料。因此,这种比色蛋白质测定依赖于染料的吸光度变化。考马斯亮蓝G-250有三种形式:阳离子(红色)、阴离子(蓝色)和中性(绿色)。在酸性条件下,染料的红色形式转化为蓝色。它证实了蛋白质的结合。如果蛋白质不存在,溶液可能保持棕色。

图01:布拉德福德蛋白质分析
Bradford蛋白质分析法与其他蛋白质分析法不同,因为它不易受到蛋白质溶液中各种化合物的干扰。这些化合物包括钠、钾、葡萄糖和蔗糖等。
什么是洛瑞蛋白测定(lowry protein assay)?
Lowry蛋白质测定法是一种用于测定溶液中蛋白质总量的生化分析法。奥利弗·洛瑞是1940年发明这种试剂的人。该程序通过颜色变化描述溶液的总蛋白质浓度,该颜色变化与溶液中的蛋白质浓度成比例。因此,这也是一个比色蛋白质测定。
肽键氧化产生的铜离子(Cu+)与Folin–Ciocalteu试剂之间的反应是该过程的基础。本试剂还含有磷钼酸和磷钨酸。然而,Lowry蛋白分析的反应机理尚不清楚。但它涉及到半胱氨酸、色氨酸和酪氨酸残基的氧化作用。
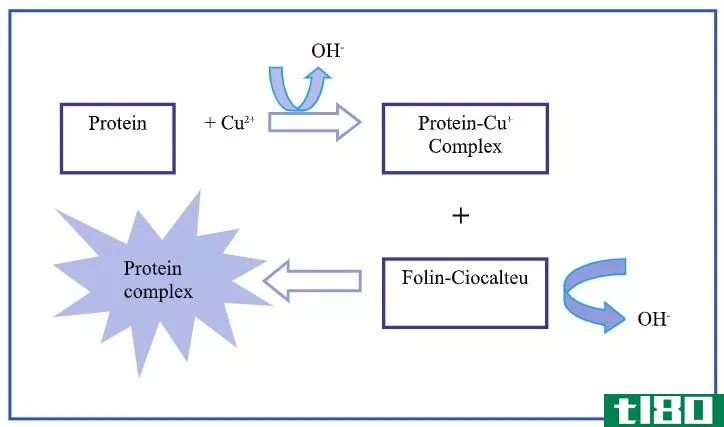
图02:Lowry蛋白质分析
半胱氨酸残基对Lowry蛋白质分析中观察到的吸光度有贡献,反应产生一个明亮的蓝色分子;杂多钼蓝。在660nm处用吸光度法测定该分子的还原度。因此,降低Folin-Ciocalteu试剂的半胱氨酸和色氨酸残基的浓度可推断溶液中蛋白质的总浓度。
布拉德福德(bradford)和洛瑞蛋白测定(lowry protein assay)的共同点
- Bradford和Lowry蛋白质分析测定溶液中的蛋白质浓度。
- 两种方法都是比色法。
- 而且,两种方法的灵敏度都很高。
布拉德福德(bradford)和洛瑞蛋白测定(lowry protein assay)的区别
Bradford和Lowry蛋白质分析是两种测定溶液中蛋白质浓度的分析方法。Bradford蛋白质分析依赖于染料考马斯亮蓝G-250的吸光度变化,而Lowry蛋白质分析则依赖于肽键氧化产生的铜离子与Folin–Ciocalteu试剂的反应。所以,这是布拉德福德和劳里蛋白质分析的关键区别。Bradford蛋白质分析需要15分钟才能得出结果,而Lowery蛋白质分析则需要40-60分钟才能得出结果。因此,这是Bradford和Lowry蛋白质分析的另一个区别。此外,Bradford蛋白分析依赖于氨基酸组成,而Lowry蛋白分析部分依赖于氨基酸组成。因此,这也是Bradford和Lowry蛋白质分析的区别。
下面的inforaphic提供了更多关于Bradford和Lowry蛋白质分析之间差异的细节。

总结 - 布拉德福德(bradford) vs. 洛瑞蛋白测定(lowry protein assay)
分析是一种分析技术,用于表征样品的主要功能成分。Bradford和Lowry蛋白质分析是两种在比色技术下起作用的蛋白质分析方法。Bradford和Lowry蛋白质分析都可以确定溶液中的蛋白质浓度。然而,Bradford和Lowry蛋白质分析的关键区别在于它们使用的比色技术。Bradford蛋白质分析使用考马斯亮蓝G-250,而Lowry蛋白质分析使用铜离子(Cu+)离子和Folin–Ciocalteu试剂。此外,Bradford法比Lowry蛋白分析法的结果更快。然而,这两种方法都是高度敏感的方法,受到各种物质的干扰。
引用
1《加拿大植物学杂志》。《加拿大植物学杂志》-60(7):1046-PDF,可在这里获得。“蛋白质分析化学”,美国赛默飞世尔科技有限公司,可在这里获取。
2“蛋白质分析化学”,美国赛默飞世尔科技公司,