氧化剂vs还原剂
氧化和还原反应结合在一起。当一种物质被氧化时,另一种物质就会减少。因此,这些反应统称为氧化还原反应。最初,氧化反应被认为是氧气参与的反应。在那里,氧与另一分子结合产生氧化物。在这个反应中,氧经历还原,另一种物质氧化。所以氧化反应基本上就是给另一种物质加氧。例如,在下面的反应中,氢经过氧化,因此氧原子加入到制氢水中。
2H2+O2->;2H2O
另一种描述氧化的方法是氢的损失。另一种描述氧化的方法是失去电子。这种方法可以用来解释化学反应,在那里我们看不到氧化物的形成或氢的损失。所以,即使没有氧气,我们也可以用这种方法来解释氧化。
氧化剂
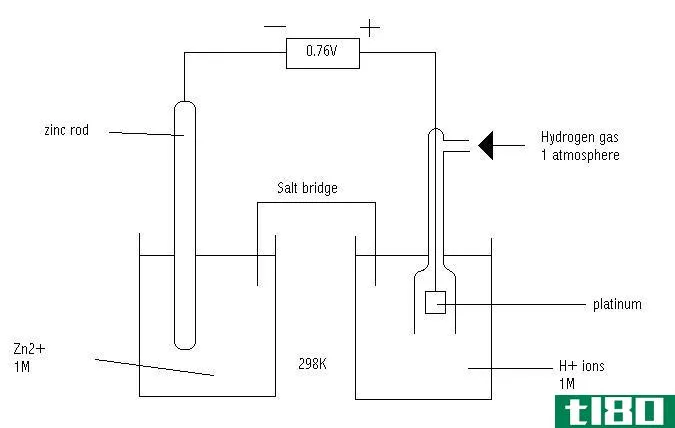
根据上述实例,氧化剂或氧化剂可定义为在氧化还原反应中从另一种物质中除去电子的试剂。因为它去除了电子,其他物质的氧化数会比反应物高。然后氧化剂进行还原。例如在下面的反应中,镁已经转化成镁离子。因为,镁失去了两个电子,它经历了氧化,氯气是氧化剂。
Mg+Cl2->;Mg2++2Cl–
在上述氢和氧之间的反应中,氧是氧化剂。氧在反应中是很好的氧化剂。此外,过氧化氢、硫酸、硝酸、卤素、高锰酸盐化合物和托伦试剂是一些常见的氧化剂。
还原剂
还原与氧化相反。就氧的转移而言,在还原反应中,氧是丢失的。在氢转移方面,还原反应发生在获得氢气时。例如,在上面的例子中,在甲烷和氧气之间,氧气减少了,因为它得到了氢气。就电子转移而言,还原就是获得电子。所以根据上面的例子,氯被还原了。
还原剂是在氧化还原反应中向另一种物质提供电子的物质。因此,另一种物质发生还原,还原剂被氧化。强还原剂具有很容易产生电子的能力。当原子半径较大时,原子核和价电子之间的吸引力减弱,因此较大的原子是很好的还原剂。此外,好的还原剂具有较低的电负性和较小的电离能。硼氢化钠、氢化铝锂、甲酸、抗坏血酸、汞齐钠和锌汞汞齐是常见的还原剂。
- 氧化剂在氧化还原反应中从另一种物质中除去电子,而还原剂则提供电子。
- 因此,氧化剂氧化其他物质,还原剂减少它们。
- 在反应过程中,氧化剂发生还原反应。相反,还原剂经历氧化。
- 与氧化剂相比,还原剂具有较低的电负性、较低的电离能和较高的原子半径。