偶极-偶极(dipole-dipole)和伦敦分散部队(london dispersion forces)的区别
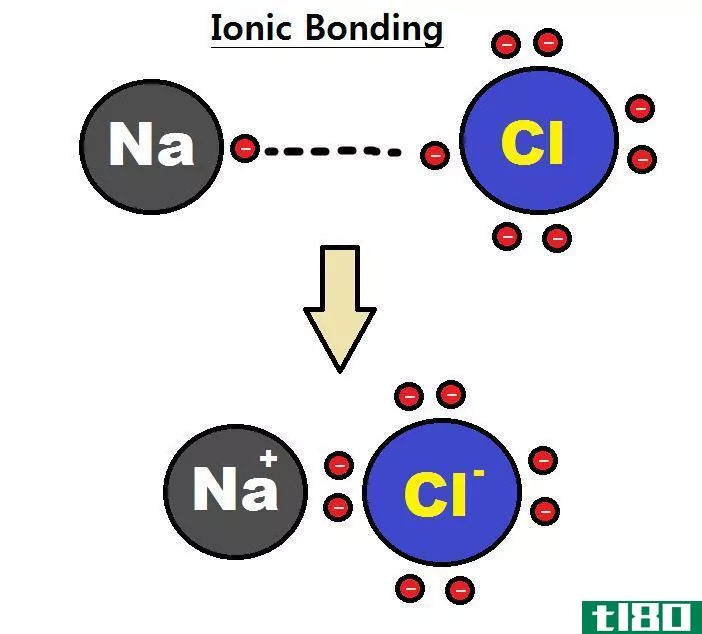
偶极-偶极和伦敦色散力是分子或原子之间的两种引力,它们直接影响原子/分子的沸点。偶极-偶极和伦敦色散力之间的关键区别在于它们的强度以及在哪里可以找到它们。伦敦色散力的强度相对弱于偶极-偶极相互作用,但这两种引力都弱于离子键或共价键。偶极和原子的相互作用有时只能在伦敦分子中发现。
什么是偶极-偶极力(dipole-dipole force)?
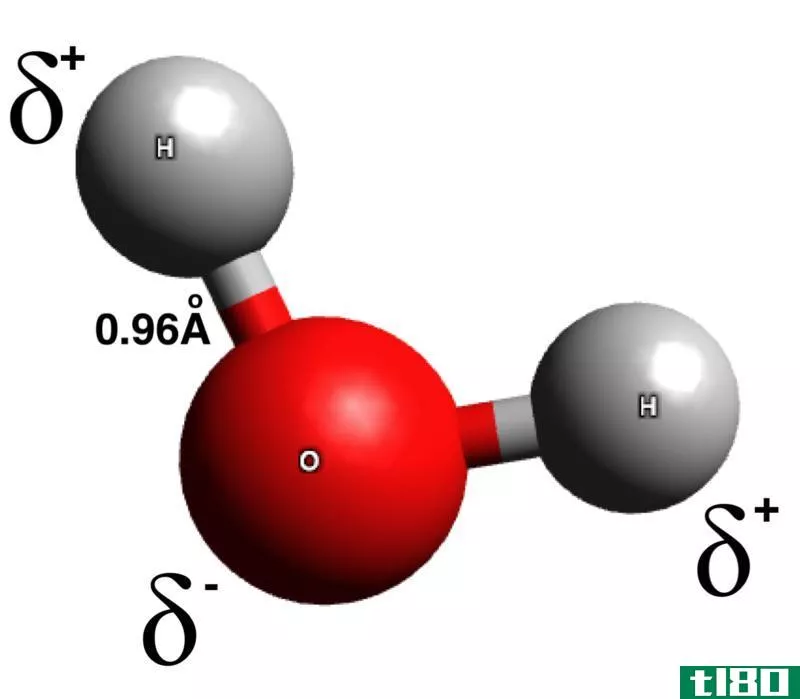
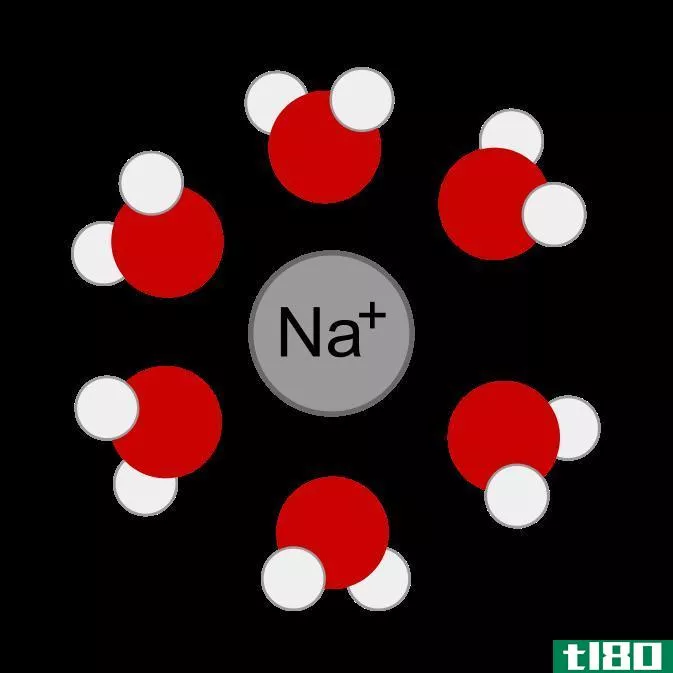
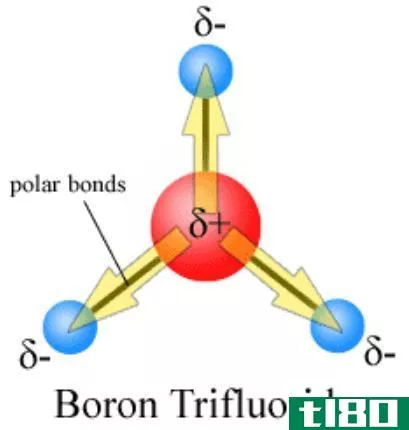
当两个相反极化的分子通过空间相互作用时,就会发生偶极-偶极相互作用。这些力存在于所有极性分子中。当两个原子形成共价键时,两个原子的电负性不同,就会形成极性分子。在这种情况下,由于电负性的差异,原子不能在两个原子之间均匀地共享电子。电负性大的原子比电负性小的原子更能吸引电子云,因此产生的分子具有微正端和微负端。其他分子中的正负偶极子可以互相吸引,这种吸引称为偶极-偶极力。

什么是伦敦分散部队(london dispersion force)?
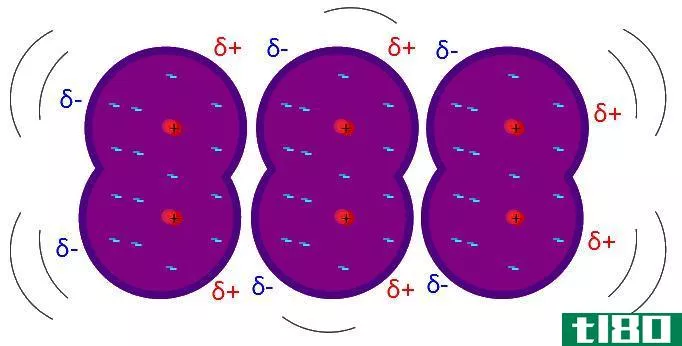
伦敦色散力被认为是相邻分子或原子间最弱的分子间作用力。当分子或原子中的电子分布出现波动时,伦敦色散力就产生了。例如,由于任何原子上的瞬时偶极子,这些类型的吸引力都会在相邻的原子中产生。它在相邻原子上诱导偶极子,然后通过微弱的引力相互吸引。伦敦色散力的大小取决于原子或分子中的电子在瞬间力的作用下极化的程度。它们是暂时的力,在任何分子中都可能存在,因为它们有电子。
偶极-偶极(dipole-dipole)和伦敦分散部队(london dispersion forces)的区别
定义:
偶极-偶极力:偶极-偶极力是极性分子的正偶极和另一个相反极化分子的负偶极之间的吸引力。
伦敦色散力:伦敦色散力是指当电子分布出现波动时,相邻分子或原子之间的暂时吸引力。
性质:
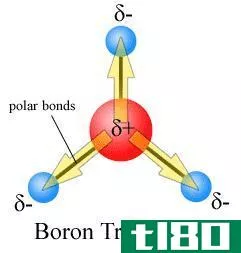
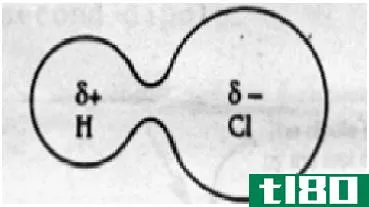
偶极-偶极力:偶极-偶极相互作用存在于极性分子中,如HCl、BrCl和HBr。当两个分子不均匀地共享电子以形成共价键时,就会出现这种情况。电子密度向更具电负性的原子移动,导致一端微负偶极子,另一端微正偶极子。
伦敦色散力:伦敦色散力可以在任何原子或分子中找到,其要求是电子云。伦敦色散力也存在于非极性分子和原子中。
强度:
偶极-偶极力:偶极-偶极力比色散力强,但比离子键和共价键弱。分散力的平均强度在1-10 kcal/mol之间变化。
伦敦分散力:由于伦敦分散力是临时力(0-1 kcal/mol),所以它们很弱。
影响因素:
偶极-偶极力:影响偶极-偶极力强度的因素是分子中原子之间的电负性差、分子大小和分子形状。换句话说,偶极子的相互作用随着键长的减小而增加。
伦敦分散力:伦敦分散力的大小取决于几个因素。它随原子中电子的数目而增加。极化率是影响伦敦色散力强度的重要因素之一,它是另一个原子/分子扭曲电子云的能力。具有较小电负性和较大半径的分子具有较高的极化率。相反,由于电子离原子核很近,所以很难扭曲较小原子中的电子云。
例子:
| 原子 | 沸点/oC | |
| 氦 | (他) | -269号 |
| 霓虹灯 | (东北) | -246个 |
| 氩 | (银币) | -186个 |
| 氪 | (韩元) | -152个 |
| 氙气 | (Xe) | -107个 |
| 重做 | (注册护士) | -62岁 |
Rn-原子越大,极易极化(极化率越高),并具有最强的吸引力。氦很小,很难扭曲,导致伦敦弥散力减弱。
Image Courtesy:
1. Dipole-dipole-interaction-in-HCl-2D By Benjah-bmm27 (Own work) [Public domain], via Wikimedia Comm***