浸出与萃取
浸出和萃取的区别可以用这两种过程中使用的化学原理来解释。浸出和萃取都是指从最初存在的混合物中分离出一种或几种化合物。当固体混合物与溶剂接触以分离可溶成分时,这个过程称为浸出。当混合物中的化合物在一个化学相中被分离到另一个时,称为萃取。
什么是浸出(leaching)?
浸出是一种将固体混合物中的组分与这些组分可溶的液体溶剂接触的过程。发生浸出需要三个重要因素。它们是化合物混合物、溶质和溶剂。当液体或溶剂被施加或与化合物混合物接触时,可溶于溶剂的组分开始溶解,而其他组分则保持在浆液中。这些溶解的组分被称为“溶质”。因此,在使用过量的溶剂时,这些溶质可以从最初的混合物中除去。即使只期望溶质存在于溶剂中,它也只在理想条件下发生。因此,溶剂通常含有浆液中的其他杂质。浸出是一种“固液”萃取。
当固体材料要从固体混合物中分离出来时,这种方法通常用于工业中。一些常见的例子包括用热水从甜菜中分离糖,用酸从金属矿石中分离金属等。在自然界中,重金属和其他土壤污染物是通过淋滤进入地下水的。

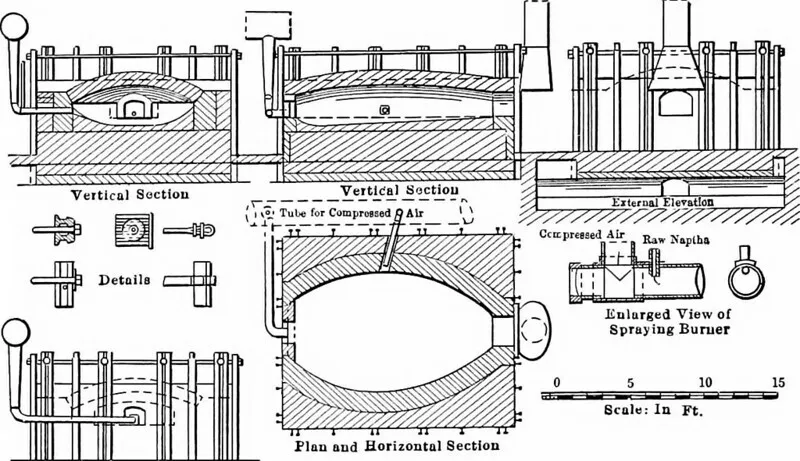
铁浸出
什么是提取(extraction)?
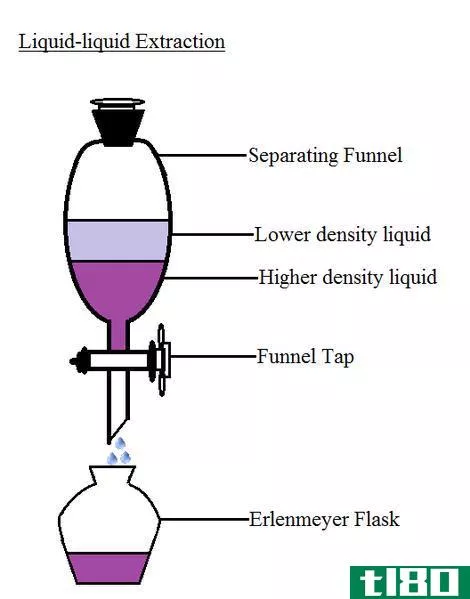
萃取也是从化合物混合物中分离组分的过程,但在这里,一个化学相中的化合物被分离到另一个相。萃取通常发生在两种不混溶的溶剂之间,这被明确称为“溶剂-溶剂”萃取。根据不同组分对所用溶剂的亲和力,化合物混合物可以在两种不混溶溶剂中分离成组分。上述亲和力通常是由于化合物的极性和各自的溶剂。常用的溶剂体系有水:乙酸乙酯、水:二氯甲烷、水/甲醇混合物:二氯甲烷、水/甲醇混合物:乙酸乙酯等。
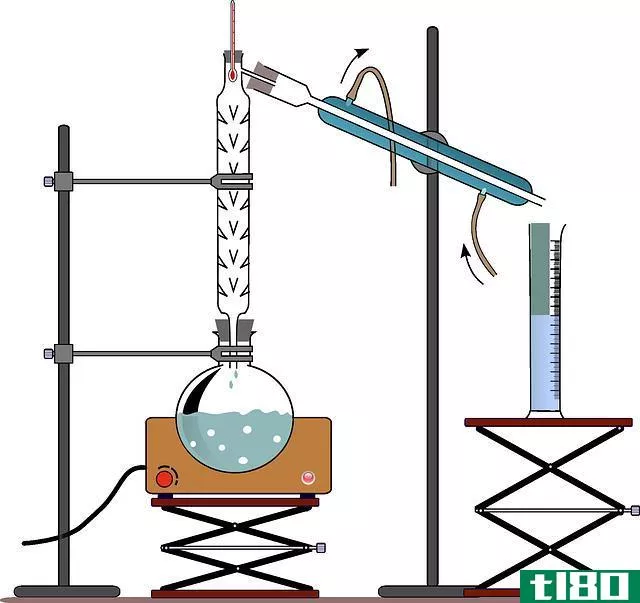
这项技术通常在化学实验室的技术条件下使用,在这种条件下,有机化合物会生成,或者作为混合物的一部分,需要分离出来。因此,进行有机溶剂萃取。从一个相到另一个相的特定化合物的萃取过程是由“分配理论”控制的。一旦一个或多个化合物从最初的混合物中分离出来进入第二个溶剂,就可以通过蒸发多余的溶剂来分离这些化合物。为此,使用了一种称为“旋转蒸发器”的仪器。
还有其他类型的萃取,如固相萃取。一些现代变体包括超临界二氧化碳萃取、超声波萃取、微波辅助萃取等。

浸出(leaching)和提取(extraction)的区别
•浸出和提取的定义:
•浸出是将混合物中的固体物质溶解在合适的溶剂中分离出来的过程。
•在萃取过程中,由于极性差异,给定化合物从一个化学相分离到另一个化学相。
•化学原理:
•通过可溶成分的浓度梯度进行浸出。
•提取受配分理论支配。
•应用:
•浸出法较为简单,通常用于工业规模。
•提取通常用于实验室水平。
- 通过Wikicomm***(公共领域)进行铁浸出
- PRHaney分离漏斗(CC by-SA 3.0)