氢化和还原的关键区别在于氢化需要催化剂,而还原不需要催化剂,除非是加氢。氢化反应是一种还原反应,其中分子氢与现有分子结合。因此,加氢和还原是相互联系的。
还原可以是氧化数的减少、氧的损失或氢的加入。但是有些还原反应不需要氧或氢作为反应物。因此,最可接受的还原定义是氧化数的减少。除了上述关键区别外,这两种化学反应之间还有一些其他的区别,比如化学反应的成分;具有双键或三键的分子可以进行氢化反应,而任何具有较高氧化数原子的分子都可以进行还原反应。
目录
1. 概述和主要区别
2. 什么是氢化
3. 什么是还原
4. 并列比较-表格形式的氢化与还原
5. 摘要
什么是氢化(hydrogenation)?
加氢是一种化学反应,包括向化学物质中添加分子氢。此外,这种反应通常在催化剂存在下发生:镍、钯、铂或它们的氧化物。它有助于减少或饱和一种化合物。氢化可以通过两种方式影响一个分子;
- Saturation of a compound containing either double or triple bonds
- Dissociation of a molecule
几乎所有的不饱和化合物都能与氢分子反应。
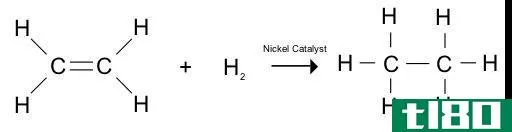
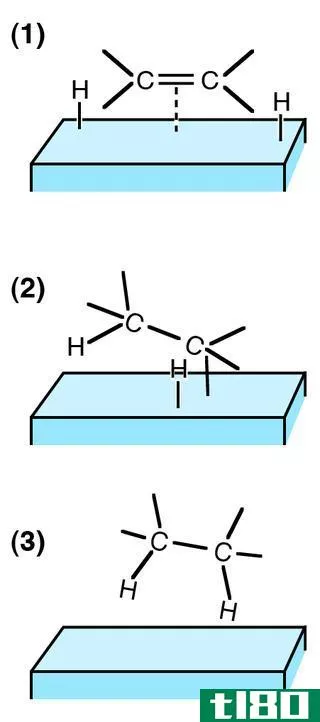
图01:烯烃加氢生成烷烃
这种化学反应在许多工业用途中都是有用的,用于合成不同的化合物,例如石油工业中用于生产不同的石油化工产品的氢化反应。
什么是减少(reduction)?
还原是化学物质氧化数的减少。这个反应是氧化还原反应的一半反应(氧化还原反应有两个平行发生的化学反应:氧化和还原)。还原反应降低氧化数,氧化反应增加氧化数。

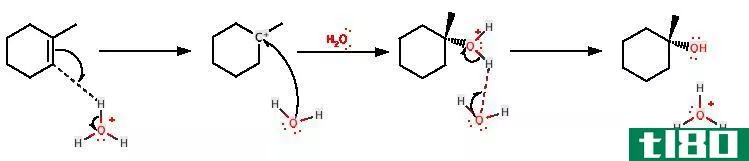
图02:白屈菜酸还原
有时,还原是除去氧或向化学物质中添加氢。此外,这种反应主要发生在三个方面:将氧化数从正值减小到负值,从零减小到负值,或从负值减小到更大的负值。还原反应的一个常见例子是铜(II)氧化成铜(0)的氧化数减少。
氢化(hydrogenation)和减少(reduction)的区别
加氢是一种化学反应,它包括向化学物质中添加氢分子。还原是化学物质氧化数的减少。氢化反应和还原反应相互关联,因为氢化是还原的一种形式。
然而,这两种化学过程之间存在一些差异,如下所示。例如,加氢本质上需要催化剂来进行反应,而还原则不需要催化剂,除非是加氢。不饱和化合物的氧化和还原也会发生。

总结 - 氢化(hydrogenation) vs. 减少(reduction)
加氢和还原反应是重要的化学反应,在工业上有着广泛的应用。氢化是还原的一种形式。氢化和还原的区别在于,氢化需要催化剂,而还原不需要催化剂,除非是加氢。
引用
1Helmenstine,Anne Marie博士,“化学还原定义”,ThoughtCo,2017年9月3日。这里有2个。“氢化作用”,维基百科,维基媒体基金会,2018年5月25日。此处提供
2“氢化作用”,维基百科,维基媒体基金会,2018年5月25日。