主要区别
电子几何学和分子几何学的主要区别在于,电子几何学包括分子中的键和电子对,而分子几何学只包括分子中存在的键的数目。
电子几何学(electron geometry) vs. 分子几何学(molecular geometry)
电子几何学是由分子中存在的电子对和键形成的;另一方面,分子几何学是由分子中存在的键形成的。电子几何学包含电子对;另一方面,分子几何学不包含电子对。在电子几何学中,孤对也被计算在内;而在分子几何学中,孤对也不计算在内。
在电子几何学中,考虑电子对的总数;在硬币的另一面,在分子几何学中,考虑参与成键的电子对的总数。电子几何学给我们提供了关于电子群的组织结构的信息;另一方面,分子几何学给我们提供了关于分子中除了孤对之外的原子的组织结构的信息。
电子几何学可以借助VESPR理论来确定;另一方面,分子几何学是由原子围绕中心原子核的排列来定义的。电子几何学包括成键电子对和非键电子对;另一方面,分子几何学只包括成键电子对。
比较图
什么是电子几何学(electron geometry)?
电子几何学是一种可以用来描述分子形状的几何学,它包括分子中存在的电子对和键对。它也可以通过VSEPR理论来确定。电子几何学的主要目的是通过原子和电子围绕中心原子的排列来确定分子的几何结构。电子对只在电子几何学中被考虑,而在分子几何学中被忽略。
它给出了围绕中心原子的电子群的排列。电子几何学也可以通过减少孤对电子之间的斥力来确定。在电子几何学中,它还考虑了具有不同密度的电子区域。非键电子也被称为孤对电子。这就是为什么电子几何学取决于这些电子区域的数目。通过减少这些电子区域之间的斥力,电子几何学给了我们分子的形状。
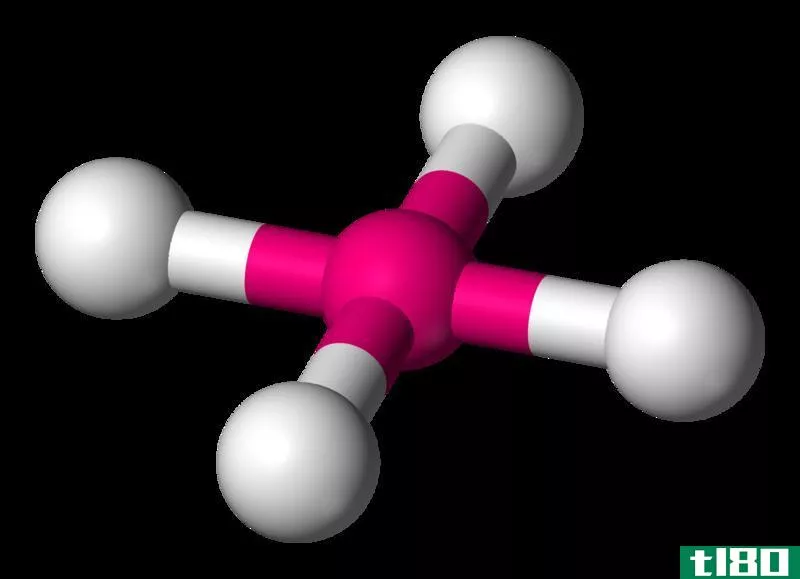
利用甲烷的公式可以给出一个电子几何学的例子。中心原子是碳,价电子数是4。四个价电子用氢原子表示,通过共享过程完成碳原子和氢原子的价壳层。分子结构中有四个单键。因此,总结出甲烷的几何结构是四面体的。
什么是分子几何学(molecular geometry)?
分子几何学是一种几何学,它可以用来描述分子的形状,而分子的形状只包括分子中存在的一对电子键。它是通过原子在中心原子核周围的排列来测量的。它的主要目的是通过原子在分子中的排列来找出分子的几何结构。在分子几何学中,主要不考虑电子对。它给出了原子在分子结构中的位置。
键合原子之间的斥力也被认为是较少找到几何的主要目的。电子几何学和分子几何学的主要区别在于,当我们讨论分子的形状时,意味着我们在决定分子的几何结构;另一方面,当我们讨论电子对的几何结构时,意味着我们在决定电子的几何结构。
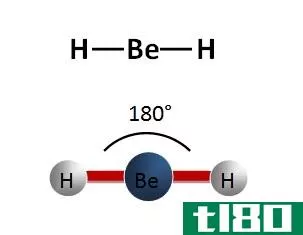
由于分子几何学是用来确定分子形状的,所以当我们讨论分子几何学中分子的形状时,我们必须使用刘易斯结构,以刘易斯法的形式画出它来确定键合电子的数目。分子几何学的例子是水分子。它包含两个成键电子和两个非键电子。中心原子是有两个孤对的氧分子。它通过共享的方法从氢原子接收两个键电子。所以,水分子的分子几何结构是弯曲的。
主要区别
- 电子几何学决定了包含电子对和键对的分子的形状;另一方面,分子几何学决定了只涉及键对的分子的形状。
- 电子几何学考虑电子对;另一方面,分子几何学不考虑电子对。
- 电子几何学有助于给出电子对的排列;相反,分子几何学有助于给出原子围绕中心核的排列。
- 电子几何学包括成键电子和非成键电子;另一方面,分子几何学只包括成键电子。
- 电子的几何结构也可以由VESPR理论来确定;另一方面,分子的几何结构也可以由中心原子核周围原子的排列来决定。
- 在电子几何学中,计算电子对和键对的总数;在分子几何学中,计算键对的总数。
结论
以上讨论得出结论,电子几何学和分子几何学都是用来确定分子形状的几何学。电子几何学给了我们分子的形状,它既包括成键电子对,也包括非键电子对;另一方面,分子几何学给我们的是只包括成键电子对的分子的形状。