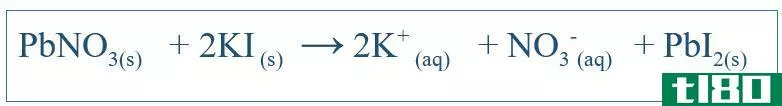什么是离子键?(ionic bonds?)

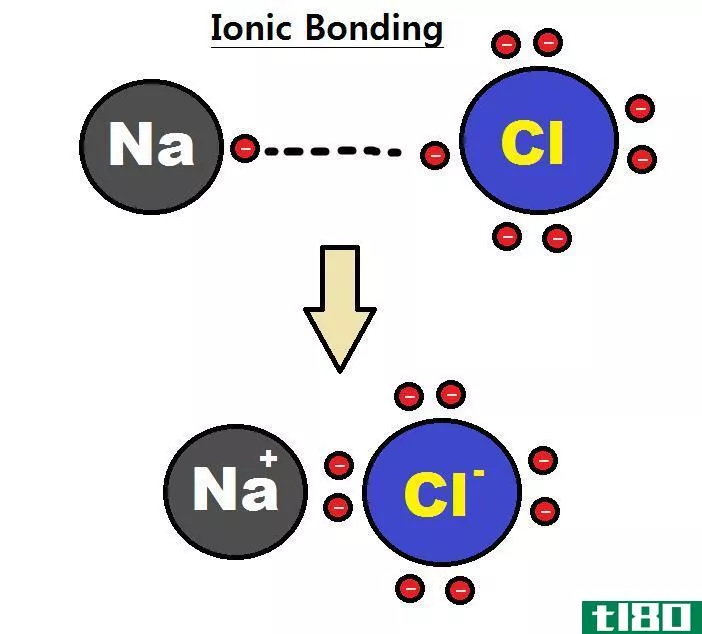
离子键是两个原子之间的一种静电键,弱于共价键,但通常强于氢键或范德瓦尔斯力,而范德瓦尔斯力正是保持水的力量。它们是离子相互吸引形成的。离子键的典型参与者是金属和非金属,如钠和氯。钠和氯结合形成一种典型的离子键合分子,氯化钠或普通食盐。
离子键可以用电子轨道理论来解释。每个原子都有一个等于或大于一的电子轨道。每个轨道都有一个最大电子极限,在这个极限之后,一个新的轨道被创建。我们所知道的元素的轨道数范围从氢或氦的1到原子序数大于铀的大分子的6、7或8。
电子轨道“希望”拥有最大数量的电子。这时它们处于最低或最稳定的能量状态。当一个从其顶轨道上只缺少一个电子的原子与一个在其顶轨道上只有一个电子的原子接触时,“想要”的原子从另一个原子“偷走”一个电子,从而稳定其轨道。结果是,它现在比质子多了一个电子,使其带负电。被盗电子的“受害者”相应地获得正电荷。在电磁理论中,对立面相互吸引,因此原子被迫相互缠绕,直到被热分解。这就是离子键。。
由于电子轨道在离子键中略微重叠,因此它们被认为是弱共价键,或由共享电子结合。最强的键是高度共价键,电子壳层彼此深度重叠。钻石就是一个例子。离子键和共价键之间的原子差异使钻石的熔点比岩盐的熔点高得多。有时,离子键中离子之间的电子差大于1。极性差越大,键就越牢固。。
浸入水中通常会击打离子结合材料,使其充分溶解。离子键合材料的分子性质也使其易于排列成晶体。除非熔化或悬浮在溶液中,否则它们是可怕的导电体。
- 发表于 2022-02-08 20:05
- 阅读 ( 99 )
- 分类:科学
你可能感兴趣的文章
电子的(electronic)和离子传导(ionic conduction)的区别
...据传导介质的不同分为两类。 目录 1. 概述和主要区别 2. 什么是电子传导 3. 什么是离子传导 4. 并列比较-电子和离子传导的表格形式 5. 摘要 什么是电子传导(electronic conduction)? 电子传导是以电流的形式传递能量的过程。这里,...
- 发布于 2020-10-01 10:15
- 阅读 ( 652 )
离子型(ionic)和金属晶体(metallic solids)的区别
...合物。这些离子被静电力凝聚在一起。我们把这些力称为离子键。离子相互结合的方式是整个化合物是中性的(没有负电荷或正电荷)。在这里,一个阴离子周围的阳离子数,反之亦然,取决于阳离子和阴离子的电荷量,不同固...
- 发布于 2020-10-15 16:13
- 阅读 ( 481 )
离子型(ionic)和二元化合物(binary compounds)的区别
.... 摘要 什么是离子化合物(ionic compounds)? 离子化合物是由离子键连接在一起的含有阳离子和阴离子的化合物。离子键是一种静电吸引力。这种吸引发生在相反的带电荷的离子(阳离子或带正电荷的离子和阴离子或带负电的离子)...
- 发布于 2020-10-16 01:42
- 阅读 ( 760 )
分子方程(molecular equation)和离子方程(ionic equation)的区别
...分子方程和离子方程的区别。 目录 1. 概述和主要区别 2. 什么是分子方程 3. 什么是离子方程 4. 并列比较-分子方程与离子方程的表格形式 5. 摘要 什么是分子方程(a molecular equation)? 分子方程表示反应物和产物的分子形式。相反...
- 发布于 2020-10-16 16:52
- 阅读 ( 578 )
完全离子型(complete ionic)和净离子方程(net ionic equation)的区别
...与最终产物形成的化学物种。 目录 1. 概述和主要区别 2. 什么是完整的离子方程 3. 什么是净离子方程 4. 并列比较-完整的离子与净离子方程式,表格形式 5. 摘要 什么是完全离子方程(complete ionic equation)? 完整的离子方程是解释...
- 发布于 2020-10-19 09:58
- 阅读 ( 1598 )
平衡方程(balanced equation)和净离子方程(net ionic equation)的区别
...的净反应。 内容1。概述和主要区别2。等式3是平衡的。什么是净离子方程式。并列比较-平衡方程式与净离子方程式5。摘要 什么是平衡方程式(a balanced equation)? Chemical reacti*** are very important in understanding the behavior of a particular syst...
- 发布于 2020-10-20 16:30
- 阅读 ( 731 )
离子迁移率(ionic mobility)和离子速度(ionic velocity)的区别
...动是由外加的静电场引起的。 目录 1. 概述和主要区别 2. 什么是离子迁移率 3. 什么是离子速度 4. 并列比较-离子迁移率与离子速度的表格形式 5. 摘要 什么是离子迁移率(ionic mobility)? 离子迁移率或电迁移率是离子在电场作用下...
- 发布于 2020-10-21 22:29
- 阅读 ( 592 )
离子键合(ionic bonding)和金属键合(metallic bonding)的区别
离子键合和金属键合的关键区别在于,离子键合发生在正离子和负离子之间,而金属键合发生在正离子和电子之间。 正如美国化学家G.N.Lewis所说,当原子的价壳层中含有8个电子时,原子是稳定的。大多数原子的价壳层中的电...
- 发布于 2020-10-24 01:03
- 阅读 ( 856 )
离子型(ionic)和共价化合物(covalent compounds)的区别
...式可以被认为是离子化合物和共价化合物的关键区别。(离子键和共价键的区别)当离子键形成时,电子由金属捐赠,捐赠电子被非金属接受。由于静电的吸引,它们形成了一个牢固的键。两种非金属之间形成共价键。在共价键...
- 发布于 2020-10-24 16:55
- 阅读 ( 494 )
氢键(hydrogen bond)和离子键(ionic bond)的区别
氢键和离子键的关键区别在于,永久性阴阳离子之间存在离子键,而部分正电荷和部分负电荷之间存在氢键。 化学键把原子和分子结合在一起。键在决定分子和原子的化学和物理行为方面很重要。正如美国化学家G.N.Lewis提出...
- 发布于 2020-11-03 00:45
- 阅读 ( 920 )