主要区别
碳正离子和碳负离子的主要区别在于碳正离子包含带正电荷的碳原子,而碳负离子包含带负电荷的碳原子。
碳阳离子(carbocation) vs. 碳负离子(carbanion)
碳正离子是一个带正电荷的碳原子的离子,而碳负离子是一个带负电荷的碳原子的离子。带正电荷的碳正离子的碳原子是sp2杂化的,而带负电荷的碳离子的碳原子是sp3杂化的。碳离子中碳原子的几何结构是三角平面的,而碳离子中碳原子的几何结构是金字塔形的。碳正离子的磁性是顺磁性的,相反碳负离子的磁性是反磁性的。在各种化学反应中,碳正离子起着电泳剂的作用;相反,在许多化学反应中,碳负离子起亲核剂的作用。碳正离子比碳负离子更稳定,因为存在三个施主甲基,它们提供电子,因此大大稳定了正电荷。碳正离子是一种缺电子的物种;另一方面,碳离子是一种富含电子的物种。碳正离子的中心碳原子在最外层有6个电子,而碳负离子的中心碳原子在最外层有8个电子。碳正离子可以极大地接受亲核分子的电子对以产生共价键,而碳负离子通常会将电子对捐赠给亲电试剂,以产生共价键。
比较图
什么是碳阳离子(carbocation)?
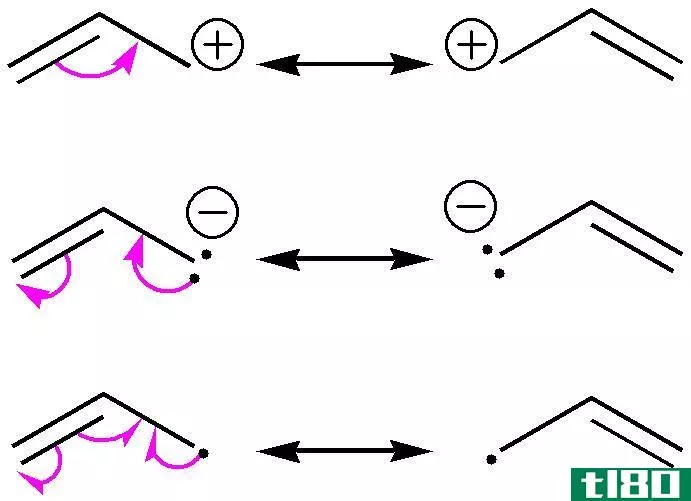
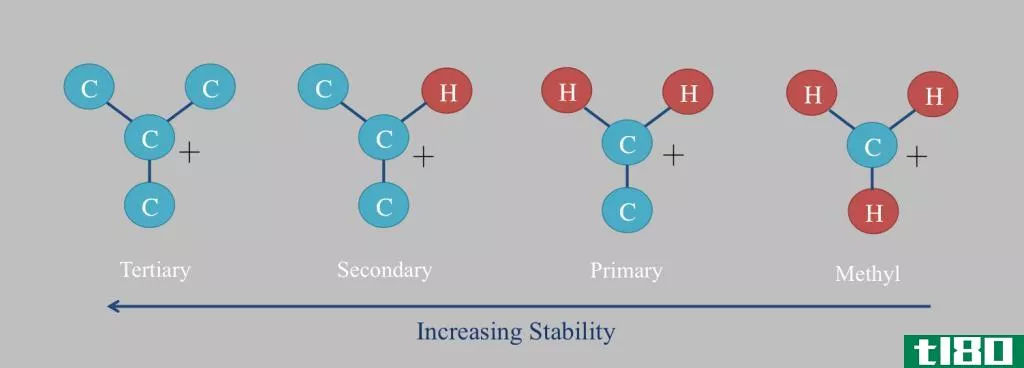
碳正离子通常被定义为中心碳原子带正电荷的离子。碳正离子通常是指整个分子,不仅代表带正电荷的碳原子,而且在其中心原子上可以有一个或多个正电荷。碳正离子通常是不稳定的,因为由于电子的损失,中心碳原子的p轨道是自由的。这就是为什么碳正离子很少或经常与其他离子发生反应,但这有利于碳正离子和亲核剂之间的反应,因为在各种化学反应中,碳正离子起着电泳剂的作用。但碳正离子比碳负离子更稳定,因为存在三个施主甲基,它们提供电子,因此大大稳定了正电荷。由于电子对不完全,碳阳离子的磁性是顺磁性的。典型的是,带有正电荷的碳阳离子的碳原子是sp2杂化的,因为一个碳原子的结构周围只能有三个键。碳正离子中碳原子的几何结构是三角平面的。碳阳离子的中心碳原子在最外层有6个电子。碳阳离子分为四类,与正电荷碳原子所依附的碳原子数一致。
碳阳离子类型
- 甲基碳阳离子
- 初级碳阳离子
- 二次碳阳离子
- 叔碳阳离子
什么是碳负离子(carbanion)?
碳负离子通常被定义为中心碳原子带负电的离子。带负电荷的中心碳原子是sp3杂化的。碳负离子中碳原子的几何构型除苄基碳负离子外均呈金字塔形。碳负离子的最外层有8个电子,这意味着它遵循八位元规则。这个八位元规则是通过从中性分子中移除带正电的原子或基团而形成的。在许多化学反应中,碳负离子几乎总是起亲核作用,并且容易与亲电试剂反应,形成共价键。碳负离子的磁性是由于电子结合的完成而具有反磁性的。被认为最小的碳负离子是“甲酰胺离子”,它是由失去质子的甲烷形成的。下面讨论四种主要类型的碳负离子。
碳负离子的类型
- 甲基碳负离子
- 伯碳负离子
- 二次碳负离子
- 叔碳负离子
主要区别
- 中心碳原子带正电荷的碳阳离子,而碳负离子的碳原子带负电荷。
- 碳正离子的碳原子是sp2杂化的,而带负电荷的碳原子是sp3
- 碳离子中碳原子的结构是三角平面的,而碳离子中碳原子的几何结构或结构是金字塔形的。
- 碳正离子的吸引力是顺磁性的,相反,碳负离子的磁性是反磁性的。
- 在各种化学反应中,碳正离子起着电泳剂的作用;相反,在许多化学反应中,碳负离子起亲核作用。
- 碳正离子变得比碳负离子更稳定,因为存在三个施主甲基,它们提供电子,因此大大稳定了正电荷。
- 碳正离子是一种缺电子的物种;另一方面,碳离子是一种富含电子的物种。
- 碳正离子的中心碳原子在最外层有6个电子,而碳负离子的中心碳原子在最外层有8个电子。
- 碳正离子可以很容易地接受亲核分子的一对电子来产生共价键,而碳负离子通常会将一个电子对捐赠给亲电试剂以产生共价键。
结论
以上讨论得出结论:碳正离子包含一个带正电荷的碳原子,它是一个缺电子的物种,而碳负离子包含一个带负电荷的碳原子和一个富含电子的物种。