吉布斯自由能和标准自由能的关键区别在于,吉布斯自由能取决于实验条件,而标准自由能描述的是处于标准状态的反应物和产物的吉布斯自由能。
吉布斯自由能和标准自由能是物理化学中常见的术语。这两个术语给出了一个几乎相似的概念,只是略有不同。吉布斯自由能和标准自由能的唯一区别在于它们的实验条件,如温度和压力。让我们详细谈谈这些条款。
目录
1. 概述和主要区别
2. 吉布斯自由能是多少
3. 什么是标准自由能
4. 并列比较-吉布斯自由能与标准自由能的表格形式
5. 摘要
什么是吉布斯自由能(gibbs free energy)?
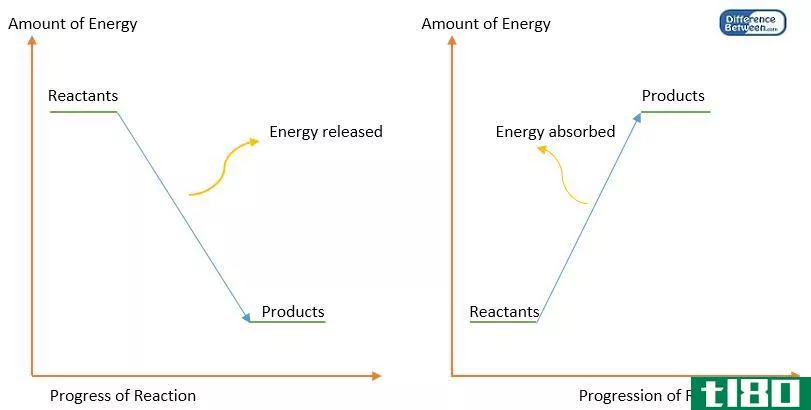
吉布斯自由能是一个热力学量,等于(系统或过程的)焓减去熵和绝对温度的乘积。这个符号是“G”。它把一个系统的焓和熵合成一个值。我们可以用“∆G”表示这个能量的变化。这种变化可以决定在恒温恒压下化学反应的方向。
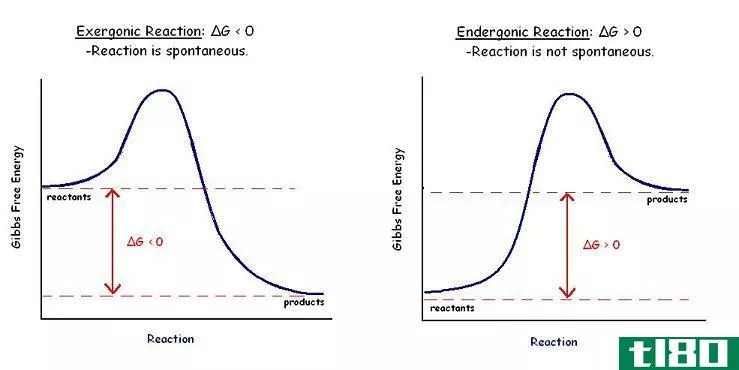
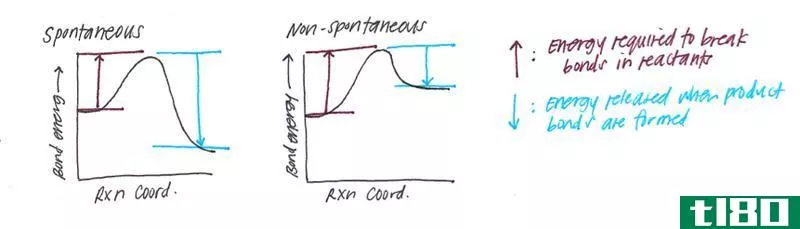
此外,如果∆G为正值,则为非自发反应,而∆G为负值表示自发反应。吉布斯自由能这个术语是由约西亚·威拉德·吉布斯(1870)提出的。该量的方程式如下:

图01:吉布斯自由能方程,其中G是吉布斯自由能,H是焓,T是绝对温度,S是熵
什么是标准自由能(standard free energy)?
标准自由能是在标准实验条件下给出吉布斯自由能的热力学量。这意味着,为了将热力学系统的能量命名为标准自由能,该系统的反应物和产物应处于标准状态。大多数情况下,遵循标准状态,都是适用的。
- 气体:1 atm分压
- 纯液体:在1大气压下的液体
- 溶质:有效浓度为1 M
- 固体:1大气压下的纯固体
通常,热力学系统的正常温度是298.15 K(或25°C),因为我们在这个温度下做实验。但准确的标准温度是273 K(0°C)。
吉布斯自由能(gibbs free energy)和标准自由能(standard free energy)的区别
吉布斯自由能是一个热力学量,等于(系统或过程的)焓减去熵和绝对温度的乘积。更重要的是,我们根据实验的实际温度和压力来计算这个量。标准自由能是在标准实验条件下给出吉布斯自由能的热力学量。这就是吉布斯自由能和标准自由能之间的关键区别。虽然标准自由能与吉布斯自由能的概念相似,但我们只计算了反应物和产物处于标准状态的热力学系统。

总结 - 吉布斯自由能(gibbs free energy) vs. 标准自由能(standard free energy)
吉布斯自由能和标准自由能在热力学中描述了几乎相似的概念。吉布斯自由能和标准自由能的区别在于,吉布斯自由能取决于实验条件,而标准自由能描述的是处于标准状态的反应物和产物的吉布斯自由能。