分子间键与分子内键的区别
氢键是某些极性分子之间的一种吸引力。它是一种比离子键或共价键弱的键,但与偶极-偶极力和范德华力相比,它是一种强大的引力。如果极性分子有一个强负电性原子,它有一个单独的电子对(可以作为电子供体)与氢原子(电子受体)结合,就会形成氢键。由于强电负性原子比氢原子能吸引键电子par朝向自己,氢原子得到部分正电荷,从而产生强烈的电荷分离。因此,常见的氢键形成化学键是O-H键、N-H键和F-H键。有两种形式的氢键可以形成:极性分子之间的分子间氢键和发生在同一单分子中的分子内氢键。分子间氢键和分子内氢键的关键区别在于,分子间氢键发生在两个分子之间,而分子内氢键发生在单个分子中。
目录
1. 概述和主要区别
2. 什么是分子间氢键
3. 什么是分子内氢键
4. 并列比较-分子间氢键与分子内氢键的表格形式
5. 摘要
什么是分子间氢键(intermolecular hydrogen bonding)?
分子间氢键发生在物质中不同分子之间。因此,电子给体和电子受体应该存在于两个独立的分子中。如果有合适的电子给体和受体,任何分子都能形成氢键。

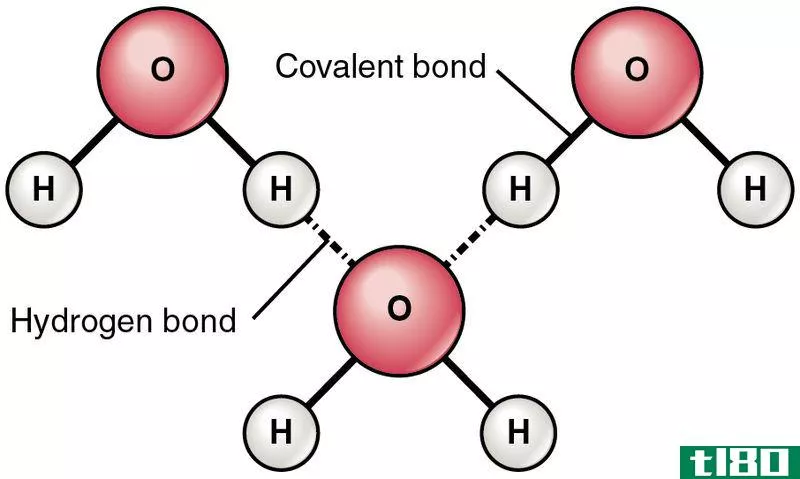
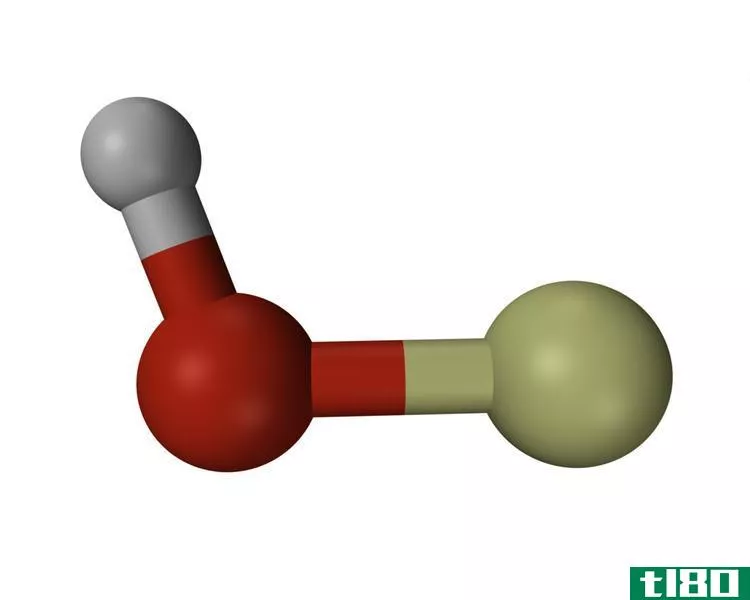
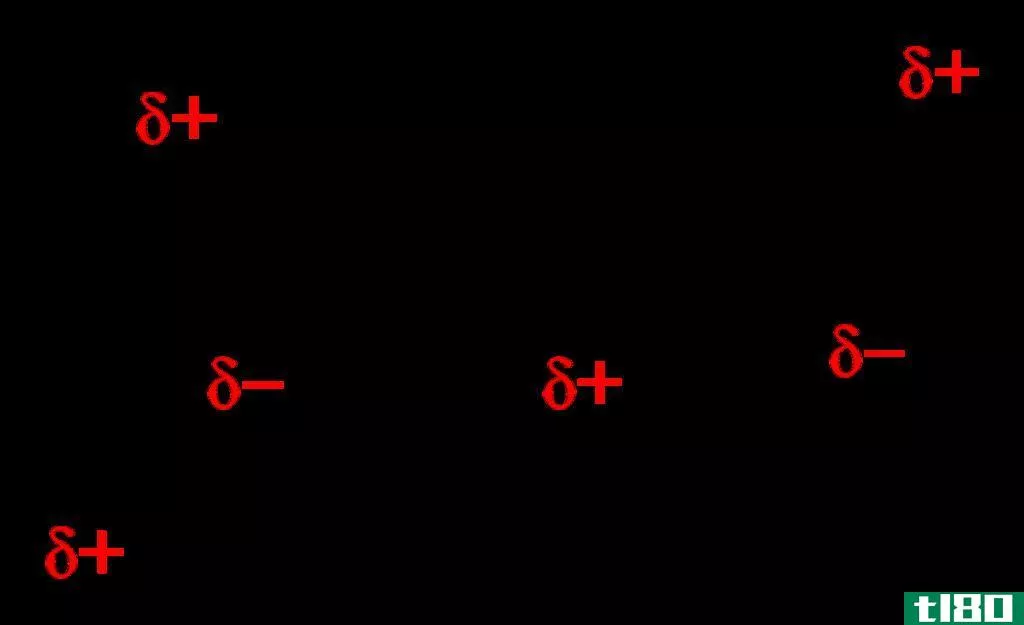
图01:水分子中的分子间氢键
可以形成分子间氢键的一个常见例子是水分子(H2O),当液态水转化为固体冰时,水分子之间的氢键会导致刚性结构的形成。
什么是分子内氢键(intramolecular hydrogen bonding)?
分子内氢键是指发生在单个分子内的氢键分子。这个当同一个单分子中存在两个能相互形成氢键的官能团时,就会产生氢键。这意味着电子给体和电子受体应该存在于同一分子中。

图02:水杨醛分子内氢键
此外,这两个官能团的位置应该足够接近这个氢键。显示这种氢键的分子最常见的例子是水杨醛(C7H6O2)。
分子间(intermolecular)和分子内氢键(intramolecular hydrogen bonding)的区别
| 分子间氢键与分子内氢键 | |
| 分子间氢键发生在物质中不同分子之间。 | 分子内氢键是指发生在单个分子内的氢键。 |
| 组件 | |
| 两个分子之间形成分子间氢键。 | 分子内的氢键是在不同的分子之间形成的。 |
总结 - 分子间(intermolecular) vs. 分子内氢键(intramolecular hydrogen bonding)
氢键是偶极-偶极相互作用的一种形式。但它是弱键型。氢键有两种形式:分子间氢键和分子内氢键。分子间氢键和分子内氢键的区别在于,分子间氢键发生在两个分子之间,而分子内氢键发生在单个分子中。
引用
1.“氢键”,化学歌词,歌词,2016年7月21日。此处提供2.“氢键”,维基百科,维基媒体基金会,2018年3月14日。此处提供
2.“氢键”,维基百科,维基媒体基金会,2018年3月14日。