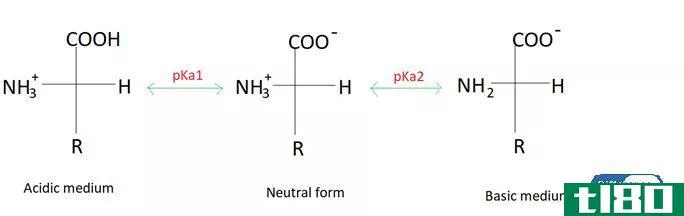
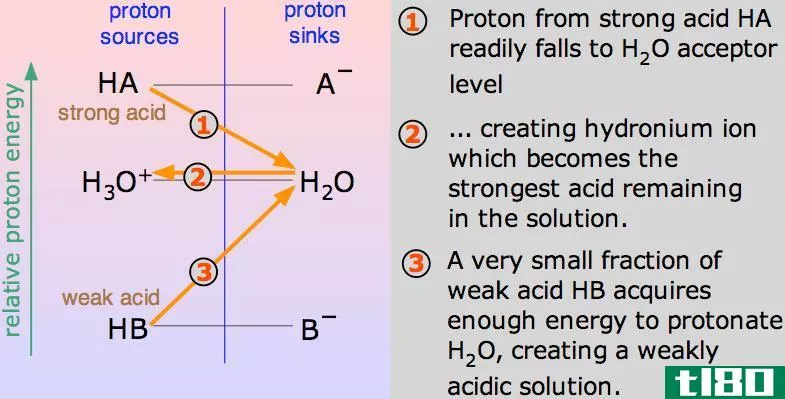
pH与pKa
我们通常认为酸是质子供体。酸有酸味。酸橙汁和醋是我们在家里遇到的两种酸。它们与产生水的碱反应,并与金属反应生成氢气,从而增加金属腐蚀速率。提供质子的能力是一种酸的特征,pH,PKa值是根据这个特性计算的。
酸碱度
pH是一个刻度,可以用来测量溶液的酸碱度。量表有1到14之间的数字。pH7被视为中性值。据说纯净水的pH值是7。在pH标度中,代表1-6种酸。根据酸分解和产生质子的能力,酸可以分为两类。像HCl,HNO3这样的强酸在溶液中完全电离产生质子。像CH3COOH这样的弱酸会部分离解,产生更少的质子。一种pH值为1的酸被认为是非常强的,随着pH值的增加,酸度降低。因此,pH值大于7表示碱度。随着碱度的增加,pH值也会增加,强碱的pH值为14。
pH值是对数的。关于溶液中H+的浓度,可以写如下。
pH=-log[H+]
在基本解中,不存在任何H+s。因此,在这种情况下,pOH可以由–log[OH–]值确定。
因为,pH+pOH=14;也可以计算碱性溶液的pH值。实验室有pH计和pH纸,可直接测量pH值。pH试纸将给出近似的pH值,而pH计给出更精确的数值。
pKa公司
酸性是一种酸的状态。这与酸的存在程度有关。根据酸分解和产生质子的能力,酸可以分为两类。像HCl,HNO3这样的强酸在溶液中完全电离,产生质子。像CH3COOH这样的弱酸会部分离解,产生更少的质子。Ka是酸分解常数。它表明了弱酸失去质子的能力。在水介质中,弱酸与其共轭碱处于平衡状态,如下例所示。
CH3COOH(水)+水(l)CH3COO–(aq)+H3O+(aq)
上述平衡可以写成,
E=[CH3COO-][H3O+]/[CH3COOH][H2O]
将该常数改为酸离解常数,可将该方程改写如下。
Ka=[CH3COO–][H3O+]/[CH3COOH]
Ka对数值的倒数就是pKa值。这是酸度的另一种表达方式。
pKa=-log千安
对于强酸,Ka值较大,pKa值较小。而对于弱酸,情况恰恰相反。
| pH值和pKa有什么区别?•pH是H+浓度对数的倒数。pKa是Ka值的对数。•pH给出了介质中H+离子数量的概念。pKa值给出了平衡偏向哪一边(酸离解程度)的概念。•pH和pKa都由Henderson-Hasselbalch方程关联:pH=pKa+log([A-]/[HA]) |