自由能(free energy)和活化能(activation energy)的区别
自由能和活化能之间的关键区别在于,自由能是热力学系统进行热力学工作可用的能量量,而化学反应的活化能是为了从反应中获得产物而必须克服的能量屏障。
自由能和活化能是两个应用不同的术语。自由能一词用于物理化学中的热力学系统,而活化能一词主要用于生物化学中的化学反应。
目录
1. 概述和主要区别 2. 什么是自由能 3. 什么是活化能 4. 并列比较-自由能与活化能的表格形式 5. 摘要
什么是自由能(free energy)?
自由能是热力学系统进行热力学功的可用能量。自由能具有能量的维度。热力学系统的自由能值是由系统的当前状态决定的,而不是由它的历史决定的。热力学中经常讨论的自由能主要有两种:亥姆霍兹自由能和吉布斯自由能。
亥姆霍兹自由能是在一个封闭的热力学系统中,在恒定的温度和体积下进行热力学工作的能量。因此,亥姆霍兹能的负值表示热力学系统通过保持其体积常数所能做的最大功。为了保持体积不变,一些总的热力学功作为边界功(保持系统的边界不变)。
吉布斯自由能是在一个封闭的热力学系统中,在恒定的温度和压力下进行热力学工作的能量。系统的容量可能会有所不同。自由能用G表示。
什么是活化能(activation energy)?
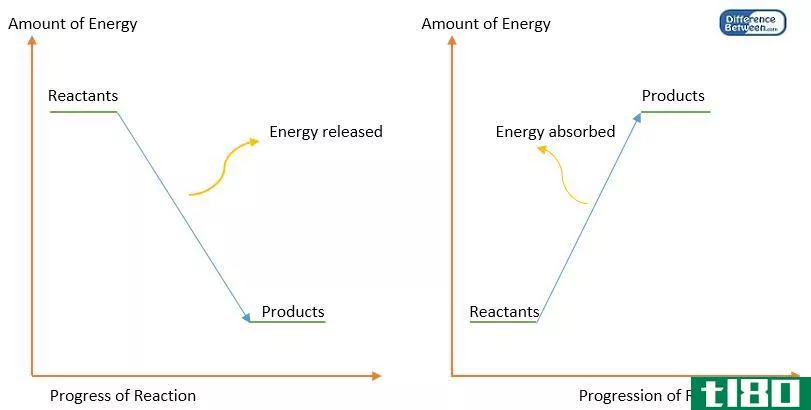
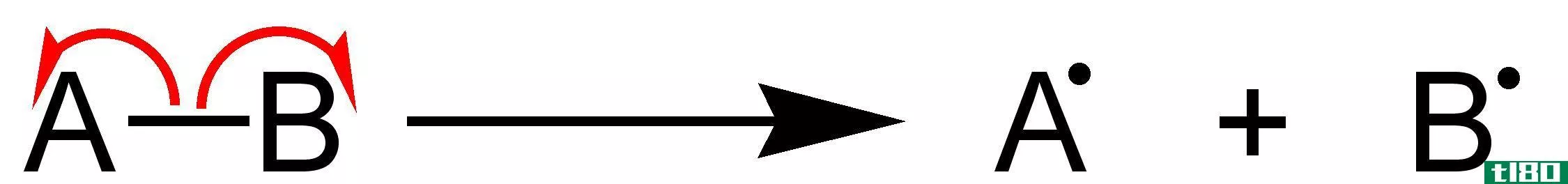
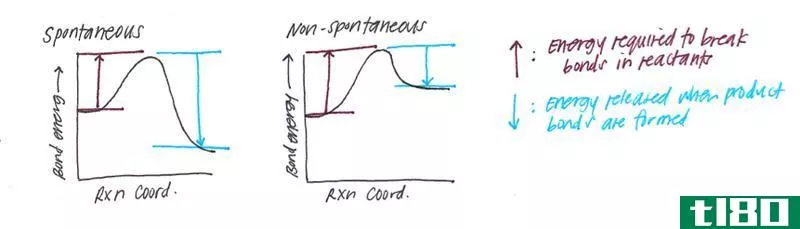
化学反应的活化能是为了从反应中获得产物而必须克服的能量屏障。换句话说,它是反应物转化为产物所需的最小能量。为了开始化学反应,总是需要提供活化能。
我们用Ea或AE表示活化能;此外,活化能被认为是化学反应中形成具有最高势能的中间体所需的最小能量。有些化学反应进展缓慢,通过两个或多个步骤进行。在这里,中间体形成,然后重新排列形成最终产品。因此,开始该反应所需的能量是形成具有最高势能的中间体所需的能量。

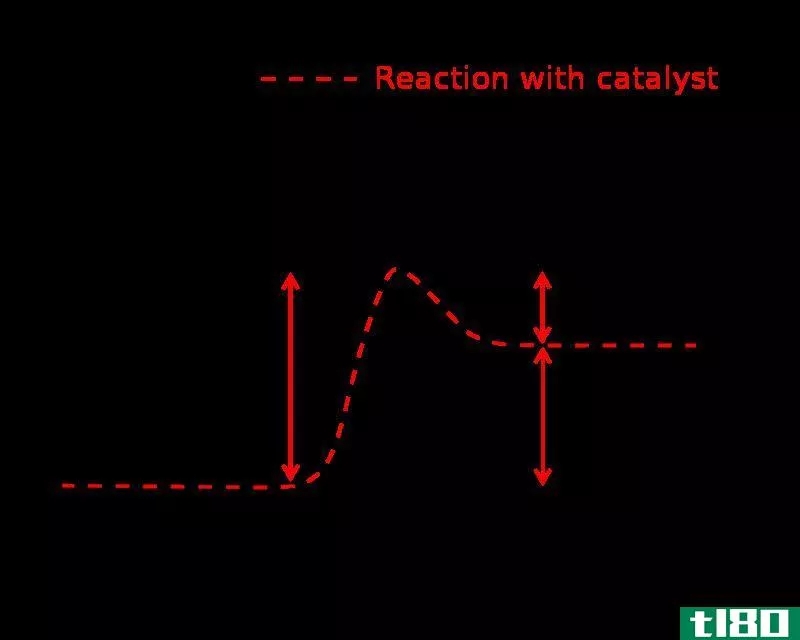
此外,催化剂可以降低活化能。因此,人们经常使用催化剂来克服能量障碍,使化学反应得以进行。酶是一种生物催化剂,可以降低组织中发生的反应的活化能。
自由能(free energy)和活化能(activation energy)的区别
自由能和活化能是两个应用不同的术语。自由能和活化能之间的关键区别在于,自由能是热力学系统进行热力学工作可用的能量量,而化学反应的活化能是为了从反应中获得产物而必须克服的能量屏障。
下面以表格形式总结了自由能和活化能之间的区别。

总结 - 自由能(free energy) vs. 活化能(activation energy)
自由能和活化能是两个应用不同的术语。自由能和活化能之间的关键区别在于,自由能是热力学系统进行热力学工作可用的能量量,而化学反应的活化能是为了从反应中获得产物而必须克服的能量屏障。
引用
- 发表于 2021-07-14 04:43
- 阅读 ( 2160 )
- 分类:科学
你可能感兴趣的文章
键能(bond energy)和键焓(bond enthalpy)的区别
...例如,甲烷分子(CH4)的键能是形成一个碳原子和4个氢自由基所需的能量。然后取每个C-H键的键离解能之和除以4,即可计算出C-H键的键能。 例:水分子中O-H键的键能可计算如下。 打破氢键所需的能量=498.7 kJ/mol 打破O-H键所需的...
- 发布于 2020-09-24 09:39
- 阅读 ( 882 )
晶场稳定能(crystal field stabilization energy)和分裂能(splitting energy)的区别
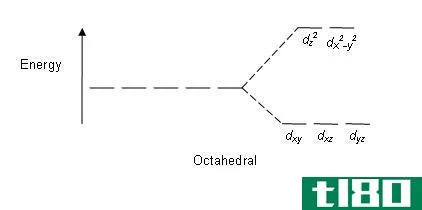
晶场稳定能与分裂能的关键区别在于,晶场稳定能是指配体的电子组态能与各向同性场的电子组态能之差。同时,晶体场分裂能是指配体的d轨道之间的能量差。 晶体场稳定能和分裂能是晶体场理论中的两个术语。晶体场理论...
- 发布于 2020-10-14 04:30
- 阅读 ( 628 )
动能(kinetic energy)和活化能(activation energy)的区别
动能和活化能之间的关键区别在于,动能是物体运动时所具有的能量类型,而活化能是为了从反应中获得产物而必须克服的能量屏障。 能量是在物理系统中执行工作的能力。“功”是指移动物体对抗力的动作。根据能量守恒...
- 发布于 2020-10-15 00:52
- 阅读 ( 718 )
活化能(activation energy)和阈值能量(threshold energy)的区别
活化能与阈能的关键区别在于,活化能描述了反应物与活化络合物之间的势能差,而阈能则描述了反应物成功碰撞形成活化络合物所需的能量。 精力是工作的能力。如果有足够的能量,我们可以用它来做一些我们想要的工作...
- 发布于 2020-10-17 18:57
- 阅读 ( 349 )
吉布斯自由能(gibbs free energy)和标准自由能(standard free energy)的区别
吉布斯自由能和标准自由能的关键区别在于,吉布斯自由能取决于实验条件,而标准自由能描述的是处于标准状态的反应物和产物的吉布斯自由能。 吉布斯自由能和标准自由能是物理化学中常见的术语。这两个术语给出了一...
- 发布于 2020-10-18 00:01
- 阅读 ( 444 )
均裂的(homolytic)和异溶键离解能(heterolytic bond dissociation energy)的区别
...键所需的能量。化学键的溶血是键的对称断裂,形成两个自由基,而不是两个离子。在这里,原子间的键电子被分成两半,由两个原子占据。例如,每一个不裂解的自由基都有一个不裂解的自由基。 图1:均分解 键离解能是指在...
- 发布于 2020-10-19 07:36
- 阅读 ( 337 )
晶格能(lattice energy)和水化能(hydration energy)的区别
关键区别-晶格能与水化能 晶格能和水化能是热力学中两个相关的术语。晶格能是晶格形成时释放的能量。水化能是晶格在水中溶解时释放的能量。晶格的形成和水合都会释放能量,因为这两个过程都涉及化学键(或化学相互...
- 发布于 2020-10-19 07:40
- 阅读 ( 626 )
自由能(free energy)和焓(enthalpy)的区别
关键区别-自由能与焓 自由能和焓是两个热力学术语,用来解释热能与热力学系统中发生的化学反应之间的关系。自由能或热力学自由能是一个热力学系统能做的功的量。换言之,自由能是热力学系统中进行热力学功的可用能...
- 发布于 2020-10-19 11:40
- 阅读 ( 613 )
溶剂化能(solvation energy)和晶格能(lattice energy)的区别
...吉布斯能时,溶剂化才是可能的(自发的)。因此,Gibbs自由能应为负值(溶液形成后体系的Gibbs自由能应降低)。溶剂化包括不同的步骤和不同的能量。 Formation of a cavity of solvent to make space for solutes. This is thermodynamically unfavourab...
- 发布于 2020-10-20 03:46
- 阅读 ( 782 )
键能(bond energy)和键离解能(bond dissociation energy)的区别
...423 kJ/mol和339 kJ/mol,这是因为第一个键断裂通过均裂形成自由基物种,因此第二个键断裂发生在自由基物种上,比第一个需要更多的能量。同样,键离解能也会一步一步地改变。 键能(bond energy)和键离解能(bond dissociation energy)的区...
- 发布于 2020-10-21 13:16
- 阅读 ( 771 )