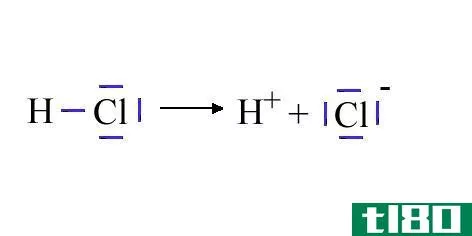酸性盐和碱性盐的主要区别在于,酸性盐溶于水时形成的溶液pH值小于7.0,而碱性盐溶于水时形成的溶液pH值高于7.0。
盐是一种含有阳离子和阴离子的离子化合物。它是一种固体化合物,没有净电荷,因为阳离子和阴离子相互结合,使阳离子的电荷与阴离子的电荷平衡。根据盐的离子组成,可以确定其性质和反应性。因此,我们可以将一种盐分为酸性盐、碱性盐和中性盐三类。
目录
1. 概述和主要区别
2. 什么是酸性盐
3. 什么是碱性盐
4. 并列比较-酸性盐和碱性盐的表格形式
5. 摘要
什么是酸性盐(an acidic salt)?
酸性盐是一种离子化合物,在水中溶解后,可以形成酸性溶液。这意味着,酸性盐形成一个小于pH 7.0的水溶液。这可能是由于金属阳离子的存在,它可以作为路易斯酸反应,或者是由于存在水解质子。最常见的是,酸性盐含有可水解的质子。这些水解的质子可能存在于阳离子或阴离子中。
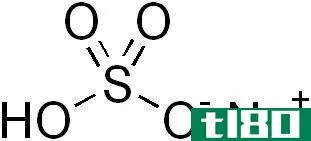
图01:亚硫酸氢钠是一种酸性盐
阳离子中可水解质子
含有阳离子和可水解质子的酸性盐主要是铵离子。铵离子来源于铵盐。此外,这些可水解的质子可以出现在含有质子化胺基的有机化合物中。E、 铵离子、甲基铵离子、乙基铵离子、苯胺离子等。
阴离子中可水解质子
酸性盐可能含有阴离子中可水解的质子。例如亚硫酸氢离子、柠檬酸二氢根、生物xate离子等。这些阴离子含有弱分解成水的质子。
什么是碱性盐(a basic salt)?
碱性盐是离子化合物,在水中溶解时能形成碱性溶液。也就是说,这些盐可以形成pH值高于7.0的水溶液。一般来说,碱性盐能使水分子脱质子,形成氢氧化离子,从而导致水溶液中的碱性。

图02:硫化钠是一种碱性盐
一些基本盐的例子包括碳酸氢钠、碳酸钙、醋酸钠、氰化钾和硫化钠。这些盐可以与水反应,迫使水分子去除氢氧化物离子。
酸性盐(acidic salt)和碱性盐(basic salt)的区别
酸性盐和碱性盐的主要区别在于,酸性盐溶于水时形成的溶液pH值小于7.0,而碱性盐溶于水时形成的溶液pH值高于7.0。铵盐、亚硫酸氢钠和草酸钙是一些酸性盐的例子,而碳酸氢钠、碳酸钙、乙酸钠、氰化钾和硫化钠是一些碱性盐的例子。
下面的信息图总结了酸性盐和碱性盐的区别。

总结 - 酸性盐(acidic salt) vs. 碱性盐(basic salt)
根据盐的离子组成,可以确定其性质和反应性。因此,我们可以把一种盐分为三类:酸性盐、碱性盐和中性盐。酸性盐和碱性盐的主要区别在于,酸性盐溶于水时形成的溶液pH值小于7.0,而碱性盐溶于水时形成的溶液pH值高于7.0。
引用
1《盐类的酸碱特性》《无限化学》流明,
2“7.8:盐的酸碱性质。”化学歌词,歌词,2019年6月3日,
三。“酸盐”,维基百科,维基媒体基金会,2019年10月17日,