利用键能求焓变
你可以用键能来计算化学反应的焓变。这个示例问题说明了该怎么做。

回顾
在开始之前,您可能希望复习热化学定律以及吸热和放热反应。单键能量表可以帮助您。
焓变问题
估算以下反应的焓变化ΔH:
H2(g)+Cl2(g)→ 2盐酸(克)
解决方案
要解决此问题,请按照简单步骤考虑反应:
步骤1:反应物分子H2和Cl2分解成原子。
H2(g)→ 2小时(克)氯2小时(克)→ 2 Cl(g)
步骤2:这些原子结合形成HCl分子。
2小时(克)+2毫升(克)→ 2盐酸(克)
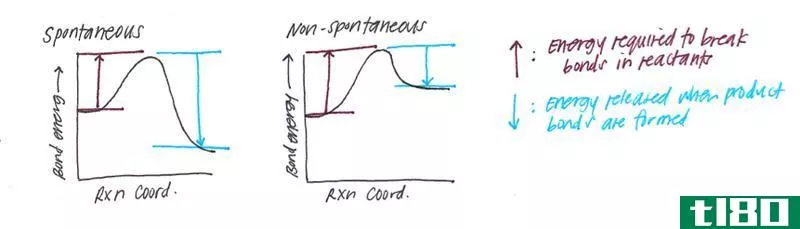
在第一步中,H-H和Cl-Cl键被破坏。在这两种情况下,一摩尔的键都断裂了。当我们查找H-H和Cl-Cl键的单键能量时,我们发现它们分别为+436 kJ/mol和+243 kJ/mol,因此对于反应的第一步:
ΔH1=+(436 kJ+243 kJ)=+679 kJ
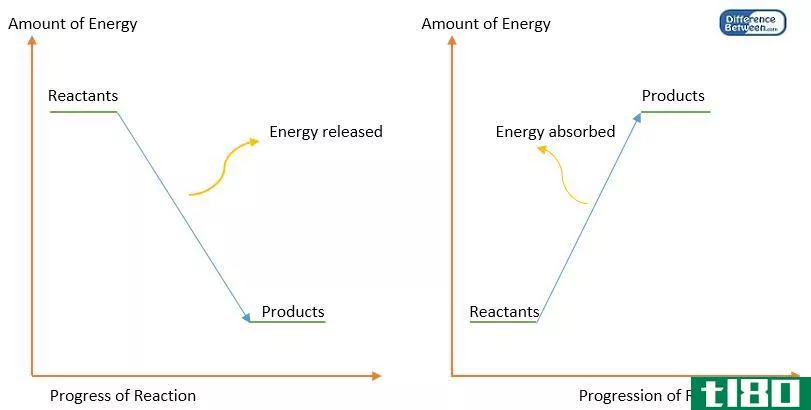
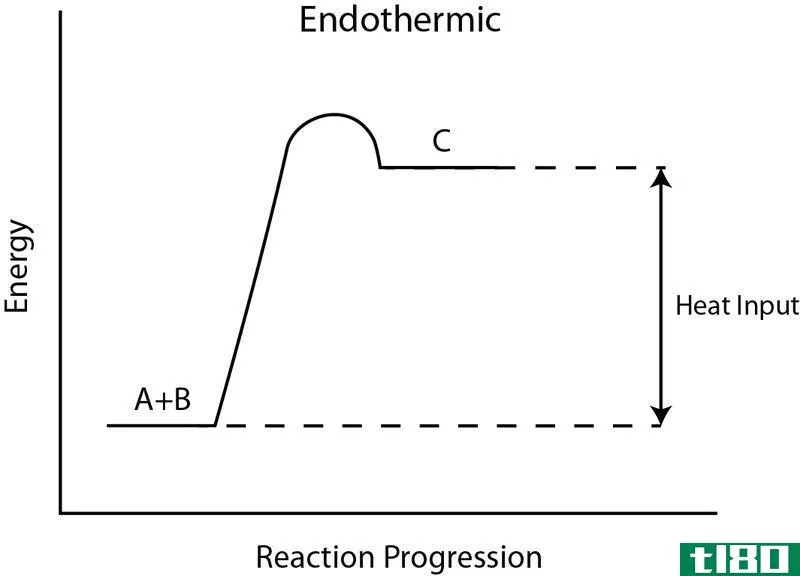
键断裂需要能量,因此我们预计该步骤的ΔH值为正值。
在反应的第二步,形成了两摩尔的H-Cl键。键断裂释放能量,因此我们预计这部分反应的ΔH为负值。使用该表,发现一摩尔H-Cl键的单键能量为431 kJ:
ΔH2=-2(431 kJ)=-862 kJ
应用赫斯定律,ΔH=ΔH1+ΔH2
ΔH=+679千焦-862千焦ΔH=-183千焦
回答
反应的焓变为ΔH=-183 kJ。
- 发表于 2021-09-15 09:49
- 阅读 ( 150 )
- 分类:化学
你可能感兴趣的文章
键能(bond energy)和键焓(bond enthalpy)的区别
关键区别-键能与键焓 键能和键焓都描述了同一个化学概念:将一摩尔分子分解成其组成原子所需的能量。它测量化学键的强度。所以也叫粘结强度。键能计算为气相化学物质在298K下的键离解能的平均值。键能和键焓这两个...
- 发布于 2020-09-24 09:39
- 阅读 ( 875 )
键焓(bond enthalpy)和晶格焓(lattice enthalpy)的区别
...可以将其命名为键离解能。其他同义词包括键强度和平均键能。 图01:一些化学键的键能 如果键的焓值很高,说明键很强,很难分解。因此,它需要更多的能量来分解这种特殊的键。通常,我们用来确定键焓值的单位是kcal/mol(...
- 发布于 2020-10-15 02:15
- 阅读 ( 435 )
键能(bond energy)和键离解能(bond dissociation energy)的区别
键能和键离解能的关键区别在于键能是一个平均值,而键离解能是一个特定键的特定值。 正如美国化学家G.N.Lewis提出的那样,当原子的价壳层中含有8个电子时,原子是稳定的。大多数原子的价壳层中的电子少于8个(周期表...
- 发布于 2020-10-21 13:16
- 阅读 ( 766 )
吸热的(endothermic)和放热反应(exothermic reactions)的区别
...能量。在吸热反应中,反应物的键断裂能大于产物的总成键能。因此,焓变为正值,反应不是自发的。因此,对于吸热反应,我们必须从外部提供能量。 例如,当氯化铵溶解在水中时,烧杯会变冷,因为溶液会吸收外界环境的...
- 发布于 2020-11-05 08:34
- 阅读 ( 1527 )
键能(bond energy)和键离解能焓(bond dissociation energy enthalpy)的区别
键能与键离解能(焓) 键能是存在于相同类型原子之间的气相键离解能(通常在298 K的温度下)的平均值。然而,键能和键离解能是不一样的。键离解能是共价键(也称为分子键,是两个非金属原子之间的化学键,涉及这些原子...
- 发布于 2021-06-26 10:13
- 阅读 ( 461 )
离子共价(ionic covalent)和金属键(metallic bonds)的区别
...。二次键包括色散键、偶极键和氢键。一次键具有较高的键能,与二次力相比,它更稳定。离子共价键与金属键的主要区别在于它们的形成;当一个原子向另一个原子提供电子时,离子键形成,而当两个原子在金属晶格**享可变...
- 发布于 2021-06-28 11:41
- 阅读 ( 808 )
键能(bond energy)和键离解能(bond dissociation energy)的区别
主差键能(main difference bond energy) vs. 键离解能(bond dissociation energy) 键能和键离解能这两个术语常常令人困惑,因为它们都与两个原子间化学键的断裂有关。键能和键离解能的概念通常用于共价键。这是因为共价键不同于离...
- 发布于 2021-06-28 18:45
- 阅读 ( 448 )
吸热的(endothermic)和放热反应(exothermic reactions)的区别
...吸热反应和放热反应,我们可以计算反应物和产物之间的焓变。如果没有,我们可以观察反应混合物的温度变化。吸热反应和放热反应的主要区别在于,吸热反应从周围吸收能量,而放热反应向周围释放能量。 覆盖的关键领域 1...
- 发布于 2021-06-29 08:53
- 阅读 ( 1291 )
常见的一般化学问题列表
...方程式教程 玻尔原子能级 玻尔原子能量变化 沸点升高 键能和焓 键极性 波义耳定律 波义耳气体定律 c:量热法和;流向d的热流:来自原料转化的稀释 量热法和热流法 碳-14年代测定 摄氏度到开尔文温度的转换 查尔斯气体定...
- 发布于 2021-09-08 10:26
- 阅读 ( 248 )
冰对水蒸气的焓变
这个焓变示例问题是当冰的状态从固态转变为液态水,最后转变为水蒸气时的焓变。 焓回顾 在开始之前,您可能希望复习热化学定律以及吸热和放热反应。 问题 给出:冰的熔化热为333 J/g(即当1克冰融化时,333 J被吸收...
- 发布于 2021-09-15 09:46
- 阅读 ( 191 )