反应实例问题的熵
这个示例问题演示了如何从反应物和产物的标准摩尔熵数据中找到反应熵。熵是指化学反应前后熵水平的变化。本质上,它反映了系统中无序或随机性的数量是由于反应而增加还是减少。

标准摩尔熵变问题
下列反应的标准摩尔熵变是多少?
4 NH3(g)+5 O2(g)→ 4个NO(g)+6个H2O(g):S°NH3=193 J/K·摩尔O2=205 J/K·摩尔NO=211 J/K·摩尔H2O=189 J/K·摩尔
(注意,在这类问题中,你要么得到反应物和产物的摩尔熵值,要么需要在表格中查找。)溶液一个反应的标准摩尔熵的变化可以通过产物的摩尔熵之和与反应物的摩尔熵之和之间的差值来发现。ΔS°反应=∑npS°产物-∑nrS°反应物ΔS°反应=(4 S°NO+6 S°H2O)-(4 S°NH3+5 S°O2)ΔS°反应=(4(211 J/K)+6(189 J/K·mol)-(4(193 J/K·mol)+5(205 J/K·mol))ΔS°反应=(844 J/K·K+1134 J/K·mol)-(772 J/K·mol+1025 J/K·mol)ΔS°反应=1978 J/K·mol-1797 J/K·mol)ΔS°反应=181 J/K·mol我们可以使用本示例问题中介绍的技术检查我们的工作。反应涉及所有气体,产物的摩尔数大于反应物的摩尔数,因此熵的预期变化应为正。
答复
反应的标准摩尔熵变为181j/K·mol。
- 发表于 2021-09-26 06:05
- 阅读 ( 191 )
- 分类:科学
你可能感兴趣的文章
自由能(free energy)和焓(enthalpy)的区别
...个热力学术语,用来解释热能与热力学系统中发生的化学反应之间的关系。自由能或热力学自由能是一个热力学系统能做的功的量。换言之,自由能是热力学系统中进行热力学功的可用能量。另一方面,焓是一个热力学量,代表...
- 发布于 2020-10-19 11:40
- 阅读 ( 609 )
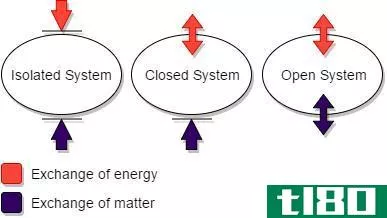
孤立系统(isolated system)和封闭系统(closed system)的区别
...分是“周围”。例如,一个系统可以是一个有机体,一个反应容器,甚至是一个细胞。在一个系统和周围环境之间有一个边界。边界定义了系统的范围。有时,物质和能量通过这些边界交换。此外,我们可以将系统分为两类:开...
- 发布于 2020-10-28 02:59
- 阅读 ( 1527 )
焓(enthalpy)和熵(entropy)的区别
...都是围绕着系统。焓和熵是描述系统和周围环境中发生的反应的两个术语。焓和熵都是热力学态函数。 目录 1.概述和主要区别 2. 什么是焓 3. 什么是熵 4. 并列比较-表格式的焓与熵 5. 摘要 什么是焓(enthalpy)? 当一个反应发生时,...
- 发布于 2020-11-04 20:59
- 阅读 ( 1860 )
疏水的(hydrophobic)和亲水分子(hydrophilic molecules)的区别
...分子之间的氢键被分解,为团块腾出空间。这是一个吸热反应,因为化学键被分解。此外,团块的形成使系统的熵减小。 根据热力学关系式, ΔG=ΔH–T型ΔS 在哪里?ΔG是吉布斯自由能 ΔH是焓的变化 T是温度 ΔS是熵的变化。 当...
- 发布于 2021-06-29 14:28
- 阅读 ( 288 )
等熵(isentropic)和绝热的(adiabatic)的区别
...程中的能量仅作为功传递给周围环境。某些具有一定化学反应的系统可以近似地认为是绝热系统,因为这些反应发生得很快,没有给它足够的时间向外释放能量或从外界获得能量。 等熵和绝热的相似性 两者都是热力学过程。 ...
- 发布于 2021-06-29 21:23
- 阅读 ( 711 )
自发的(spontaneous)和非自发性反应(nonspontaneous reactions)的区别
自发的主要差异(main difference spontaneous) vs. 非自发性反应(n***pontaneous reacti***) 自发反应和非自发反应是环境中可能发生的两类化学反应。自发反应在给定的条件下自行发生。然而,应该为非自发反应提供能量。对于自发反应,吉...
- 发布于 2021-06-29 21:57
- 阅读 ( 697 )
化学中的标准摩尔熵定义
...关于标准摩尔熵的基础知识,以及如何使用它来预测化学反应。 关键收获:标准摩尔熵 标准摩尔熵定义为标准状态条件下一摩尔样品的熵或随机度。 标准摩尔熵的常用单位为焦耳/摩尔开尔文(J/mol·K)。 正值表示系统的...
- 发布于 2021-09-15 10:47
- 阅读 ( 1131 )
日常生活中的有机化学实例
...合物的研究,它扩展到了解生物体及其衍生产品中的化学反应。在日常生活中有许多有机化学的例子。 他们就在我们身边 以下是工作中的有机化学示例: 聚合物由长链和分子分支组成。你每天遇到的常见聚合物是有机分...
- 发布于 2021-09-15 10:54
- 阅读 ( 172 )
科学中的焓变定义
焓变大约等于化学反应中用于断裂键的能量与在反应中形成新化学键所获得的能量之差。它描述了系统在恒定压力下的能量变化。焓变化用ΔH表示。在恒定压力下,ΔH等于系统的内能加上系统对其周围环境所做的压力-体积功。 ...
- 发布于 2021-09-15 16:34
- 阅读 ( 273 )
化学性质定义及实例
化学性质是物质发生化学变化或反应时可以观察到的特性或行为。化学性质可以在反应过程中或反应后观察到,因为样品中的原子排列必须被破坏,才能对性质进行研究。这与物理性质不同,物理性质是可以在不改变试样化学...
- 发布于 2021-09-15 16:42
- 阅读 ( 313 )