主要区别
电解质和非电解质的主要区别在于电解质是在溶液中具有电离能力的化合物,而非电解质是在溶液中不具有电离能力的化合物。
电解质(electrolytes) vs. 非电解质(nonelectrolytes)
电解质是在水溶剂中完全电离成离子的化合物,而非电解质是在水溶剂中不电离成离子的化合物。在电解质溶液中导电是可能的;另一方面,在非电解质溶液中不可能导电。电解质是由弱键组成的化合物,而非电解质是由强键组成的化合物。
电解液化合物中存在电价键;另一方面,非电解质化合物中存在共价键。电解质通常包括在电价化合物中;另一方面,非电解质也包括在共价化合物中。碱、酸和盐称为电解质;另一方面,碳水化合物、脂肪、脂类、糖和有机化合物称为非电解质。
电解质进一步分为两类,而非电解质则不进一步分为两类。极性化合物称为电解质;另一方面,非极性化合物称为非电解质。
电解质的熔融形式是可电离的;从另一方面讲,非电解质的熔融形式是不可电离的。用于标准电极电位识别的电解液;另一方面,非电解液不用于标准电极电位的识别。电解液的导电性随电解槽温度的升高而增大;另一方面,非电解质的电流传导与温度无关。
电解液中的键很弱,在电流传导过程中很容易断裂;另一方面,电解液中的键是一种很强的键,在电流的传导过程中不会断裂。电解质有能力完全溶解在溶液中;另一方面,非电解质没有完全溶解在溶液中的能力。
电解质可以分解成正离子和负离子;另一方面,非电解质不会分解成正离子和负离子。电解质不包括纯水;相反,非电解质也包括纯水。电解液的电导率随着电解液中弱电解液量的增加而增加,而非电解液则不受浓度的影响,因为它们与电导率无关。
比较图
什么是电解质(electrolytes)?
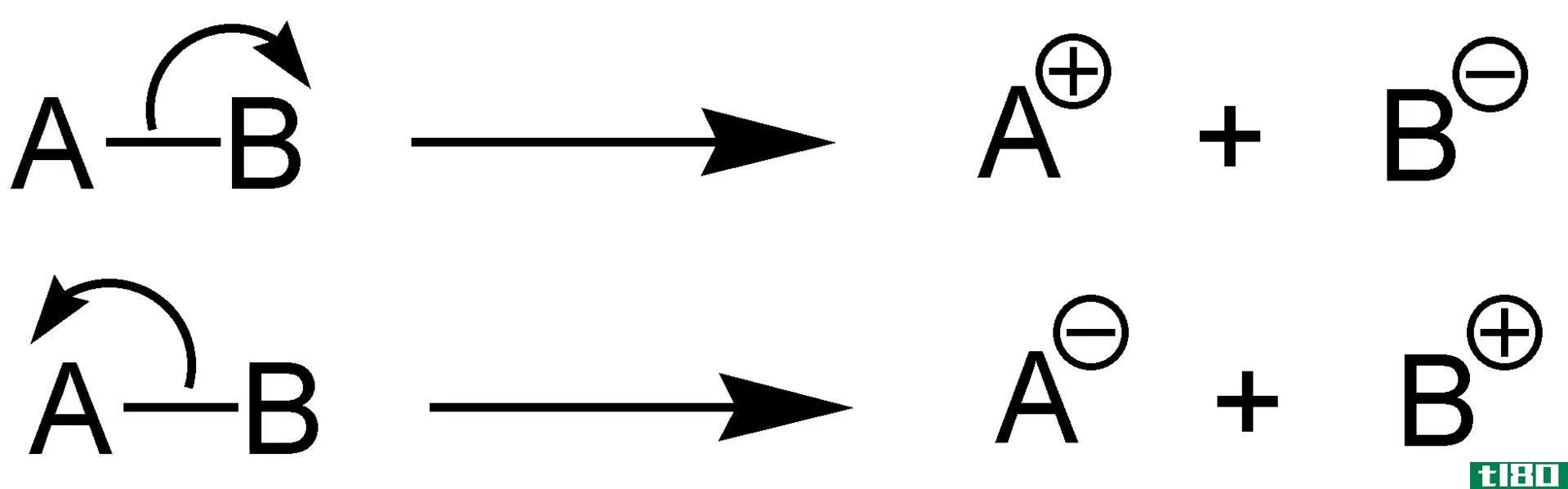
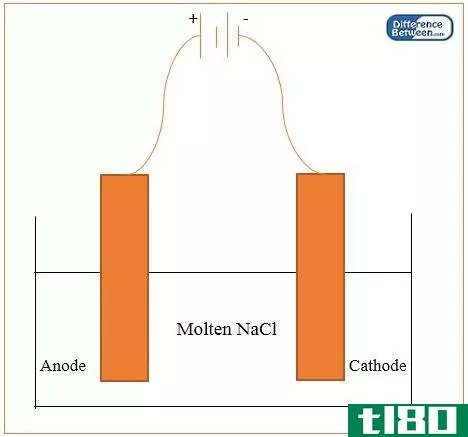
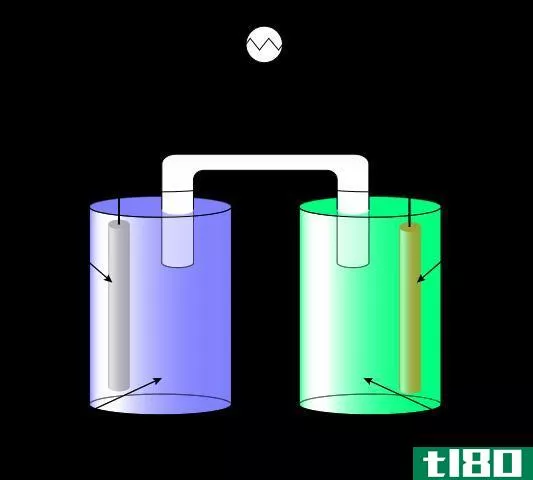
电解质是在水溶液中完全解离并给溶液提供正离子和负离子的化合物。这些离子也能在电解槽中传导电流。电能的传导随溶液或电池温度的升高而增加。它与金属或导体的电流传导正好相反。
它可以在固体或熔融状态下形成阳离子和阴离子。通常由很弱的化学键如价键或离子键组成的电解质。这就是为什么这些化合物包括在离子化合物分类中。电解质也被称为极性化合物。
但纯水或蒸馏水不包括在电解质中,因为它们不能在溶液中形成离子。电解液中的离子能够在电解槽中移动,使溶液发生多次变化。其类型有强电解质和弱电解质。
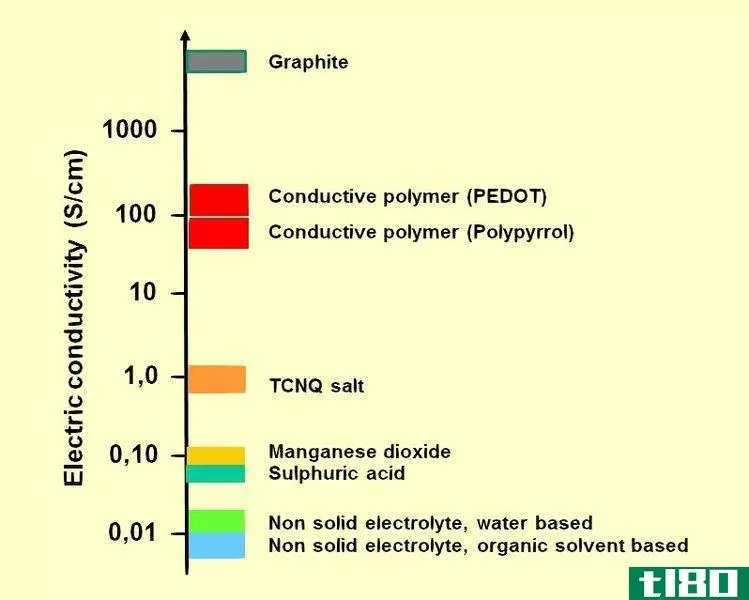
好的电解质有硫酸、硫酸铜溶液、氢氧化钾、乙醇、硫酸锌溶液等。
应用
- 用于**碱金属
- 用于电镀工艺
- 用于金属等的阳极氧化。
什么是非电解质(nonelectrolytes)?
非电解质是指在水溶液中不能完全离解而使溶液中的正离子和负离子的化合物。这些化合物也不具备在电解槽中传导电流的能力。非电解质溶液不受温度的影响,因为它们与电解导电或金属导电无关。
在固体或熔融状态下,它不会形成阳离子或阴离子等离子。非电解质的化合物通常由非常强的化学键(如共价键)组成,需要很大的力才能将化合物分解成离子。这就是为什么这些化合物被包括在共价化合物分类中。
非电解质也被称为非极性化合物。纯水或蒸馏水包含在非电解质中,因为它们不能在溶液中形成离子。非电解质的例子有糖、脂类、脂肪、碳水化合物、葡萄糖和含碳化合物等。
主要区别
- 电解质是在水溶液中能完全解离成离子的化合物;另一方面,非电解质是在水溶液中不能完全解离成离子的化合物。
- 电解质总是电离成正负离子;另一方面,非电解质不容易电离成正负离子。
- 电解质通常由弱化学键结合;在另一方面,非电解质通常由强化学键结合。
- 电解液通常由价键结合;在另一方面,非电解质通常由共价键结合。
- 还有两种类型的电解质;另一方面,没有其他类型的非电解质。
- 在它的侧面,电解液是不可电离的。
- 用于标准电极电位测量的电解液;另一方面,非电解液不用于标准电极电位的测量。
- 在电解液中可以导电,而在非电解液中则不可能导电。
- 电解液中的键很弱,在电流传导过程中很容易断裂;另一方面,电解液中的键是一种很强的键,在电流的传导过程中不会断裂。
- 碱、酸和盐称为电解质;另一方面,碳水化合物、脂肪、脂类、糖和有机化合物称为非电解质。
- 电解质是基本的极性化合物;另一方面,非电解质是基本的非极性化合物。
- 纯水不包括在电解质中;另一方面,纯水可以包含在非电解质中。
- 电解质溶液的导电能力随电解质用量的增加而增加,而非电解质浓度与电导率无关。
- 电解质的例子是钾离子、钠离子等,而非电解质的例子是糖、脂肪、有机化合物等。
结论
以上讨论得出结论:电解质和非电解质都能分解化合物。电解质是在水溶液中离解形成正负离子的化合物,而非电解质是在水溶液中不离解形成正负离子的化合物。